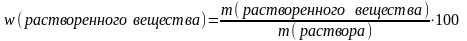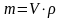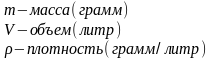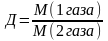Просмотр содержимого документа
«Памятка по химии 9 класс»
| Реакции ионного обмена. Условия протекания.
Реакции ионного обмена – это реакции между ионами, образовавшимися в результате диссоциации электролитов. Реакции ионного обмена протекают до конца в следующих случаях: Если образуется осадок (нерастворимое в воде вещество):
р р н р NaCl + AgNO3 = AgCl + NaNO3 Na+ + Cl- + Ag+ + NO3- = AgCl + Na+ + NO3- Ag+ + NO3- = AgCl
Если образуется газообразное вещество :
Na2C O3 + 2НCl =2NaCl + Н2O + СО2 2Na+ + C O3 2-+ 2Н++ 2С l - = 2Na+ + 2Cl - + Н2O + СО2 C O3 2-+ 2Н+= Н2O + СО2
Если образуется малодиссоциирующее вещество - Н2O:
КОН + НNO3 = КNO3 + Н2O К+ + ОН - + Н + + NO3- = Н2O + К+ + NO3- ОН - + Н + = Н2O
Если в растворах нет таких ионов, которые могут связываться между собой с образованием осадка, газа, или воды Н2O, то реакция является обратимой. Составление ионных уравнений. Правила: Простые вещества, оксиды, нерастворимые кислоты, основания и соли не диссоциируют. Для реакции берут растворы веществ, поэтому даже малорастворимые вещества находятся в растворах в виде ионов. Если малорастворимое вещество образуется в результате реакции, то при записи ионного уравнения его считают нерастворимым.
| Алгоритм составления ионного уравнения реакции | Пример | Записать молекулярное уравнение реакции. Расставить коэффициенты. С помощью таблицы растворимости определить растворимость каждого вещества Составить полное ионное уравнение, записывая растворимые в воде вещества в виде ионов, а нерастворимые вещества, газообразные вещества и воду в виде молекул. Составить сокращённое ионное уравнение, найдя одинаковые ионы в уравнении слева и справа и сократив их.
| 3NaОН + FeCl3 = Fe(ОН)3 + 3NaCl р р н р 3NaОН + FeCl3 = Fe(ОН)3 + 3NaCl
3Na++3ОН- + Fe3++3Cl - = Fe(ОН)3 + 3Na+ +3Cl-
3Na++3ОН- + Fe3++3Cl - = Fe(ОН)3 + 3Na+ +3Cl- 3ОН- + Fe3+ = Fe(ОН)3 |
|


Алгоритм решения задач по уравнению химической реакции
Запомни: Все задачи решаются на основе закона сохранения массы веществ: масса веществ, вступивших в реакцию, равна массе веществ, получившихся в результате реакции.
Порядок решения задач:
Краткая запись условия задачи.
Запись уравнения химической реакции.
Запись известных и неизвестных величин над формулами веществ.
Запись под формулами веществ количества, молярные массы и массы(или молярные объемы и объемы) веществ.
Составление и решение пропорции.
Запись ответа задачи.
Образец решения задачи:
Задача: Сколько граммов оксида меди (II) образовалось при прокаливании 6,4 кг меди.
Д![]() ано: Решение
ано: Решение
m![]() (Cu) = 6,4 кг 6,4 кг Х кг
(Cu) = 6,4 кг 6,4 кг Х кг
Найти:m(CuO) 2Cu + O2 = 2CuO
ν = 2 кмоль ν = 2 кмоль по уравнению реакции
М = 64кг/моль М = 80 кг/моль
m = 128кг m = 160 кг
Составляем пропорцию: 6,4 кг : 128 кг = Х кг : 160 кг
Х = 6,4 * 160 / 128 Х = 8 кг
Ответ: 8 кг
Как увидели задачу- написали уравненье!
Подписали то, что знаем.
Где m, там M, значит можно n найти!
Из молярных отношений, и нашедшегося n –делаем пропорцию!
Ну а m равно тому, M множить с n! (m=M*n)
Формулы для решения задач по химии.
1.Вычисление относительной молекулярной массы вещества:
Mr (H2SO4)=Ar(H)∙2+Ar(S)+Ar(O)∙4=98
2.Вычисление массовой доли элемента в веществе:
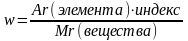
3.Выведение молекулярной формулы вещества:
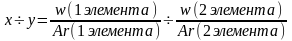
4.Вычисление количества вещества:
а.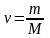
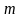 -масса (грамм)
-масса (грамм)
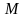 -молярная масса (грамм/моль)
-молярная масса (грамм/моль)
б. только для газообразных веществ при нормальных условиях ( 00 С, 750 мм. рт. ст.)
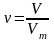
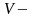 объем (литр)
объем (литр)
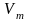 -молярный объем (литр/моль)
-молярный объем (литр/моль) 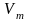 = 22,4 л/моль
= 22,4 л/моль
в. 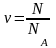
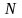 -число частиц
-число частиц
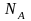 - постоянная Авогадро 6 ∙ 1023
- постоянная Авогадро 6 ∙ 1023
5.Массовая доля растворенного вещества:


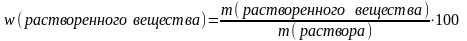
6.Вычисление массы:
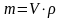
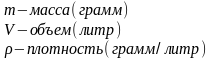
7.Вычисление относительной плотности газов:
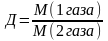
8.Вычисление выхода продукта (%) от теоретически возможного:
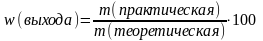
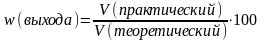








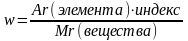
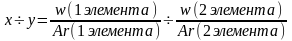
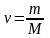
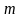 -масса (грамм)
-масса (грамм) 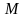 -молярная масса (грамм/моль)
-молярная масса (грамм/моль)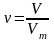
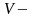 объем (литр)
объем (литр)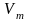 -молярный объем (литр/моль)
-молярный объем (литр/моль) 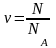
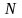 -число частиц
-число частиц 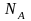 - постоянная Авогадро 6 ∙ 1023
- постоянная Авогадро 6 ∙ 1023