КВАНТОВЫЕ ПОСТУЛАТЫ БОРА

Датский физик, один из создателей современной физики.
Основатель (1920) и руководитель Института теоретической физики в Копенгагене (Институт Нильса Бора);
создатель мировой научной школы; иностранный член АН СССР (1929).
Создал теорию атома,
в основу которой легли планетарная модель атома,
квантовые представления и предложенные им постулаты.
Важные работы по теории металлов, теории атомного ядра и ядерных реакций.
Бор Нильс Хенрик Давид (7.10.1885 -18.11.1962)

Модель Резерфорда
1. В центре атома находится положительно заряженное ядро, занимающее ничтожную часть пространства внутри атома (порядка 10 -12 - 10 -13 см, что в десятки или даже в сотни тысяч раз меньше размеров самого атома).
2. Весь положительный заряд и почти вся масса атома сосредоточены в его ядре (масса электрона равна 1/1823 а.е.м.).
3. В целом атом нейтрален, из чего следует, что число внутриатомных электронов, как и заряд ядра, равно порядковому номеру элемента в периодической таблице.

Модель Резерфорда
Электроны движутся вокруг ядра, подобно тому как планеты движутся вокруг солнца .
Такой характер движения обусловлен действием кулоновских сил

Модель Резерфорда
- крупный шаг в развитии знаний о строении атома .
- наглядная и полезная для объяснения многих экспериментальных данных, в частности была совершенно необходимой для объяснения опытов по рассеянию α-частиц
но
обнаружила и свои недостатки:
неспособна объяснить
не смогла объяснить все свойства атомов,
факт длительного существования атома , т. е. его
устойчивость

Модель Резерфорда
По классическим законам атом должен излучать электромагнитные волны, т.к. электроны движутся с ускорением.
Это должно приводить к уменьшению запаса потенциальной энергии в системе ядро – электрон, а следовательно, и к постепенному уменьшению радиуса орбиты электрона и, наконец, к падению электрона на ядро (за время порядка 10 –8 с атом прекратил бы свое существование) .
НО
- атомы обычно не излучают электромагнитные волны, а
- атомы устойчивы, т.е. электроны не падают на атомные ядра

Модель Резерфорда
Никаких доказательств того, что атомы непрерывно исчезают, не было,
следовательно,
модель Резерфорда в чем-то ошибочна

ПОСТУЛАТЫ БОРА
Бор предположил, что
электрон в атоме не подчиняется законам классической физики.

В 1913 году Бор показал, что поведение микрочастиц нельзя описывать теми же законами , что и макроскопических тела .
Бор предположил , что величины характеризующие микромир, должны квантоваться , т.е. они могут принимать только определенные дискретные значения .
Законы микромира - квантовые законы!
Эти законы в начале 20 столетия еще не были установлены наукой. Бор сформулировал их в виде трех постулатов дополняющих ( и "спасающих") атом Резерфорда.

ПОСТУЛАТЫ БОРА
I постулат
- Атомная система может находиться только в особых стационарных, или квантовых, состояниях, каждому из которых соответствует определенная энергия.

ПОСТУЛАТЫ БОРА
I постулат
I. Электрон может вращаться вокруг ядра не по произвольным, а только по строго определенным (стационарным) круговым орбитам.
Радиус орбиты r и скорость электрона v связаны квантовым соотношением Бора:
mrv =nћ
где m — масса электрона,
n — номер орбиты,
ћ — постоянная Планка (ћ = 1,05∙10-34 Дж∙с).

ПОСТУЛАТЫ БОРА II постулат
2 . При движении по
стационарным орбитам
электрон не излучает и
не поглощает энергии

III постулат
3. Излучение света происходит при переходе атома из стационарного состояния с большей энергией в стационарное состояние с меньшей энергией.

III постулат
При этом энергия испущенного атомом фотона равна разности энергий стационарных состояний , а
частота излучения определяется по формуле:
где Ek - энергия атома в более высоком энергетическом состоянии; Еn - энергия атома в более низком энергетическом состоянии.

Третий постулат позволяет вычислить по известным экспериментальным значениям энергий стационарных состояний частоты излучения атома водорода.
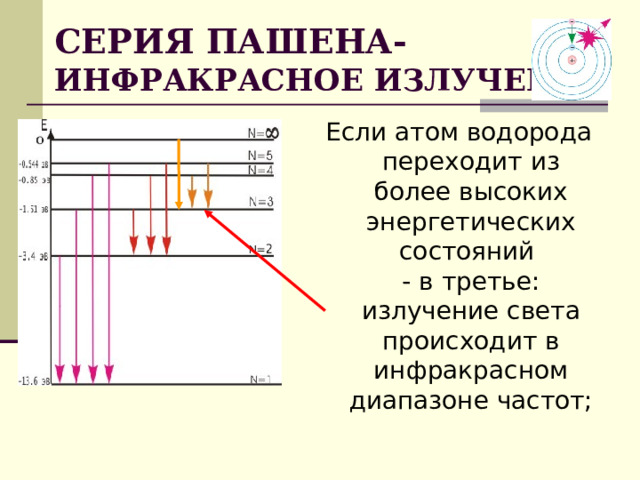
СЕРИЯ ПАШЕНА- ИНФРАКРАСНОЕ ИЗЛУЧЕНИЕ
Если атом водорода переходит из более высоких энергетических состояний - в третье: излучение света происходит в инфракрасном диапазоне частот;
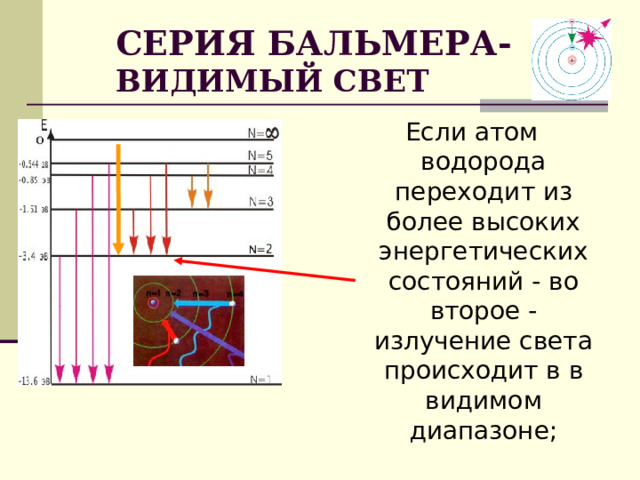
СЕРИЯ БАЛЬМЕРА- ВИДИМЫЙ СВЕТ
Если атом водорода переходит из более высоких энергетических состояний - во второе -излучение света происходит в в видимом диапазоне;
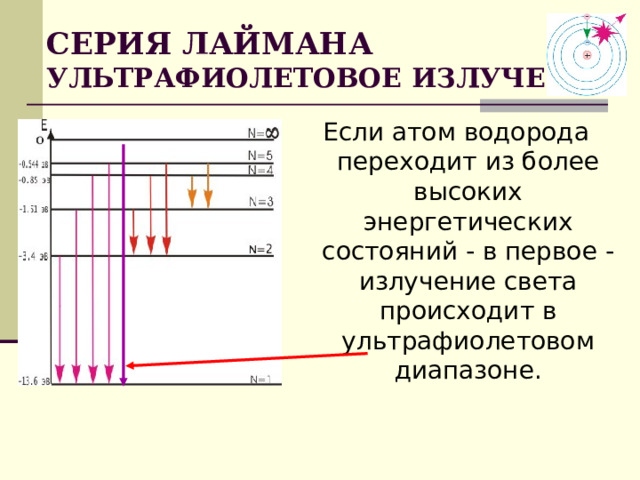
СЕРИЯ ЛАЙМАНА УЛЬТРАФИОЛЕТОВОЕ ИЗЛУЧЕНИЕ
Если атом водорода переходит из более высоких энергетических состояний - в первое - излучение света происходит в ультрафиолетовом диапазоне.

ПОСТУЛАТЫ БОРА
Если атом переходит в одно из возбужденных состояний, долго оставаться там он не может: атом самопроизвольно (спонтанно) переходит в основное состояние.
ИК видимый УФ

Свои постулаты Бор применил для объяснения излучения и поглощения света атомом водорода.
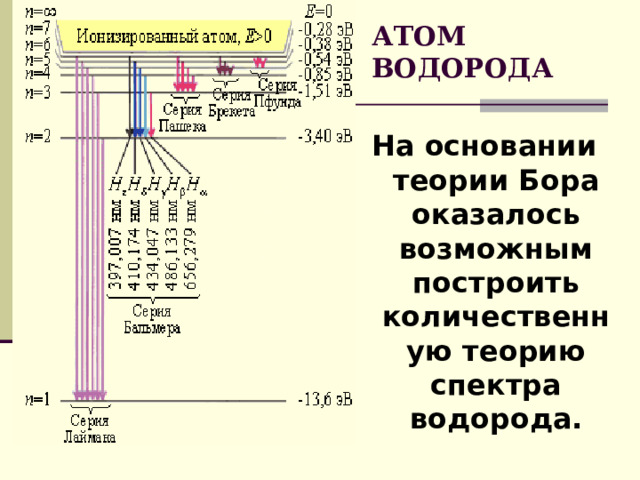
АТОМ ВОДОРОДА
На основании теории Бора оказалось возможным построить количественную теорию спектра водорода.

АТОМ ВОДОРОДА
ИНФРАКРАСНОЕ
ВИДИМЫЙ СВЕТ
УЛЬТРАФИОЛЕТ

спектры излучения
Спектр нагретого вещества в газообразном состоянии состоит из узких линий разного цвета. Такой спектр называется линейчатым спектром излучения . Для получения такого спектра используют дуговой или искровой разряд . Линейчатый спектр излучения у каждого химического элемента свой, не совпадающий со спектром другого химического элемента.

СПЕКТРЫ ИСПУСКАНИЯ
Расчеты Бора привели к согласию с экспериментально определенными частотами.
Частоты излучений можно определить по спектрам атомов: на фоне сплошного спектра поглощения (на черном фоне) видны цветные линии излучения, соответствующие определенным длинам волн или частотам

СПЕКТРЫ ПОГЛОЩЕНИЯ
Поглощение света- процесс, обратный излучению: атом переходит из низших энергетических состояний в высшие. При этом атом поглощает излучение тех же частот , которые излучает при обратных переходах.

СПЕКТРЫ ИСПУСКАНИЯ
1-сплошной
2- натрия
3-водорода
4-гелия
СПЕКТРЫ ПОГЛОЩЕНИЯ
5-солнечный
6-натрия
7-водорода
8-гелия

ТРУДНОСТИ ТЕОРИИ
Построить количественную теорию уже для атома гелия на основе боровских представлений оказалось затруднительным

В современной физике с помощью квантовой механики построена количественная теория излучения и поглощения света.
В рамках классической физики оказалось невозможным ответить на многие вопросы, связанные с поведением электронов внутри атомов, с излучением и поглощением атомов

Домашнее задание:
- подготовить конспект по материалам презентации;
- подготовить ответ на вопрос: «В чем «трудность» теории Бора?»














































