Практическая работа № 5
«Получение, собирание и распознавание газов».
Цели занятия: Совершенствовать умения выполнять химический эксперимент по получению, собиранию и распознаванию газов.
Техника безопасности: аккуратно работать с реактивами и приборами; не смешивать реактивы без согласия с заданием; тушить спиртовку, накрывая колпачком ,приступайте к работе с химическими реактивами после изучения инструкции.
Ход работы.
Задание 1.
Проверьте свою готовность к работе – выберите один правильный ответ.
1. При большой концентрации углекислого газа у человека может развиться:
А.мигрень Б.удушье В.гипертония Г.рвота
Б. раствор серной кислоты и железо Г. угольная кислота и цинк
2.Газообразные вещества, которые можно собирать способом вытеснения воды:
А. аммиак и водород В. углекислый газ и озон
Б. кислород и метан Г. этилен и сероводород
3.В природе углекислый газ образуется:
А.при сжигании и гниении Б.во время дождя В.при понижении температуры ниже 0 градусов
4.Для обнаружения кислорода можно использовать:
А. бромную воду В. тлеющую лучинку
Б. хлороводород Г. известковую воду
4.Газы, которые способом вытеснения воздуха собирают в сосуд, расположенный вверх дном:
А. аммиак и кислород В. метан и водород
Б. этилен и углекислый газ Г. озон и угарный газ
5.Газ без запаха:
А. аммиак Б. озон В. сероводород Г. метан
6. Водород в лаборатории можно получить
а) при взаимодействии кислоты с любым металлом
б) разложением воды
в) реакцией активного металла с водой
г) разложением солей нитратов
7.Для обнаружения углекислого газа можно использовать:
А. бромную воду В. тлеющую лучину
Б. фенолфталеин Г. известковую воду
8.Укажите газ, который не горит, не поддерживает горения и поэтому применяется для тушения пожаров: А) СО2 Б) СН4 В) С2Н2 Г) СO
Опыт 1. Получение, собирание и распознавание водорода. Соберите прибор для получения газов и проверьте его на герметичность (как проверить прибор на герметичность). В пробирку положите 1-2 гранулы цинка и прилейте в неё 1-2 мл соляной кислоты. Закройте пробирку пробкой с газоотводной трубкой и наденьте на кончик трубки ещё одну пробирку. (Объясните, почему водород собираем в пробирке вверх дном). Что наблюдаете?
Подождите некоторое время, чтобы пробирка заполнилась выделяющимся газом. Проверьте водород на чистоту. Снимите пробирку с водородом и, не переворачивая её, поднесите к горящей спиртовке. Если водород чистый, то мы услышим глухой хлопок, а если
Оформите отчет о выполнении в виде таблицы.
| Действия 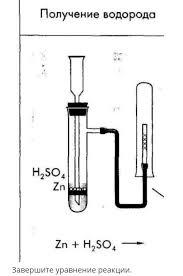
| Наблюдения | Уравнения реакций. Выводы. |
|
| 1.Что происходит при взаимодействии цинка с Н2SO4? Составьте УХР и дайте ее характеристику по всем изученным признакам классификации химических реакций. 2. Рассмотрите записанную реакцию с точки зрения процессов окисления-восстановления 3.Физические свойства Н2.Как происходит сгорание водорода? 4. Как можно распознать водород? |
Опыт 2. Получение, собирание и распознавание кислорода. Соберите прибор, как показано в учебнике на рисунке 109, и проверьте его на герметичность. Пробирку примерно на ¼ объема заполните перманганатом калия KMnO4, у отверстия расположите рыхлый комочек ваты. Закройте пробирку пробкой с газоотводной трубкой. Укрепите пробирку в лапке штатива так, чтобы конец газоотводной трубки доходил почти до дна сосуда для сбора кислорода.
Сначала 2-3 движениями пламени прогрейте всю пробирку (почему?) с перманганатом калия, а затем прогревайте только в том месте, где находится вещество.
Наличие кислорода в сосуде проверяйте тлеющей лучинкой (Что наблюдаете?)
Оформите отчет о выполнении в виде таблицы.
| Действия | Наблюдения | Уравнения реакций. Выводы. |
| 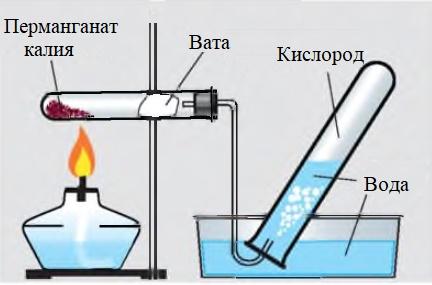 | | 1. Составьте уравнение реакции и дайте ее характеристику по всем изученным признакам классификации химических реакций. 2. Рассмотрите записанную реакцию с точки зрения процессов окисления-восстановления. 3. Опишите физические свойства кислорода 4.Как можно распознать кислород? |
| | | |
Опыт 3. Получение, собирание и распознавание углекислого газа.
Закрепите пробирку с карбонатом кальция в штативе, добавьте в нее раствор соляной кислоты и быстро закройте пробкой с газоотводной трубкой. Что наблюдаете? Запишите уравнение реакции.
Соберите газ в сухую пробирку и внесите в верхнюю часть пробирки горящую лучинку. Что наблюдаете?
В пробирку налейте 1-2 мл прозрачного раствора известковой воды и опустите туда газоотводную трубку. Что наблюдаете? Запишите уравнение реакции.
Оформите отчет о выполнении в виде таблицы.
| Действия | Наблюдения | Уравнения реакций. Выводы. |
| 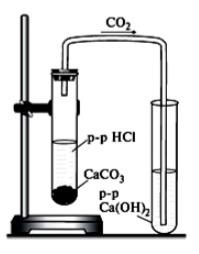 | | 1. Что происходит при взаимодействии мрамора с соляной кислотой? Составьте уравнение реакции и дайте ее характеристику по всем изученным признакам классификации химических реакций. 2. Рассмотрите проведенную реакцию в свете теории электролитической диссоциации. 3.Физические свойства СО2 4.Опишите два способа распознавания углекислого газа. |
| | |
|
Вывод:


























