Просмотр содержимого документа
«Практическая работа "Гидролиз солей"»
Практическая работа № 1
Гидролиз солей
(теория в учебнике с.107) (ЕГЭ № 21, 1 часть, 1 балл, время выполнения 2-3 минуты)
Цель работы:
Оборудование:
Для характеристики среды водного раствора используют водородный показатель рН.
(лат. pondus Hydrogenii - «вес водорода»); произносится «пэ-аш».
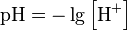

Опыт 1. Определение рН среды для растворов
Определите рН растворов и заполните таблицу.
| № | Формула соли | Значение рН | Каким основанием и какой кислотой образована соль | Наличие гидролиза | Гидролиз по катиону или аниону | Уравнение реакции |
| H2O |
|
|
|
|
|
| H2SO4 |
|
|
|
|
|
| NaOH |
|
|
|
|
|
| NaCl |
|
|
|
|
|
| Na2CO3 |
|
|
|
|
|
| AlCl3 |
|
|
|
|
|
| ZnSO4 |
|
|
|
|
|
| Na2SO3 |
|
|
|
|
|
Гидролиз характерен для следующих катионов: NH4+ ; Zn2+ ; Cu2+ ; Fe2+; Fe3+; Cr3+; Al3+ (cоли магния гидролизуются незначительно, соли серебра не гидролизуются)
Гидролиз характерен для следующих анионов:CH3COO - ; S2- ; F- ; SO32- ; SiO32- ; CO32- ; PO43-
Уравнения реакций гидролиза солей
Взаимодействие солей с водой называют ионным гидролизом.
а) Обратимый гидролиз
NH4Cl + H2O
ZnCl2 + H2O
б) Необратимый гидролиз
Al2S3 + H2O
в) Совместный гидролиз
Na2S + AlBr3 + H2O
Na2SO3 + Cr2(SO4)3 + H2O
Опыт 2. Совместный гидролиз
Поместите в пробирку 2 мл раствора хлорида алюминия, затем добавляйте по каплям раствор карбоната натрия. Запишите наблюдения, составьте уравнение реакции.
Задания № 21 ЕГЭ-2022
Для веществ, приведённых в перечне, определите характер среды их водных растворов, имеющих одинаковую концентрацию (моль/л).
1) фенол
2) хлоруксусная кислота
3) гидроксид калия
4) фторид натрия
З



 апишите номера веществ в порядке убывания значения рН их водных растворов.
апишите номера веществ в порядке убывания значения рН их водных растворов.
Для веществ, приведённых в перечне, определите характер среды их водных
растворов, имеющих одинаковую концентрацию (моль/л).
1) пероксид водорода
2) нитрат алюминия
3) гидроксид натрия
4) формиат калия 



Запишите номера веществ в порядке возрастания значения рН их водных
растворов.
3. Для веществ, приведённых в перечне, определите характер среды их водных
растворов, имеющих одинаковую концентрацию (моль/л).
1) хлорат калия
2) азотная кислота
3) сульфид натрия
4) серная кислота
Запишите номера веществ в порядке возрастания значения рН их водных
растворов.




Для веществ, приведённых в перечне, определите характер среды их водных
растворов, имеющих одинаковую концентрацию (моль/л).
1) ацетон
2) уксусная кислота
3) гидроксид натрия
4) карбонат калия
З



 апишите номера веществ в порядке убывания значения рН их водных растворов.
апишите номера веществ в порядке убывания значения рН их водных растворов.
Для веществ, приведённых в перечне, определите характер среды их водных
растворов, имеющих одинаковую концентрацию (моль/л).
1) гипохлорит калия
2) йодид аммония
3) йодид цезия
4) йодоводород
З



 апишите номера веществ в порядке убывания значения рН их водных растворов.
апишите номера веществ в порядке убывания значения рН их водных растворов.