
Автор: Пунгина А.П. учитель биологии МБОУСОШ с. Болдыревка

Меняя каждый миг Свой образ прихотливый, Капризна, как дитя, и призрачна как дым, Кипит повсюду жизнь в тревоге суетливой, Великое смешав с ничтожным и смешным… С.Я. Надсон .
Чему посвящены строки из стихотворения Надсона? Что такое жизнь? Откуда она взялась на земле? Этим вопросом задавались многие века и многие ученые. Среди них путешественник и естествоиспытатель Александр Гумбольт, Фридрих Энгельс, которые определили «жизнь, как … способ существования белковых тел…»

- Белки – это сложные органические соединения, представляющие собой высокомолекулярные полимеры – макромолекулы, - построенные из стандартных субмолекулярных блоков, соединенных химической связью особого типа и образующих специфические пространственные конфигурации. Первым установил блочный принцип строения белка и химическую структуру блоков выдающийся немецкий биохимик Эмиль Герман Фишер (1852 -1919). Белки называют также протеинами.

- Каждый тип белка имеет уникальный химический состав и структуру, которыми определяются его биологические свойства.
- в настоящее время приняты три разные классификации белков:
- 1) по составу, 2) по структуре, 3) по функциям

Примерный химический состав
белка
С 50 – 55%
О 19 – 24%
Н 6,5 – 7,3%
N 15 – 19%
S 0,2 -2,4%

- На долю белков приходится более 50% общей массы органических соединений животной клетки:
в мышцах – 80%
в коже – 63%
в печени – 57%
в мозге – 45%
в костях -28%

- Химические формулы некоторых белков:
Пенициллин С 16 Н 18 О 4 N 2
Казеин С 1864 Н 3021 О 576 N 468 S 2
Гемоглобин С 3032 Н 4816 О 872 N 780 S 8 F е 4
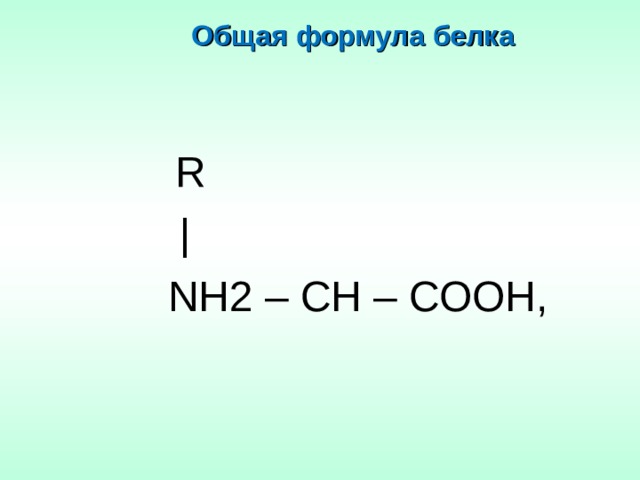
Общая формула белка
R
|
N Н2 – СН – СООН,

Белки (полипептиды) биополимеры, построенные из остатков
-аминокислот, соединенных пептидными связями.
Пептидной связью называют амидную связь – CO – NH –, образованную при взаимодействии -аминокислот за счет реакции между аминогруппой NH 2 одной молекулы и карбоксильной группы COOH – другой.
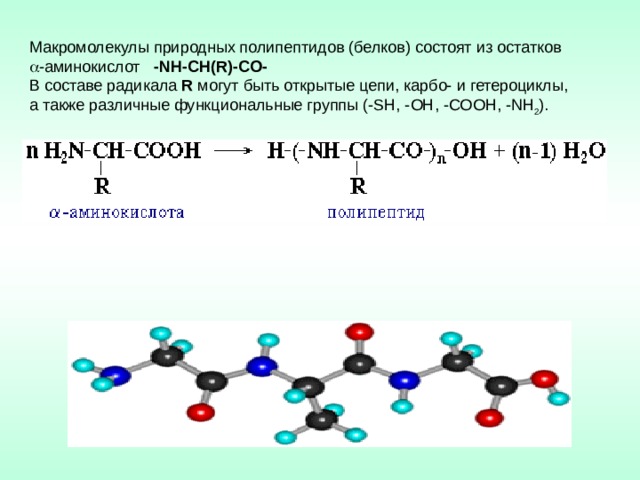
Макромолекулы природных полипептидов (белков) состоят из остатков
-аминокислот - NH - C Н( R )-С O -
В составе радикала R могут быть открытые цепи, карбо- и гетероциклы,
а также различные функциональные группы (- SH , - OH , - COOH , - NH 2 ).

Схема образования полипептида
Схема образования полипептида

Макромолекулы белков имеют строго упорядоченное химическое и
пространственное строение, исключительно важное для проявления ими определенных биологических свойств.
Выделяют 4 уровня структурной организации белков:
Первичная структура
Вторичная структура
Третичная структура
Четвертичная структура

Первичная структура – определенный набор и последовательность
-аминокислотных остатков в полипептидной цепи .

Вторичная структура –
конформация полипептидной цепи, закрепленная множеством водородных связей между группами N–H и С=О.
Одна из моделей вторичной структуры – -спираль .

Третичная структура
– форма закрученной спирали в пространстве,
образованная главным образом за счет дисульфидных мостиков -S-S-,
водородных связей, гидрофобных и ионных взаимодействий.

Четвертичная структура
– агрегаты нескольких белковых макромолекул (белковые комплексы), образованные за счет взаимодействия разных полипептидных цепей.


Демонстрация опыта:
- Опыт N 1 Белок +нагревание --- денатурация (выпадение осадка)
- Опыт N 2 Белок + фенол --- денатурация (выпадение осадка)
- Опыт N 3 Белок + СиSО4 --- денатурация (выпадение осадка)

Растворимость
Гидролиз
При гидролизе белков образуются аминокислоты.
Денатурация.
При нагревании белков происходит разрушение сначала четвертичной, потом третичной структуры белка и так далее. При прекращении нагревания молекулы белка снова объединяются в сложные структуры. Следовательно, полностью разрушить белок можно только при очень высоком нагревании, при котором разрушается первичная структура – полипептидная цепь.
Цветные реакции:
Для белков характерно сворачивание и образование жёлтого осадка при действии азотной кислоты (ксантопротеиновая реакция) и образование фиолетового окрашивания при взаимодействии белка с гидроксидом меди ( II) ( биуретовая реакция)

Функции белков в природе :
- каталитические (ферменты);
- регуляторные (гормоны);
- структурные (кератин шерсти, фиброин шелка, коллаген);
- двигательные (актин, миозин);
- транспортные (гемоглобин);
- запасные (казеин, яичный альбумин);
- защитные (иммуноглобулины) и т.д.


Значение белков и ферментов
- Среди белков выделяется особый и очень важный подкласс - ферменты
- Ферменты – белки, обладающие каталитической активностью, т.е. ускоряющие протекание реакций. Все ферменты высокоспецифичные к своему субстрату и, как правило, катализируют только одну вполне определенную реакцию. На работу ферментов влияют многочисленные факторы: рН, температура, ионный состав среды и.т.д.
- Широко известны заболевания, вызываемые ферментной недостаточностью. Пример: неперевариваемость молока (нет фермента лактазы); гиповитаминозы (витаминная недостаточность) Определение активности ферментов в биологических жидкостях имеет большое значение для диагностики заболевания. Например, по активности ферментов в плазме крови определяют вирусный гепатит.
Самопроверка
1.Наличие в белках пептидной связи предположил ученный:
А) М.В. Ломоносов ; Б) А.Я. Данилевский;
В) В.В. Марковников; Г) Э.Г. Фишер.
2Какую функцию выполняет белок инсулин в организме?
А) Способствует свертыванию крови;
Б) образует комплексы с инородными белками;
В) переносит О2 в мышцах;
Г ) регулирует обмен глюкозы.
3. Имитацией третичной структуры белковой молекулы является:
А) клубок ниток; Б) свернутая в клубок электроспираль;
В) телевизионная антенна; Г) выпрямленный телефонный шнур.
4.Как называется белок, у которого первым удалось расшифровать первичную структуру?
А) Рибонуклеаза; Б) Инсулин ; В) Глобин; Г) Миоглобин.
5.Биологическими катализаторами – веществами белковой природы – называются:
А) Гормоны ; Б) Ферменты ; В) Витамины; Г) Углеводы.
6. Какая структура белковой молекулы определяет специфическую биологическую активность белка?
А) Четвертичная ; Б) Третичная; В) Вторичная; Г) Первичная.
7. Какой вид химической связи поддерживает вторичную структуру белковой молекулы?
А) Водородная ; Б) Ионная; В) Пептидная; Г) Гидрофобная.
8.Укажите элементный состав простых белков:
А) С,Н ; Б) С, Н, О, N , S ; В) С, Н, N ; Г) Вся таблица Менделеева.

Наш урок мы начали со слов «жизнь».
Закончить урок нам хочется этим же понятием «Жить – это значит узнавать!
Жить – это значит мечтать широко и привольно!
Жить – это значит творить, трудясь без устали,с неисчерпаемым вдохновением!

СПАСИБО ЗА ВНИМАНИЕ

В подготовке презентации использованы:
- И.Г. Хомченко. Общая химия.
- В.Г. Жириков. Органическая химия.
- В.Б. Захаров, С,Г. Мамонтов, В.И. Сивоглазов. Биология. Общие закономерности: Учебник для 10-11-х классов общеобразовательных учебных заведений.
- А.О. Рувинский, Л. В. Высоцкая, С.М.Глаголев. Общая биология: Учебник для 10-11 класса с углубленным изучением.
5. Ресурсы Интернет (все фотографии, рисунки)
6. Информационно-образовательные ресурсы по биологии.










































