
Тема: «Сущность процесса электролитической диссоциации»
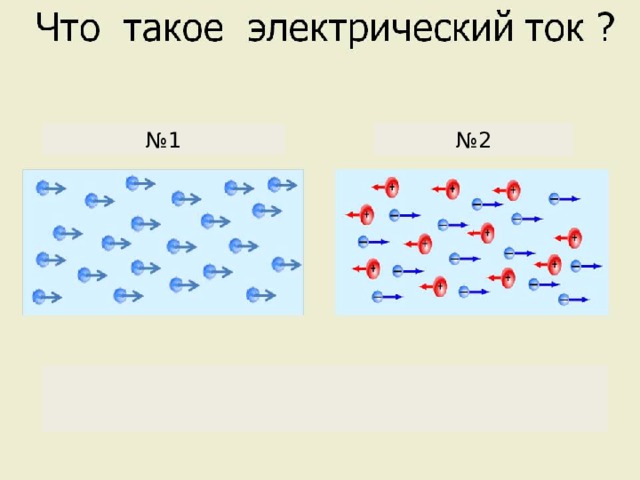
- Учащиеся вспоминают из курса физики, что такое электрический ток (упорядоченное движение носителей электрических
- зарядов).
№ 1
№ 2

Какие частицы являются переносчиками тока в металлах?
- Металлы — это проводники первого рода.
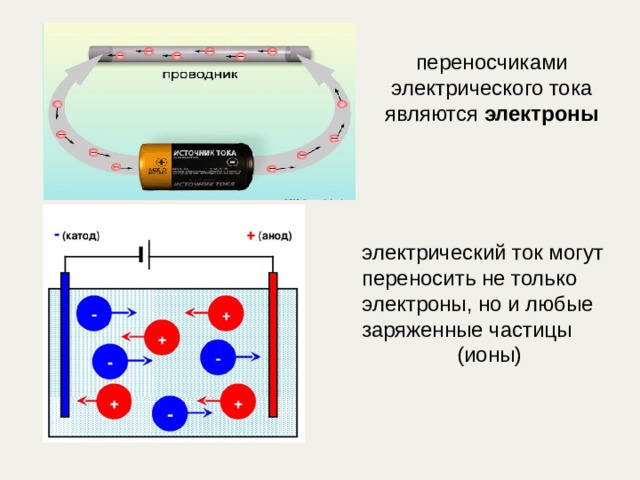
переносчиками электрического тока являются электроны
электрический ток могут переносить не только электроны, но и любые заряженные частицы
(ионы)
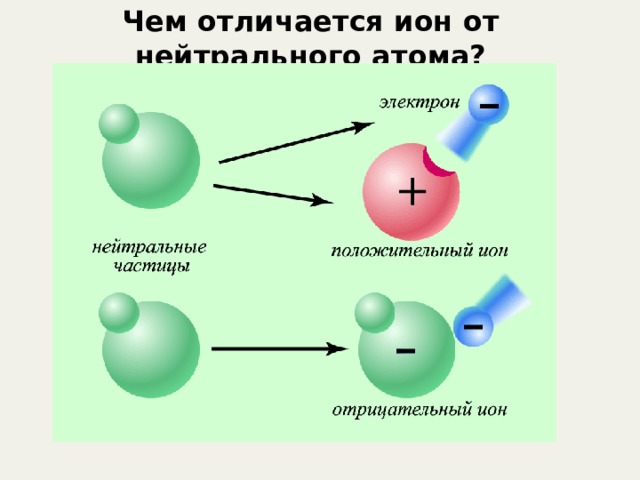
Чем отличается ион от нейтрального атома?
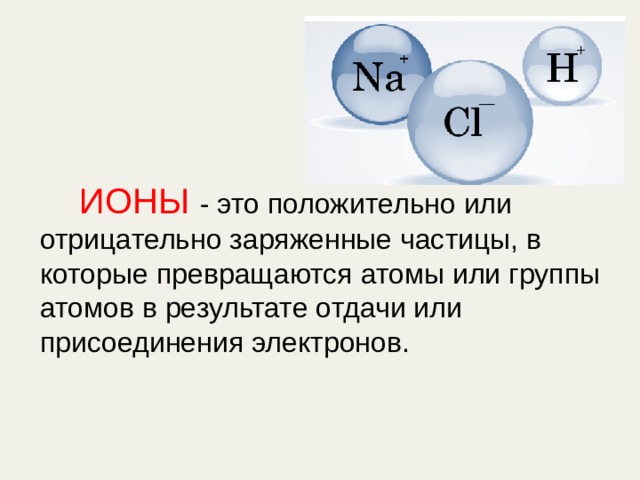
ИОНЫ - это положительно или отрицательно заряженные частицы, в которые превращаются атомы или группы атомов в результате отдачи или присоединения электронов.

Чем отличается металлический натрий от иона натрия?
Атом натрия Na 0 Ион натрия Na +
11 p + , 12n 0 , 10 e
11 p + , 12n 0 , 11 e
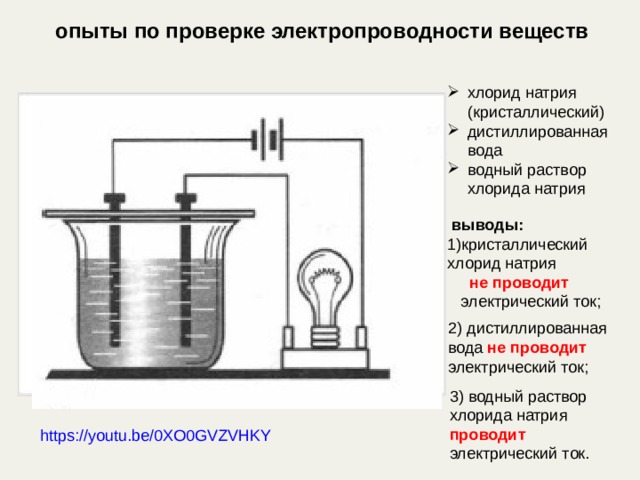
опыты по проверке электропроводности веществ
- хлорид натрия (кристаллический)
- дистиллированная вода
- водный раствор хлорида натрия
выводы:
- кристаллический хлорид натрия
не проводит
электрический ток;
2) дистиллированная вода не проводит электрический ток;
3) водный раствор хлорида натрия проводит электрический ток.
https://youtu.be/0XO0GVZVHKY

Фарадей Майкл
22. IX. 1791 – 25. VIII. 1867
Английский физик и химик.
В первой половине 19 в. ввел понятие
об электролитах и неэлектролитах.

Теория электролитической диссоциации (ТЭД)
В 1887 году шведский учёный
С. Аррениус для объяснения
особенностей водных растворов
веществ предложил теорию
электролитической диссоциации.
В дальнейшем эта теория была
развита многими учёными.
Сванте Аррениус
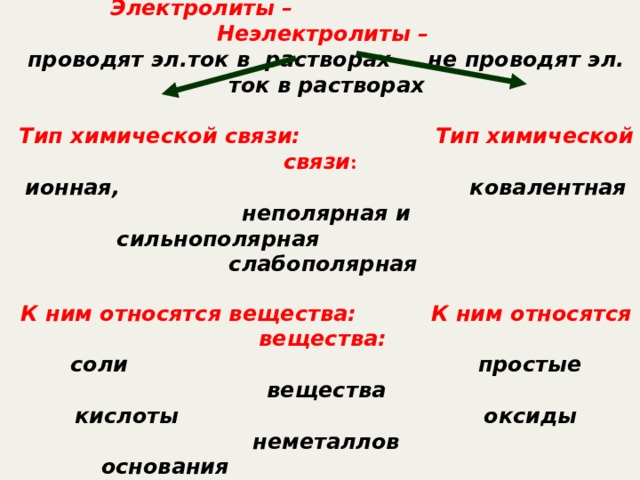
Вещества
Электролиты – Неэлектролиты –
проводят эл.ток в растворах не проводят эл. ток в растворах
Тип химической связи: Тип химической связи :
ионная, ковалентная неполярная и
сильнополярная слабополярная
К ним относятся вещества: К ним относятся вещества:
соли простые вещества
кислоты оксиды неметаллов
основания органические вещества
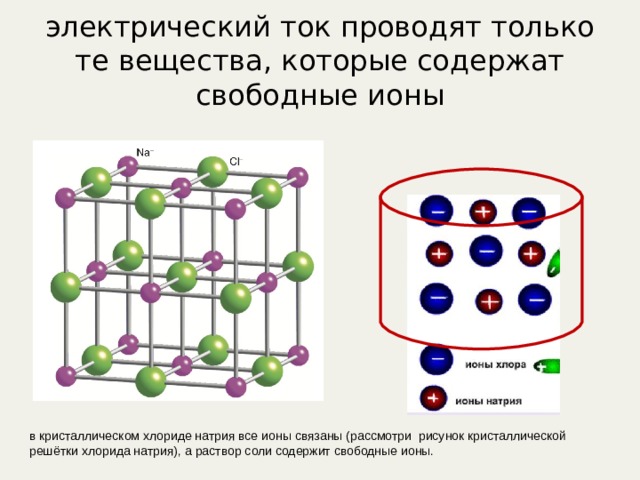
электрический ток проводят только те вещества, которые содержат свободные ионы
в кристаллическом хлориде натрия все ионы связаны (рассмотри рисунок кристаллической решётки хлорида натрия), а раствор соли содержит свободные ионы.

Процесс распада электролита на ионы при растворении его в воде или расплавлении называется электролитической диссоциацией.
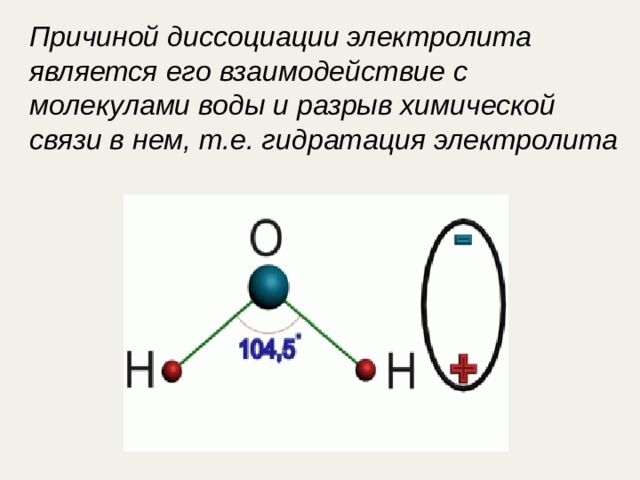
Причиной диссоциации электролита является его взаимодействие с молекулами воды и разрыв химической связи в нем, т.е. гидратация электролита
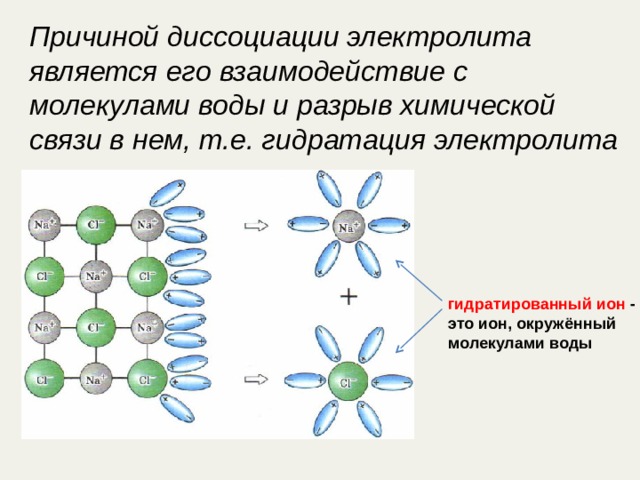
Причиной диссоциации электролита является его взаимодействие с молекулами воды и разрыв химической связи в нем, т.е. гидратация электролита
гидратированный ион - это ион, окружённый молекулами воды
+ -
+ -
+ -
+ -
+ -
+ -
+ -
+ -
+ -
+ -
+ -
+ -
+ -
+ -
+ -
+ -
+ -
+ -
+ -
+ -
+ -
+ -
+ -
+ -
+ -
+ -
+ -
+ -
+ -
+ -
+ -
+ -
+ -
+ -
+ -
+ -
+ -
+ -
+ -
+ -
+ -
+ -
+ -
+ -
+ -
+ -
+ -
+ -
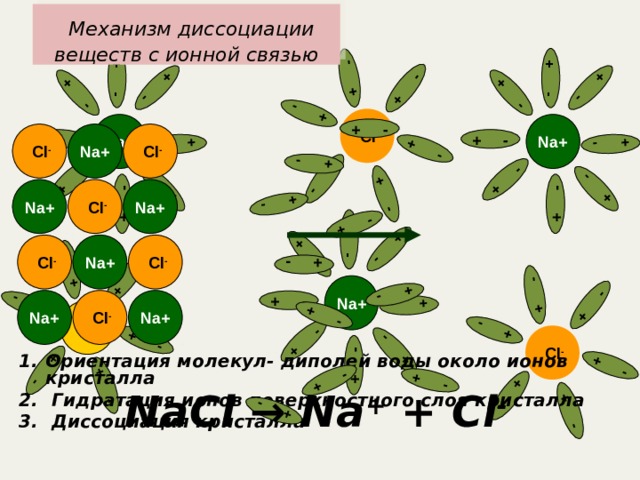
Механизм диссоциации веществ с ионной связью
Cl -
Na+
Na+
+ -
Cl -
Cl -
Na+
+ -
+ -
Na+
Cl -
Na+
Cl -
Cl -
Na+
Na+
Na+
Cl -
Na+
+ -
Cl -
Cl -
- Ориентация молекул- диполей воды около ионов кристалла
- Гидратация ионов поверхностного слоя кристалла
- Диссоциация кристалла
NaCl → Na + + Cl -
Сущность процесса электролитической диссоциации веществ с ионной связью
- ориентация молекул воды около ионов, образующих кристалл;
- взаимодействие молекул воды с ионами поверхностного слоя кристалла (гидратация);
- распад кристалла на гидратированные ионы (диссоциация).
NaCl = Na + Cl
+ -
+ -
+ -
+ -
+ -
+ -
+ -
+ -
+ -
+ -
+ -
+ -
+ -
+ -
+ -
+ -
+ -
+ -
+ -
+ -
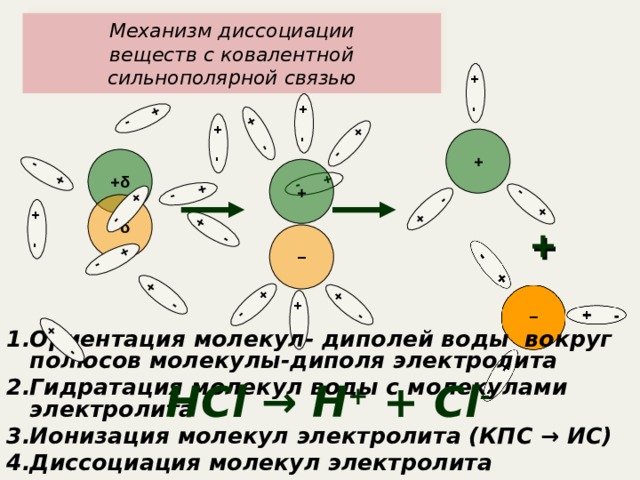
Механизм диссоциации веществ с ковалентной сильнополярной связью
+
+ δ
+
− δ
+
−
- Ориентация молекул- диполей воды вокруг полюсов молекулы-диполя электролита
- Гидратация молекул воды с молекулами электролита
- Ионизация молекул электролита (КПС → ИС)
- Диссоциация молекул электролита
HCl → H + + Cl -

Сущность процесса электролитической диссоциации веществ с ковалентной полярной связью
- ориентация молекул воды вокруг полюсов молекулы электролита;
- взаимодействие молекул воды с молекулами электролита;
- ионизация электролита (превращение ковалентной полярной связи в ионную);
- диссоциация (распад) молекул электролита на гидратированные ионы.
Н Cl = Н + Cl

Кристаллогидраты — кристаллы, содержащие молекулы воды и образующиеся, если в кристаллической решётке катионы образуют более прочную связь с молекулами воды, чем связь между катионами и анионами в кристалле безводного вещества.
Кристаллизационная вода – это вода , входящая в структуру кристаллов некоторых веществ, называемых кристаллогидратами.

Рефлексия
- Я умею определять ….. и …..
- Я умею записывать … и ….
- Я знаю, что ……..

Домашнее задание
- §6 прочитать, выучить основные определения.
- Выполнить задания 1- 4







































