

название «галоген» происходит от слов рождать соль
Фтор
Хлор
Бром
Йод
Астат

История открытия фтора
В 1886 году французский химик А. Муассан, используя электролиз жидкого фтороводорода, охлажденного до температуры –23°C (в жидкости должно содержаться немного фторида калия, который обеспечивает ее электропроводимость), смог на аноде получить первую порцию нового, газа. В первых опытах для получения фтора Муассан использовал очень дорогой электролизер, изготовленный из платины и иридия. При этом каждый грамм полученного фтора «съедал» до 6 г платины.
Анри Муассан
(1852 – 1907)

История открытия хлора
В 1774 году шведский ученый К. Шееле открыл хлор, который принял за сложное вещество и назвал "дефлогистированной соляной кислотой".
В 1807 году английский химик Гемфри Дэви получил тот же газ. Он пришел к выводу, что получил новый элемент и назвал его "хлорин" (от "хлорос" - желто-зеленый).
В 1812 году Гей-Люсеок дал газу название хлор.
Карл Вильгельм Шееле
(1742 – 1786)

История открытия брома
В 1825 году французский химик А.Ж.Балар при изучении маточных рассолов выделил темно-бурую жидкость, который он назвал - "мурид" (от латинского слова muria , означающего "рассол"). Комиссия Академии, проверив это сообщение, подтвердила открытие Балара и предложила назвать элемент бромом (от "бромос", с греческого "зловонный").
Антуан Жером Балар (1802 – 1876)

История открытия йода
В 1811 году французский химик Бернар Куртуа открыл иод путём перегонки маточных растворов от своего азотнокислого кальция с серной кислотой Чтобы другие химики могли изучать новое вещество, Б. Куртуа подарил его (правда, очень небольшое количество) фармацевтической фирме в Дижоне.
В 1813 году Ж.-Л.Гей-Люссак подробно изучил этот элемент и дал ему современное название. Название "иод" происходит от греческого слова "иодэс" - "фиолетовый" (по цвету паров).
Бернар Куртуа (1777 – 1838 )

История открытия астата
В 1869 г Д.И.Мендеелеев предсказал его существование и возможность открытия в будущем (как «эка-иод»).
Впервые астат был получен искусственно в 1940 г открыт Д.Корсоном, К.Маккензи и Э.Сегре (Калифорнийский университет в Беркли) . Для синтеза изотопа 211 At они облучали висмут альфа-частицами.
В 1943-1946 годах изотопы астата были обнаружены в составе природных радиоактивных рядов. Астат является наиболее редким элементом среди всех, обнаруженных в природе. В поверхностном слое земной коры толщиной 1,6 км содержится всего 70 мг астата.
Периодическая система химических элементов Д.И.Менделеева
Периоды
Ряды
Группы элементов
I
VII
III
VI
V
IV
VIII
II
Галогены
He
H
1
2
1
I
1.00797
4,003
Водород
Гелий
Ne
Be
O
N
В
Li
C
F
5
9
1 0
4
6
3
8
7
II
2
10 .811
18.9984
20,18
15 .996
14.0 067
12,011
9 ,012
6,9 39
Кислород
Азот
Бор
Углерод
Литий
Вериллий
фтор
Неон
Ar
Na
Cl
Al
S
Si
P
Mg
11
1 8
1 6
1 5
13
1 4
1 2
1 7
III
3
28,086
39,948
32,064
30,9738
35,453
22,9898
24,312
26,9815
Натрий
Хлор
Фосфор
Алюминий
Сера
Кремний
Магний
Аргон
Cr
V
Ti
S с
Co
Ni
Fe
Mn
K
Ca
28
2 3
26
24
25
27
22
21
20
19
4
IV
44.956
50.942
51.996
55.847
40,08
54.938
58.71
47.90
39.102
58.933
Хром
Ванадий
Железо
Скандий
Кальций
Кобальт
Калий
Никель
Титан
Марганец
Br
Kr
As
Ga
Cu
Zn
Se
Ge
36
35
31
29
30
34
33
32
5
83,8
74.9216
78.96
79.904
72.59
69.72
63.54 6
65 . 37
Медь
Галлий
Криптон
Цинк
Бром
Мышьяк
Селен
Германий
T с
Rh
Ru
Pd
Rb
Nb
Sr
Mo
Y
Zr
45
41
39
40
44
42
46
38
4 3
37
6
V
85.47
106.4
95.94
92.906
88.9059
91.224
99
101.07
87.62
102.905
Родий
Цирконий
Рубидий
Рутений
Технеций
Палладий
Молибден
Ниобий
Иттрий
Стронций
In
Xe
Cd
Te
Ag
I
Sb
Sn
53
47
52
49
54
48
50
51
7
131,3
126.904
127.60
114 .82
107.868
118.71
112.41
121.75
Иод
Олово
Теллур
Серебро
Ксенон
Сурьма
Индий
Кадмий
Cs
La
Hf
W
Ta
Re
Pt
Os
Ba
Ir
57
73
78
76
72
77
74
75
56
55
8
VI
180.9479
195.09
190.2
137.34
178.49
183.85
132.905
138.81
186.2
192.2
Цезий
Гафний
Иридий
Осмий
Барий
Вольфрам
Лантан
Платина
Тантал
Рений
Pb
Hg
Tl
At
Au
Rn
Po
Bi
85
81
79
84
83
8 6
80
82
9
[22 2 ]
210
200.59
207.2
208.982
208.98
204.383
196.966
Золото
Свинец
Астат
Таллий
Ртуть
Висмут
Полоний
Радон
Rf
Sg
Mt
Db
Hs
Bh
Ac
Fr
Ra
105
106
107
89
104
109
87
88
108
VII
10
[ 226 ]
[ 261 ]
[ 262 ]
[ 223 ]
[ 263 ]
[ 266 ]
[ 262 ]
227.028
[ 265 ]
Мейтнерий
Дубний
Сиборгий
Хассий
Резерфордий
Борий
Радий
Актиний
Франций
![Периодическая система химических элементов Д.И.Менделеева Периоды Ряды Группы элементов VI VII V IV VIII II III I I 1 Фтор/Fluorum (F) Внешний вид простого вещества Бледно-жёлтый газ. Очень ядовит . Электронная коефигуранция [He] 2s 2 2p 5 ЭО (по Полингу) 3,98 Степень окисления − 1 Плотность (при −189 °C)1,108 г/см ³ Температура плавления 53,53К Температура кипения 85,01 К II 2 III 3 4 IV 5 6 V 7 VI 8 9 10 VII](https://fsd.multiurok.ru/html/2025/11/19/s_691dcea4f4124/img8.jpg)
Периодическая система химических элементов Д.И.Менделеева
Периоды
Ряды
Группы элементов
VI
VII
V
IV
VIII
II
III
I
I
1
Фтор/Fluorum (F)
Внешний вид простого вещества
Бледно-жёлтый газ. Очень ядовит .
Электронная коефигуранция
[He] 2s 2 2p 5
ЭО (по Полингу)
3,98
Степень окисления
− 1
Плотность
(при −189 °C)1,108 г/см ³
Температура плавления
53,53К
Температура кипения
85,01 К
II
2
III
3
4
IV
5
6
V
7
VI
8
9
10
VII
![Периодическая система химических элементов Д.И.Менделеева Периоды Ряды Группы элементов VI VII V IV VIII II III I I 1 Хлор / Chlorum (Cl) Внешний вид простого вещества Газ жёлто-зеленого цвета с резким запахом. Ядовит . Электронная коефигуранция [Ne] 3s 2 3p 5 ЭО (по Полингу) 3.16 Степень окисления 7, 6, 5, 4, 3, 1, −1 Плотность (при −33.6 °C)1,56 г/см ³ Температура плавления 172.2 К Температура кипения 238.6 К II 2 III 3 4 IV 5 6 V 7 VI 8 9 10 VII](https://fsd.multiurok.ru/html/2025/11/19/s_691dcea4f4124/img9.jpg)
Периодическая система химических элементов Д.И.Менделеева
Периоды
Ряды
Группы элементов
VI
VII
V
IV
VIII
II
III
I
I
1
Хлор / Chlorum (Cl)
Внешний вид простого вещества
Газ жёлто-зеленого цвета с резким запахом. Ядовит .
Электронная коефигуранция
[Ne] 3s 2 3p 5
ЭО (по Полингу)
3.16
Степень окисления
7, 6, 5, 4, 3, 1, −1
Плотность
(при −33.6 °C)1,56 г/см ³
Температура плавления
172.2 К
Температура кипения
238.6 К
II
2
III
3
4
IV
5
6
V
7
VI
8
9
10
VII
![Периодическая система химических элементов Д.И.Менделеева Периоды Ряды Группы элементов VI VII V IV VIII II III I I 1 Бром / Bromum (Br) Внешний вид простого вещества красно-бурая жидкость с сильным неприятным запахом Электронная конфигуранция [Ar] 3d 10 4s 2 4p 5 ЭО (по Полингу) 2,96 Степень окисления 7, 5, 3, 1, -1 Плотность 3,12 г/см³ Температура плавления 265,9 К Температура кипения 331,9 К II 2 III 3 4 IV 5 6 V 7 VI 8 9 10 VII](https://fsd.multiurok.ru/html/2025/11/19/s_691dcea4f4124/img10.jpg)
Периодическая система химических элементов Д.И.Менделеева
Периоды
Ряды
Группы элементов
VI
VII
V
IV
VIII
II
III
I
I
1
Бром / Bromum (Br)
Внешний вид простого вещества
красно-бурая жидкость с сильным неприятным запахом
Электронная конфигуранция
[Ar] 3d 10 4s 2 4p 5
ЭО (по Полингу)
2,96
Степень окисления
7, 5, 3, 1, -1
Плотность
3,12 г/см³
Температура плавления
265,9 К
Температура кипения
331,9 К
II
2
III
3
4
IV
5
6
V
7
VI
8
9
10
VII
![Периодическая система химических элементов Д.И.Менделеева Периоды Ряды Группы элементов VI VII V IV VIII II III I I 1 Ио́д / Iodum (I) Внешний вид простого вещества Черно-фиолетовые кристаллы с металлическим блеском Электронная конфигуранция [Kr] 4d 10 5s 2 5p 5 ЭО (по Полингу) 2,66 Степень окисления 7, 5, 3, 1, -1 Плотность 4,93г/см³ Температура плавления 386,7 К Температура кипения 457,5 К II 2 III 3 4 IV 5 6 V 7 VI 8 9 10 VII](https://fsd.multiurok.ru/html/2025/11/19/s_691dcea4f4124/img11.jpg)
Периодическая система химических элементов Д.И.Менделеева
Периоды
Ряды
Группы элементов
VI
VII
V
IV
VIII
II
III
I
I
1
Ио́д / Iodum (I)
Внешний вид простого вещества
Черно-фиолетовые кристаллы с металлическим блеском
Электронная конфигуранция
[Kr] 4d 10 5s 2 5p 5
ЭО (по Полингу)
2,66
Степень окисления
7, 5, 3, 1, -1
Плотность
4,93г/см³
Температура плавления
386,7 К
Температура кипения
457,5 К
II
2
III
3
4
IV
5
6
V
7
VI
8
9
10
VII
![Периодическая система химических элементов Д.И.Менделеева Периоды Ряды Группы элементов VI VII V IV VIII II III I I 1 Аста́т / Astatium (At) Внешний вид простого вещества Нестабильные чёрно-синие кристаллы Электронная конфигуранция [Xe] 4f 14 5d 10 6s 2 6p 5 ЭО (по Полингу) 2,2 Степень окисления 7, 5, 3, 1, −1 Плотность n/a г/см Температура плавления 517 К Температура кипения 582 К II 2 III 3 4 IV 5 6 V 7 VI 8 9 10 VII](https://fsd.multiurok.ru/html/2025/11/19/s_691dcea4f4124/img12.jpg)
Периодическая система химических элементов Д.И.Менделеева
Периоды
Ряды
Группы элементов
VI
VII
V
IV
VIII
II
III
I
I
1
Аста́т / Astatium (At)
Внешний вид простого вещества
Нестабильные чёрно-синие кристаллы
Электронная конфигуранция
[Xe] 4f 14 5d 10 6s 2 6p 5
ЭО (по Полингу)
2,2
Степень окисления
7, 5, 3, 1, −1
Плотность
n/a г/см
Температура плавления
517 К
Температура кипения
582 К
II
2
III
3
4
IV
5
6
V
7
VI
8
9
10
VII

Химические свойства 45 F 2 - наиболее реакционноспособен , реакции идут на холоду, при нагревании – даже с участием Au , Pt .
С простыми веществами:
С металлами( в том числе золотом и
платиной.) С неметаллами
2Na + F 2 → 2NaF H 2 + F 2 → 2HF
Mo + 3F 2 → MoF 6 Xe + 2F 2 → XeF 4
Со сложными веществами:
2 H 2 O + F 2 → 4 HF + O 2
2 KCl + F 2 → Cl 2 + 2Na F
2KBr + F 2 → Br 2 + 2К F
2KI + F 2 → I 2 + 2К F

Фтор не может быть растворим в воде, так как энергично разлагает еѐ.
SiO2 +2 F2 = SiF4 + O2 + 157 ккал
2H2 O + 2F2 = 4 HF + O 2+ 143 ккал
Фтор является самым сильным окислителем.
Непосредственно фтор не реагирует только с кислородом, азотом и
углеродом (в виде алмаза).
.

Химические свойства Cl 2 - сильно реакционноспособен (искл. C , O 2 , N 2 и некот. др.)
С простыми веществами:
С металлами С неметаллами
2Fe + 3Cl 2 → 2FeCl 3 H 2 + Cl 2 → 2HCl ( t º, hυ )
Cu + Cl 2 → Cu Cl 2 2P + 5Cl 2 → 2PCl 5 ( t º, в изб. С l 2 )
Со сложными веществами:
H 2 O + Cl 2 → HCl + HClO хлорная вода
2 NaOH + Cl 2 → NaOCl + NaCl + H 2 O жавелевая вода
2KBr + Cl 2 → Br 2 + 2К Cl
2KI + Cl 2 → I 2 + 2К Cl

Хлор непосредственно взаимодействует со всеми
простыми веществами за исключением кислорода, азота и благородных газов.
Такие неметаллы как фосфор, мышьяк, сурьма и кремний при высокой температуре реагируют с хлором с выделением большого количества тепла.
.

Химические свойства Br 2 - реакционноспособен
С простыми веществами:
С металлами С неметаллами
2Al + 3 Br 2 → 2Al Br 3 H 2 + Br 2 → 2HCl
Cu + Br 2 → Cu Br 2 2P + 5Br 2 → 2PBr 5
Со сложными веществами:
Br 2 + H 2 O → HBr + HBrO бромная вода
2KI + Br 2 → I 2 + 2К Cl

Химические свойства I 2 - химически наименее активен
С простыми веществами:
С металлами С неметаллами
Hg + I 2 → HgI 2 H 2 + I 2 → 2HCl ( t º)
2Al + 3I 2 → 2AlI 3 2P + 3Br 2 → 2PI 3
Со сложными веществами:
I 2 + H 2 O → HI + HIO
I 2 + р - р крахмала → темно-синее окрашивание

Йод с водородом реагирует только при достаточно сильном
нагревании , и не полностью, т.к. начинает идти обратная реакция-разложение жидкого водорода:
H2 + J2 2HJ -12, 7 ккал.
.

- все галогены активно взаимодействуют со всеми простыми веществами. Особенно быстро и с выделением большого количества теплоты
- протекает реакция соединения галогенов с металлами.
- Так, расплавленный металлический натрий в атмосфере хлора сгорает
ослепительной вспышкой, а на стѐклах сосуда появляется белый налѐт хлорида натрия:
2N а + C12=2Na C1
Сравнение химических свойств галогенов показывает, что их
относительная активность последовательно уменьшается от фтора к астату.
Этот эффект проявляется в способности более легких галогенов в виде
простых веществ окислять галоген - ионы более тяжелых галогенов:
F2+CI2 2F+CI2
CI2+Br2 2CI+Br2
Br2+2J 2Br+J2
J2+2CIO3 2JO3+CI2
.

Физические свойства галогенов
Фтор – газ светло-желтого цвета, обладающий резким запахом. Ядовит
.

. Хлор – газ светло-зеленого цвета, также как и фтор имеет резкий запах. Сильно ядовит. При повышенном давлении и комнатной температуре легко переходит в жидкое состояние

. Бром – тяжелая жидкость красно-бурого цвета с характерным неприятным резким запахом. Жидкий бром, а также его пары сильно ядовиты. Бром плохо растворяется в воде и хорошо в неполярных растворителях

. Йод – твердое вещество темно-серого цвета с металлическим блеском. Пары йода имеют фиолетовый цвет. Йод легко возгоняется, т.е. переходит в газообразное состояние из твердого, при этом минуя жидкое состояние.
.

- Астат — твёрдое вещество сине-чёрного цвета, по внешнему виду похожее на иод. Для него характерно сочетание свойств неметаллов (галогенов) и металлов (полоний, свинец и другие). Как и иод, астат хорошо растворяется в органических растворителях и легко ими экстрагируется. По летучести немного уступает иоду, но также может легко возгоняться.
.

Получение галогенов
- Галогены можно получить при электролизе растворов или расплавов галогенидов:
- MgCl 2 = Mg + Cl 2 ( расплав).
- Наиболее часто галогены получают по реакции окисления галогенводородных кислот:
- MnO 2 + 4HCl = MnCl 2 + Cl 2 ↑ +2H 2 O;
- K 2 Cr 2 O 7 + 14HCl = 3Cl 2 ↑ + 2KCl +2CrCl 3 +7H 2 O;
- 2KMnO 4 +16HCl = 2MnCl 2 +5Cl 2 ↑ +8H 2 O +2KCl.
.

.

.
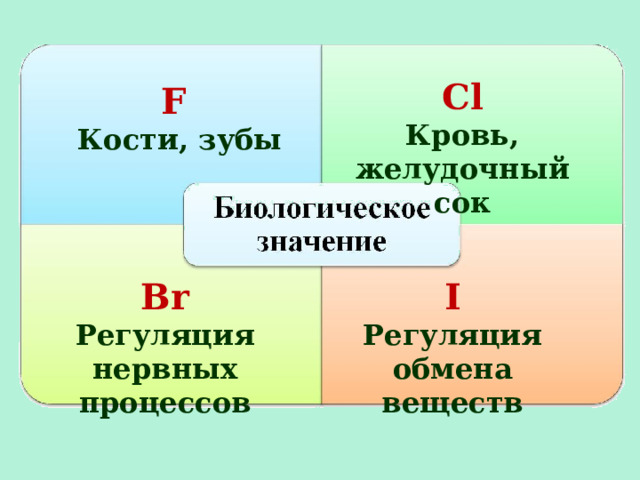
С l
Кровь, желудочный сок
F
Кости, зубы
Br
I
Регуляция нервных процессов
Регуляция обмена веществ
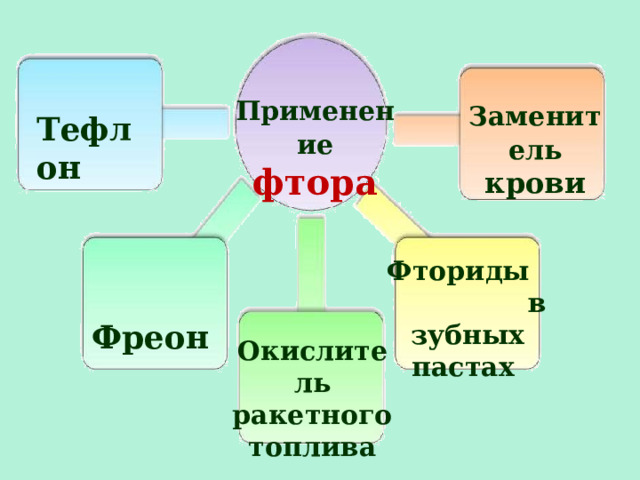
Применение фтора
Заменитель крови
Тефлон
Фториды в зубных пастах
Фреон
Окислитель ракетного топлива

Содержание фтора в организме человека около 10-5% – в костной
ткани, ногтях и зубах . В зубах в виде фторапатита Ca5(PO4)3F содержится
0,01% фтора.
При избытке фтора повышается хрупкость костей (флюороз).
У рабочих электролизных цехов алюминиевых заводов со стажем работы более 10 лет заболеваемость флюорозом превышает 10%
Фтор - сильное ядовитое вещество, вызывает воспаление слизистых
оболочек и сильные, долго незаживающие ожоги кожи.
Соединения фтора приводят к сильным отравлениям. Например, при отравлении фтористым натрием наблюдаются следующие признаки: рвота, иногда кровью, понос, сильное возбуждение, порезы мышц, судороги, паралич дыхательного
центра.
Оказание первой помощи : промывание желудка, солевое слабительное,
известковая вода, и обратится к врачу!
.
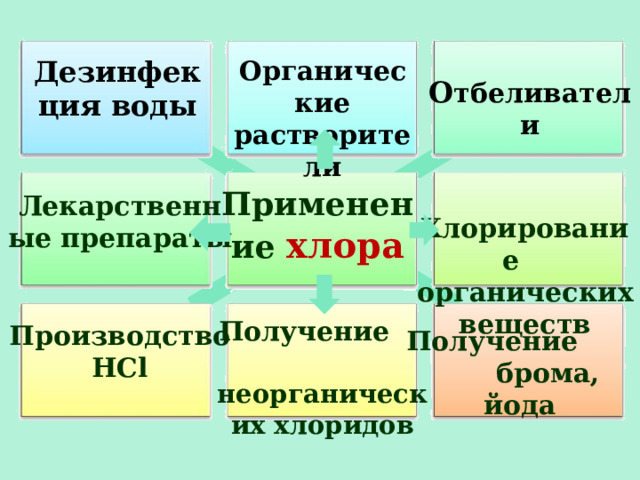
Дезинфекция воды
Органические растворители
О тбеливатели
Хлорирование органических веществ
Применение хлора
Лекарственные препараты
Получение неорганических хлоридов
Производство
HCl
Получение брома, йода

Содержание хлора в организме человека около 0,15%.
Массовая доля соляной кислоты в желудочном соке (рН 1÷3) около 0,3%. Она необходима для перехода фермента пепсина в активную форму.
Хлорид-анион участвует вместе с катионами калия и натрия в солевом обмене между клетками и межклеточными тканями.
Суточная потребность в хлориде натрия – 5-10 г.
Это сильное ядовитое вещество. При вдыхании паров вызывает ожог
слизистых дыхательных путей, кашель, удушье, боли в груди и в глазах,
слезотечение, отѐк легких, ослабление сердца. При приеме внутрь – рвота, боли в желудке, мокрота, спазм голосовой
щели..
Первая помощь : вдыхание кислорода, вдыхать тѐплые водяные пары с
нашатырьным спиртом. Полный покой, постельный режим. При попадании в
глаз – промывание 2% раствором соды и обратится к врачу.
Лекарственные препараты
Ветеренарные препараты
Фотография
Применение брома
Присадки к бензину
Красители
Ингибиторы

Содержание брома в организме человека 10 -5 % – преимущественно в
гипофизе. Бромид-анионы накапливаются в мозге и действуют
успокаивающе. В 1910 г. один из учеников И.П.Павлова, П.М.Никифоровский, установил в опытах на собаках, что бромиды не снижают возбудимость, а усиливают торможение.
Бром - ядовитое вещество. При вдыхании паров брома: насморк, кашель,
удушье, явление бронхита и бронхопневмонии, слезотечение, конъюктивит.
Слизистая рта и языка имеет коричневый цвет. При внутреннем приеме: боли
в животе, рвота и понос.
Первая помощь : вдыхать водяные пары с небольшой примесью нашатырного спирта, ингаляции с содовым раствором. При
отравлении через рот – промывание желудка 0,5% раствором тиосульфата
натрия.
19.11.25
Сафиканов А.Ф.
Лекарственные препараты
Дезинфекция одежды
Применение йода
Красители
Фотография
Электролампы

Йод - ядовитое вещество. Симптомы острого отравления : бурое окрашивание языка и слизистой оболочки рта, рвота бурыми и синими
массами, понос, головная боль, насморк, кожная сыпь. В тяжелых случаях - судороги, коматозное состояние.
Помощь при отравлениях : промывание
желудка 0,5% раствором тиосульфата натрия, внутрь 20-30г активированного угля в водной взвеси. Промывать, прополоскать, нос, рот, глотку 2% раствором двууглекислого натрия.
Больше половины содержащегося в человеке иода (всего 4*10-5%) находится в щитовидной железе – в составе гормонов тироксина и
трииодтиронина. В небольших дозах регулирует работу щитовидной железы. При
недостатке йода возникает базедова болезнь.
Йод применяют для йодной настойки(5% раствора йода в спирте,) йодид калия используют в медицине, аналитической химии, а йодид серебра – при изготовлении фотоматериалов.













![Периодическая система химических элементов Д.И.Менделеева Периоды Ряды Группы элементов VI VII V IV VIII II III I I 1 Фтор/Fluorum (F) Внешний вид простого вещества Бледно-жёлтый газ. Очень ядовит . Электронная коефигуранция [He] 2s 2 2p 5 ЭО (по Полингу) 3,98 Степень окисления − 1 Плотность (при −189 °C)1,108 г/см ³ Температура плавления 53,53К Температура кипения 85,01 К II 2 III 3 4 IV 5 6 V 7 VI 8 9 10 VII](https://fsd.multiurok.ru/html/2025/11/19/s_691dcea4f4124/img8.jpg)
![Периодическая система химических элементов Д.И.Менделеева Периоды Ряды Группы элементов VI VII V IV VIII II III I I 1 Хлор / Chlorum (Cl) Внешний вид простого вещества Газ жёлто-зеленого цвета с резким запахом. Ядовит . Электронная коефигуранция [Ne] 3s 2 3p 5 ЭО (по Полингу) 3.16 Степень окисления 7, 6, 5, 4, 3, 1, −1 Плотность (при −33.6 °C)1,56 г/см ³ Температура плавления 172.2 К Температура кипения 238.6 К II 2 III 3 4 IV 5 6 V 7 VI 8 9 10 VII](https://fsd.multiurok.ru/html/2025/11/19/s_691dcea4f4124/img9.jpg)
![Периодическая система химических элементов Д.И.Менделеева Периоды Ряды Группы элементов VI VII V IV VIII II III I I 1 Бром / Bromum (Br) Внешний вид простого вещества красно-бурая жидкость с сильным неприятным запахом Электронная конфигуранция [Ar] 3d 10 4s 2 4p 5 ЭО (по Полингу) 2,96 Степень окисления 7, 5, 3, 1, -1 Плотность 3,12 г/см³ Температура плавления 265,9 К Температура кипения 331,9 К II 2 III 3 4 IV 5 6 V 7 VI 8 9 10 VII](https://fsd.multiurok.ru/html/2025/11/19/s_691dcea4f4124/img10.jpg)
![Периодическая система химических элементов Д.И.Менделеева Периоды Ряды Группы элементов VI VII V IV VIII II III I I 1 Ио́д / Iodum (I) Внешний вид простого вещества Черно-фиолетовые кристаллы с металлическим блеском Электронная конфигуранция [Kr] 4d 10 5s 2 5p 5 ЭО (по Полингу) 2,66 Степень окисления 7, 5, 3, 1, -1 Плотность 4,93г/см³ Температура плавления 386,7 К Температура кипения 457,5 К II 2 III 3 4 IV 5 6 V 7 VI 8 9 10 VII](https://fsd.multiurok.ru/html/2025/11/19/s_691dcea4f4124/img11.jpg)
![Периодическая система химических элементов Д.И.Менделеева Периоды Ряды Группы элементов VI VII V IV VIII II III I I 1 Аста́т / Astatium (At) Внешний вид простого вещества Нестабильные чёрно-синие кристаллы Электронная конфигуранция [Xe] 4f 14 5d 10 6s 2 6p 5 ЭО (по Полингу) 2,2 Степень окисления 7, 5, 3, 1, −1 Плотность n/a г/см Температура плавления 517 К Температура кипения 582 К II 2 III 3 4 IV 5 6 V 7 VI 8 9 10 VII](https://fsd.multiurok.ru/html/2025/11/19/s_691dcea4f4124/img12.jpg)




































