
Электролитическая диссоциация
Электролиты и неэлектролиты

Проводят ли электрический ток вода, соль и раствор соли?
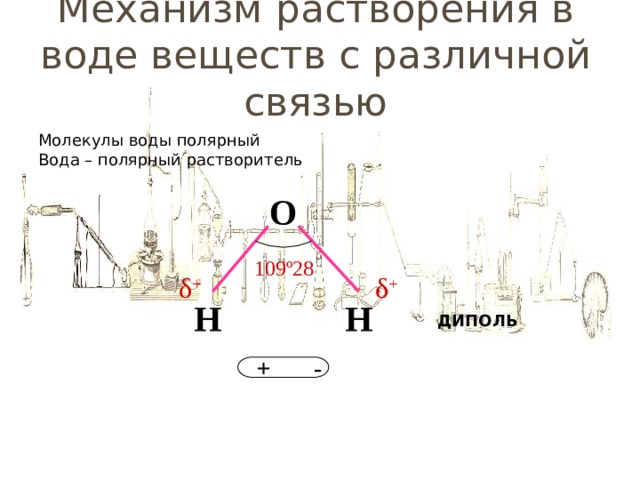
Механизм растворения в воде веществ с различной связью
Молекулы воды полярный
Вода – полярный растворитель
О
109 º28
δ +
δ +
Н
Н
ДИПОЛЬ
+ -
+ -
+ -
+ -
- +
- +
+ -
+ -
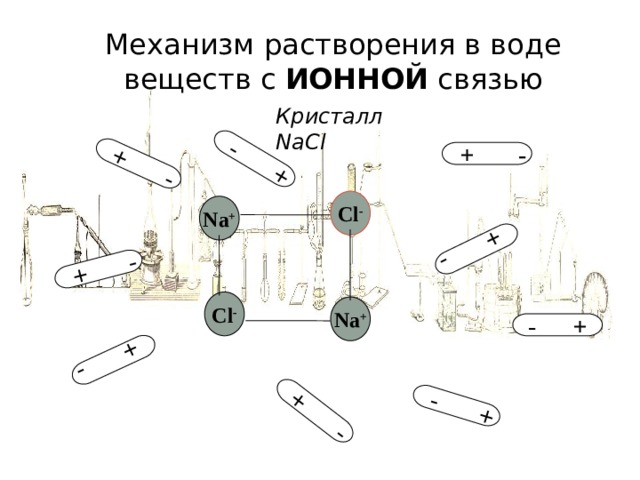
Механизм растворения в воде веществ с ИОННОЙ связью
Кристалл NaCl
+ -
Cl -
Na +
Cl -
Na +
- +
+ -
+ -
+ -
- +
- +
+ -
+ -
+ -
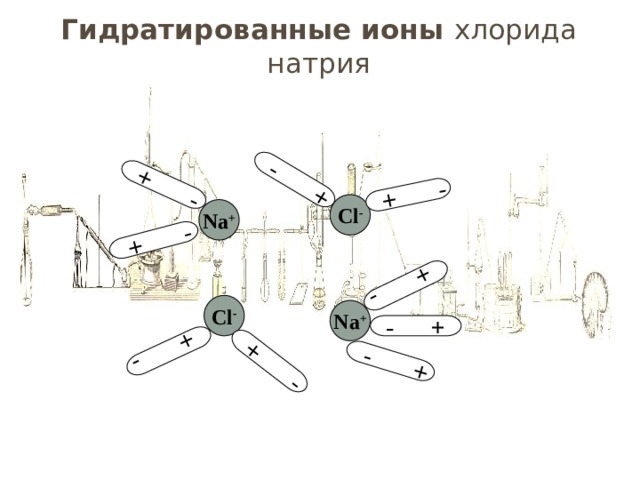
Гидратированные ионы хлорида натрия
Cl -
Na +
Cl -
Na +
- +


Механизм растворения в воде веществ с ИОННОЙ связью
Процессу гидратации способствует большая диэлектрическая проницаемость воды.
При 20 о она равна 81.
Это значить, что химическая связь между ионами в воде в 81 раз слабее, чем в вакууме.

+ -
+ -
+ -
+ -
+ -
+ -
Механизм растворения в воде веществ с КОВАЛЕНТНОЙ ПОЛЯРНОЙ связью
HCl

+ -
+ -
+ -
+ -
+ -
Механизм растворения в воде веществ с КОВАЛЕНТНОЙ ПОЛЯРНОЙ связью
+ -
+ -
Под действием полярного растворителя ковалентная полярная связь поляризуется еще больше (Ионизируется), вследствие чего становится ионной.
+ -
+ -
+ -
+ -
+ -
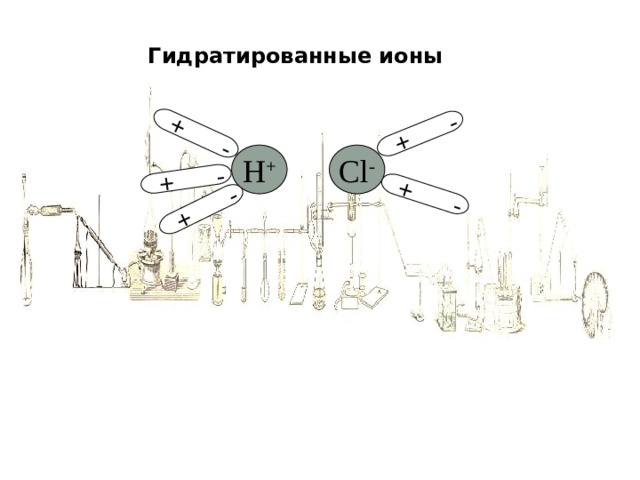
Гидратированные ионы
H +
Cl -

Соли и щелочи проводят ток не только в растворах, но и в расплавах .
А сахар, ацетон и спирт ток не проводят.
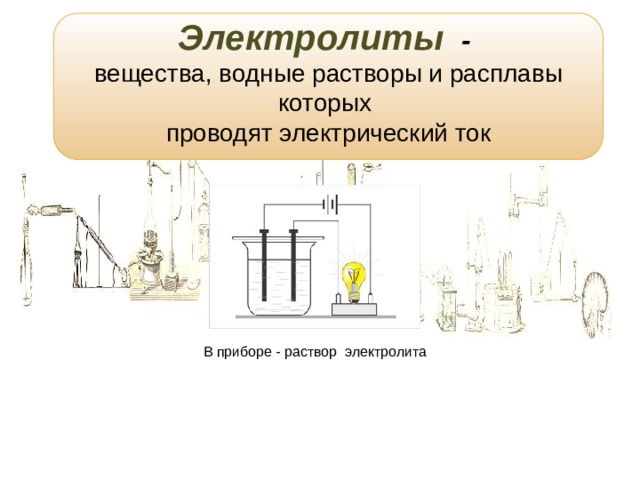
Электролиты -
вещества, водные растворы и расплавы которых
проводят электрический ток
В приборе - раствор электролита
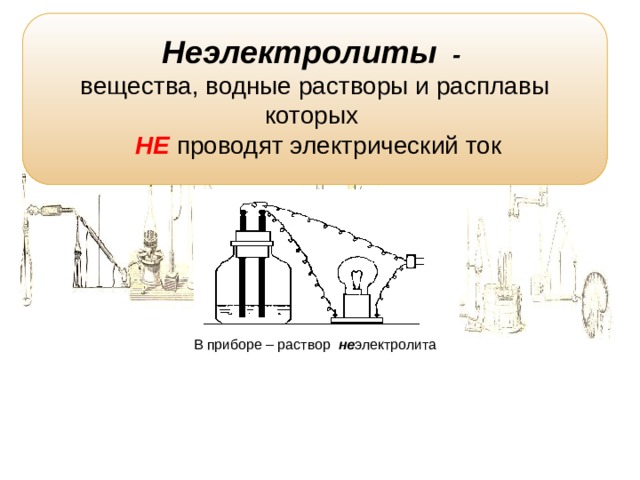
Неэлектролиты -
вещества, водные растворы и расплавы которых
НЕ проводят электрический ток
В приборе – раствор не электролита
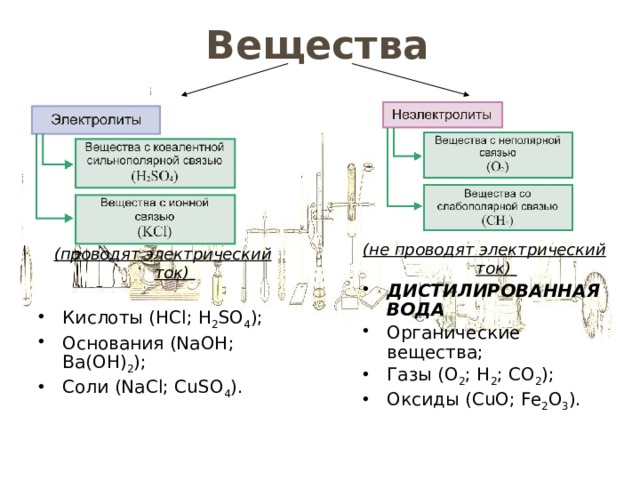
Вещества
(не проводят электрический ток)
- ДИСТИЛИРОВАННАЯ ВОДА
- Органические вещества;
- Газы (O 2 ; H 2 ; CO 2 );
- Оксиды (CuO; Fe 2 O 3 ).
(проводят электрический ток)
- Кислоты (HCl; H 2 SO 4 );
- Основания (NaOH; Ba(OH) 2 );
- Соли (NaCl; CuSO 4 ).

Электролитическая диссоциация - процесс распада электролита на ионы при растворении в воде или расплавлении.
Сванте Август
Аррениус
1859-1927гг.
Шведский физико-химик,
создатель теории
электролитической
диссоциации.

Теория электролитической диссоциации
1. Электролиты при растворении в воде или расплавлении распадаются ( диссоциируют ) на положительно заряженные ионы (катионы) и отрицательно заряженные (анионы) .
В водных растворах ионы химически связаны с молекулами воды - гидратированы

Теория электролитической диссоциации
1. Электролиты при растворении в воде или расплавлении распадаются ( диссоциируют ) на положительно заряженные ионы (катионы) и отрицательно заряженные (анионы) .
В водных растворах ионы химически связаны с молекулами воды - гидратированы
Уравнение диссоциации записывают упрощенно
KCl → K + + Cl -

Теория электролитической диссоциации
1. Электролиты при растворении в воде или расплавлении распадаются ( диссоциируют ) на положительно заряженные ионы (катионы) и отрицательно заряженные (анионы) .
В водных растворах ионы химически связаны с молекулами воды - гидратированы
Уравнение диссоциации записывают упрощенно
KCl → K + + Cl -
CuSO 4 → Cu 2+ + SO 4 2-

Теория электролитической диссоциации
1. Электролиты при растворении в воде или расплавлении распадаются ( диссоциируют ) на положительно заряженные ионы (катионы) и отрицательно заряженные (анионы) .
В водных растворах ионы химически связаны с молекулами воды - гидратированы
Уравнение диссоциации записывают упрощенно
KCl → K + + Cl -
CuSO 4 → Cu 2+ + SO 4 2-
Na 2 SO 4 → 2Na + + SO 4 2-

Теория электролитической диссоциации
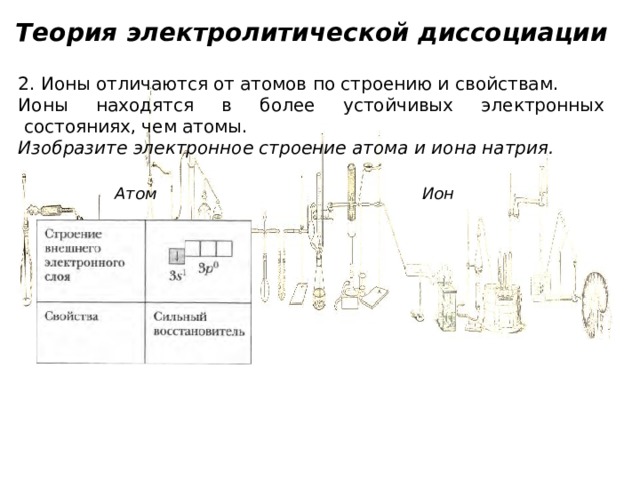
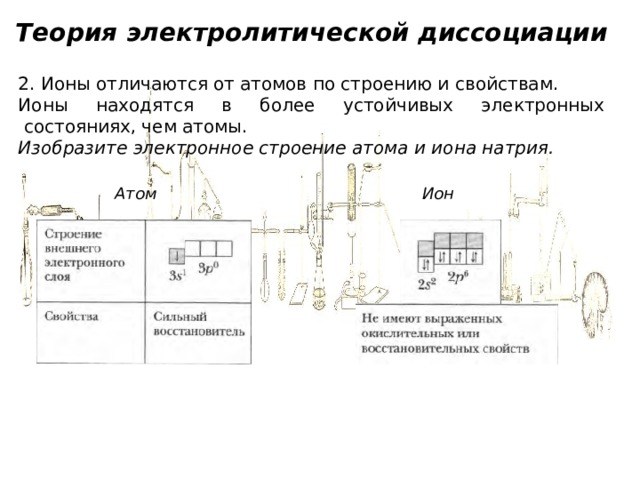
2. Ионы отличаются от атомов по строению и свойствам.
Ионы находятся в более устойчивых электронных состояниях, чем атомы.
Изобразите электронное строение атома и иона натрия.
Атом
Ион
Теория электролитической диссоциации
2. Ионы отличаются от атомов по строению и свойствам.
Ионы находятся в более устойчивых электронных состояниях, чем атомы.
Изобразите электронное строение атома и иона натрия.
Атом
Ион
Теория электролитической диссоциации
2. Ионы отличаются от атомов по строению и свойствам.
Ионы находятся в более устойчивых электронных состояниях, чем атомы.
Изобразите электронное строение атома и иона натрия.
Атом
Ион
Теория электролитической диссоциации
3. В растворах и расплавах электролиты проводят электрический ток . При пропускании тока ионы движутся упорядоченно
катионы к катоду (-) анионы к аноду (+)

Растворение – физико-химический процесс
При растворение в воде серной кислоты выделяется большое количество тепла.
При растворении аммиачной селитры (нитрата аммония) NH 4 NO 3 – поглощается тепло.
Тепловые явления являются признаком химической реакции.

Гидратированные ионы могут отличаться по окраске от негидратированных
- Гидратированные ионы меди придают раствору голубой цвет
- При выпаривании образуются голубые кристаллы медного купороса CuSO 4 *5H 2 O

Домашнее задание
§ 6 – учить!


















































