
Углеводороды. Предельные (насыщенные) углеводороды. Непредельные (ненасыщенные) углеводороды
9 класс
(АДАПТИВНАЯ ПРОГРАММА)
Углеводороды
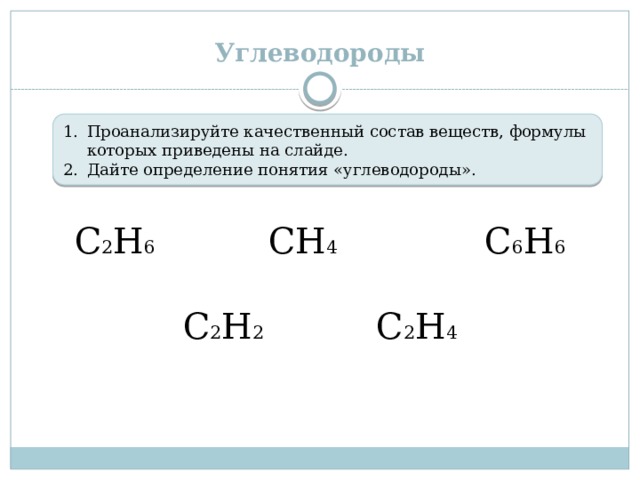
- Проанализируйте качественный состав веществ, формулы которых приведены на слайде.
- Дайте определение понятия «углеводороды».
С 2 Н 6 СН 4 С 6 Н 6
С 2 Н 2 С 2 Н 4
Углеводороды
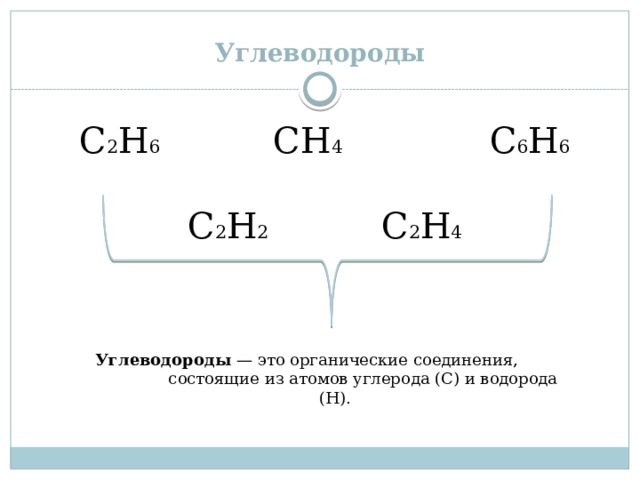
С 2 Н 6 СН 4 С 6 Н 6
С 2 Н 2 С 2 Н 4
Углеводороды — это органические соединения, состоящие из атомов углерода (С) и водорода (Н).
Классификация углеводородов
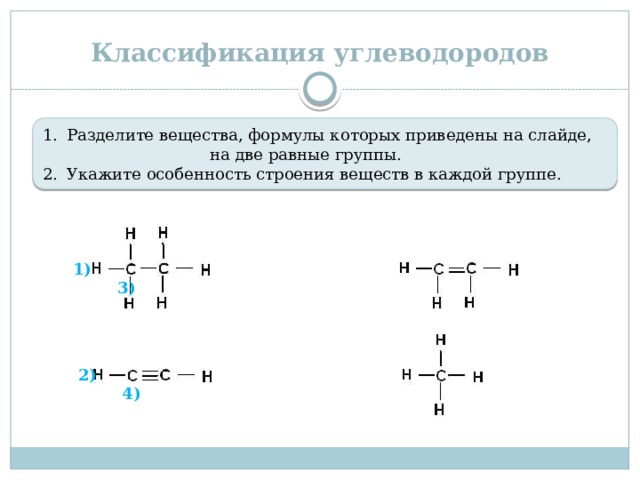
- Разделите вещества, формулы которых приведены на слайде, на две равные группы.
- Укажите особенность строения веществ в каждой группе.
1) 3)
2) 4)
Классификация углеводородов
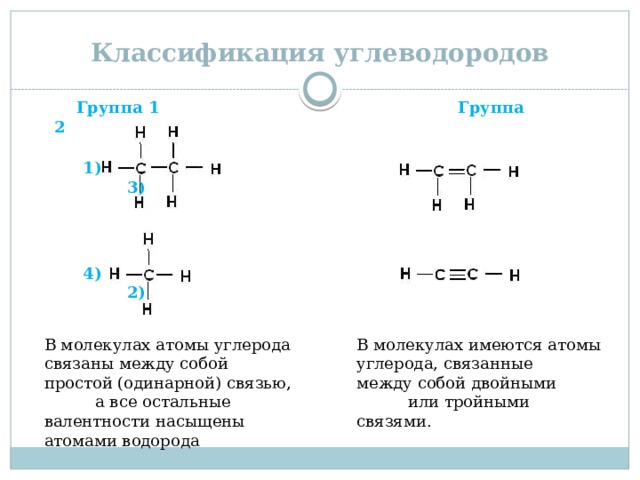
Группа 1 Группа 2
1) 3)
4) 2)
В молекулах атомы углерода связаны между собой
В молекулах имеются атомы углерода, связанные
простой (одинарной) связью, а все остальные валентности насыщены атомами водорода
между собой двойными или тройными связями.
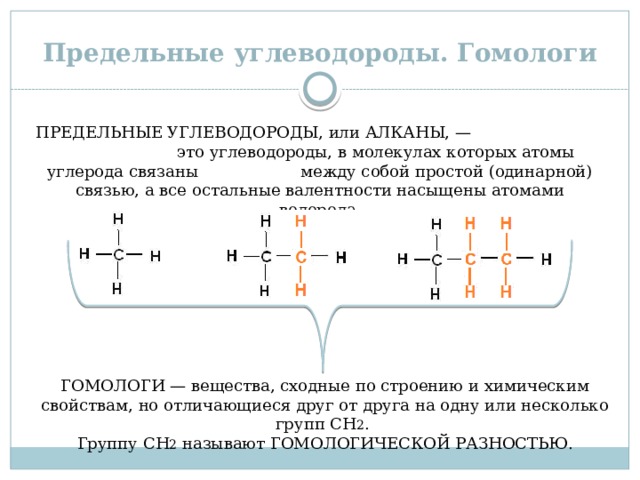
Предельные углеводороды. Гомологи
ПРЕДЕЛЬНЫЕ УГЛЕВОДОРОДЫ, или АЛКАНЫ, — это углеводороды, в молекулах которых атомы углерода связаны между собой простой (одинарной) связью, а все остальные валентности насыщены атомами водорода.
ГОМОЛОГИ — вещества, сходные по строению и химическим свойствам, но отличающиеся друг от друга на одну или несколько групп СН 2 .
Группу СН 2 называют ГОМОЛОГИЧЕСКОЙ РАЗНОСТЬЮ.

Предельные углеводороды
БЕНЗИН
НЕФТЬ
ПРИРОДНЫЙ ГАЗ
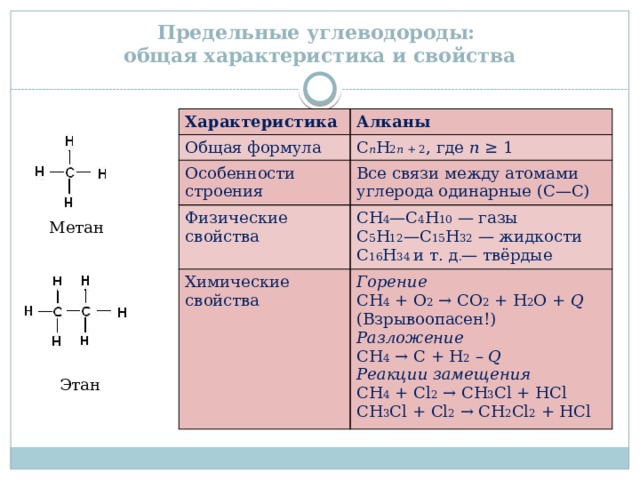
Предельные углеводороды: общая характеристика и свойства
Характеристика
Алканы
Общая формула
C n H 2 n + 2 , где n ≥ 1
Особенности строения
Физические свойства
Все связи между атомами углерода одинарные (С—С)
СН 4 —С 4 Н 10 — газы
Химические свойства
С 5 Н 12 —С 15 Н 32 — жидкости
Горение
С 16 Н 34 и т. д . — твёрдые
СН 4 + О 2 → СО 2 + Н 2 О + Q
(Взрывоопасен!)
Разложение
СН 4 → С + Н 2 – Q
Реакции замещения
СН 4 + Cl 2 → CH 3 Cl + НCl
CH 3 Cl + Cl 2 → CH 2 Cl 2 + НCl
Метан
Этан
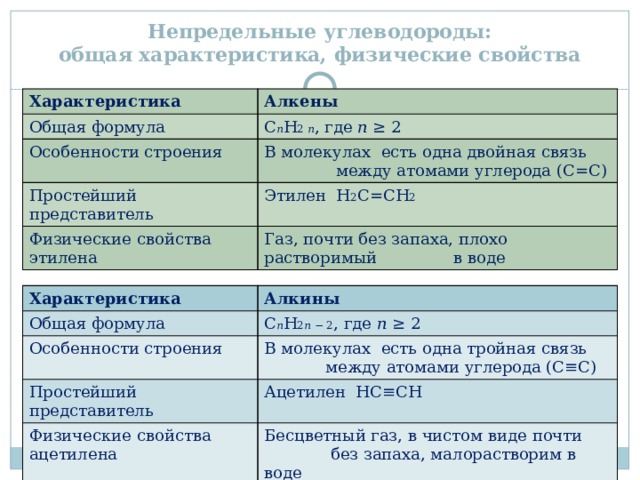
Непредельные углеводороды: общая характеристика, физические свойства
Характеристика
Алкены
Общая формула
C n H 2 n , где n ≥ 2
Особенности строения
В молекулах есть одна двойная связь между атомами углерода (С=С)
Простейший представитель
Этилен H 2 С=СH 2
Физические свойства этилена
Газ, почти без запаха, плохо растворимый в воде
Характеристика
Общая формула
Алкины
Особенности строения
C n H 2 n − 2 , где n ≥ 2
В молекулах есть одна тройная связь между атомами углерода (С≡С)
Простейший представитель
Физические свойства ацетилена
Ацетилен НС≡СН
Бесцветный газ, в чистом виде почти без запаха, малорастворим в воде
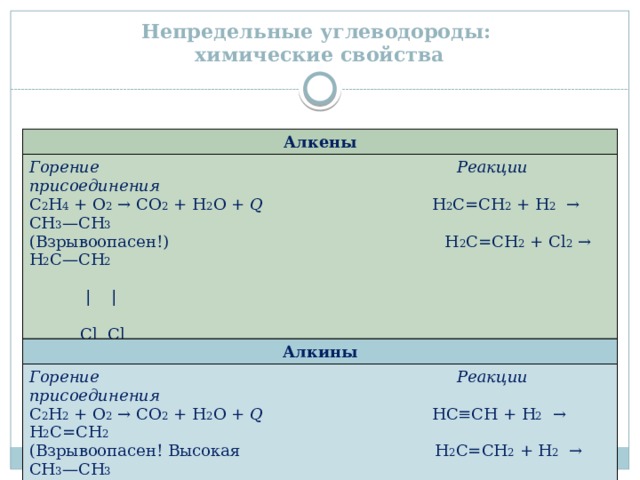
Непредельные углеводороды: химические свойства
Алкены
Горение Реакции присоединения
С 2 Н 4 + О 2 → СО 2 + Н 2 О + Q H 2 С=СH 2 + Н 2 → СН 3 —СН 3
(Взрывоопасен!) H 2 С=СH 2 + Cl 2 → H 2 С—СH 2
| |
Cl Cl
Реакция полимеризации
n H 2 С=СH 2 → (—H 2 С—СH 2 —) n
полиэтилен
Алкины
Горение Реакции присоединения
С 2 Н 2 + О 2 → СО 2 + Н 2 О + Q HС≡СH + Н 2 → H 2 С=СH 2
(Взрывоопасен! Высокая H 2 С=СH 2 + Н 2 → СН 3 —СН 3
температура пламени,
используется для резки и сварки металлов)



























