
Аморфные и кристаллические вещества. Кристаллические решетки

Агрегатное состояние вещества (на примере кислорода О 2 )
Т пл
Т кип
жидкое
твердое
газ
- 218,8°
- 194°
t°, C
0°
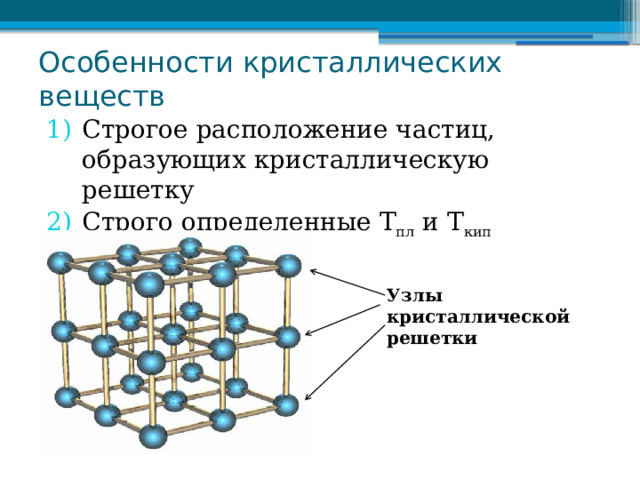
Особенности кристаллических веществ
- Строгое расположение частиц, образующих кристаллическую решетку
- Строго определенные Т пл и Т кип
Узлы кристаллической
решетки
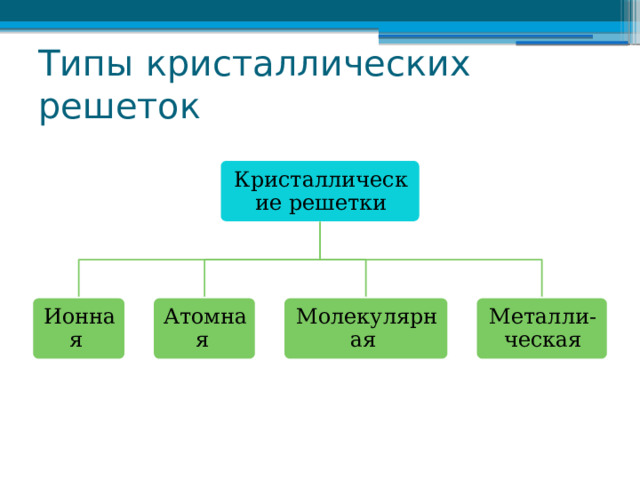
Типы кристаллических решеток
Кристаллические решетки
Ионная
Атомная
Молекулярная
Металли-ческая
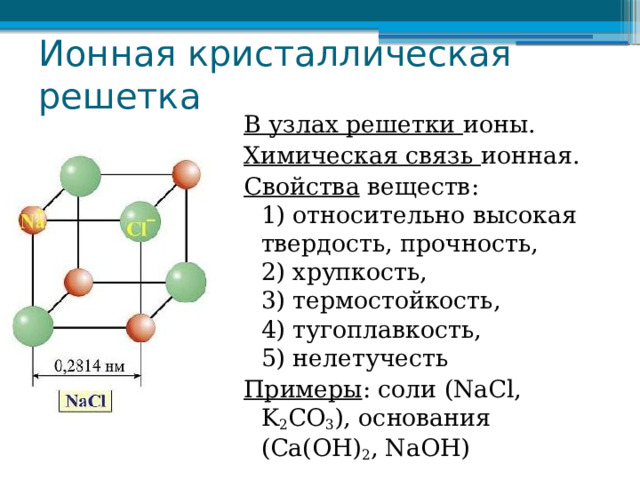
Ионная кристаллическая решетка
В узлах решетки ионы.
Химическая связь ионная.
Свойства веществ: 1) относительно высокая твердость, прочность, 2) хрупкость, 3) термостойкость, 4) тугоплавкость, 5) нелетучесть
Примеры : соли (NaCl, K 2 CO 3 ), основания (Ca(OH) 2 , NaOH)
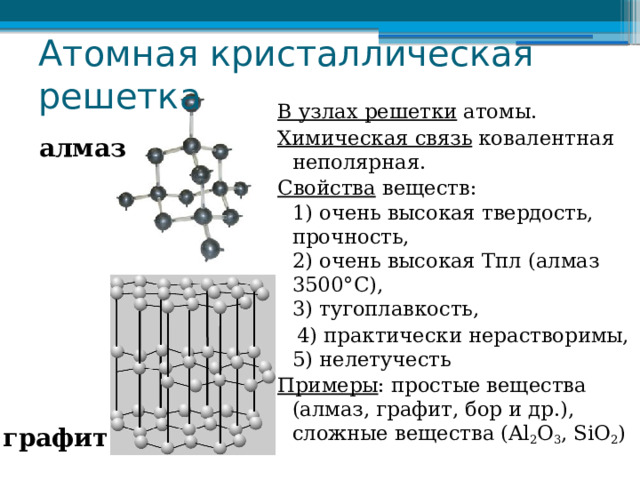
Атомная кристаллическая решетка
В узлах решетки атомы.
Химическая связь ковалентная неполярная.
Свойства веществ: 1) очень высокая твердость, прочность, 2) очень высокая Тпл (алмаз 3500 ° С), 3) тугоплавкость,
4) практически нерастворимы, 5) нелетучесть
Примеры : простые вещества (алмаз, графит, бор и др.), сложные вещества (Al 2 O 3 , SiO 2 )
алмаз
графит

Молекулярная кристаллическая решетка
В узлах решетки молекулы.
Химическая связь ковалентная полярная и неполярная.
Свойства веществ: 1) малая твердость, прочность, 2) низкие Тпл, Ткип, 3) при комнатной Т обычно жидкость или газ, 4) высокая летучесть.
Примеры : простые вещества (H 2 , N 2 , O 2 , F 2 , P 4 , S 8 , Ne, He), сложные вещества (СО 2 , H 2 O, сахар С 12 H 22 O 11 и др.)
йод I 2
углекислый газ СО 2
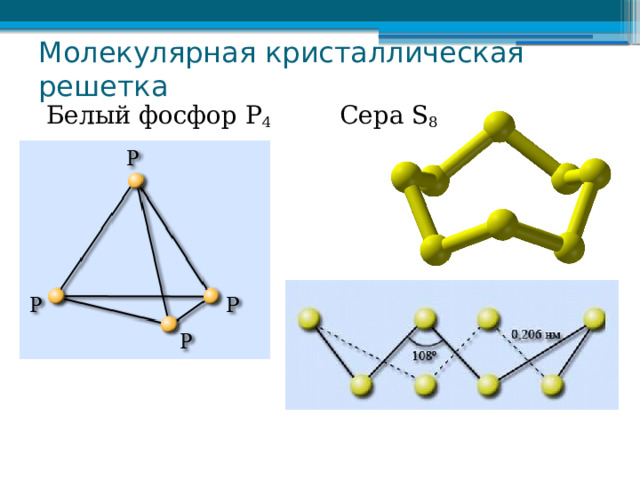
Молекулярная кристаллическая решетка
Белый фосфор Р 4
Сера S 8
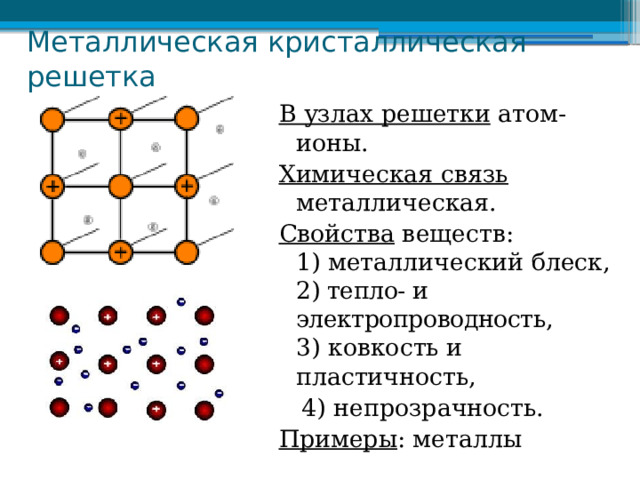
Металлическая кристаллическая решетка
В узлах решетки атом-ионы.
Химическая связь металлическая.
Свойства веществ: 1) металлический блеск, 2 ) тепло- и электропроводность, 3) ковкость и пластичность,
4) непрозрачность.
Примеры : металлы

Закон постоянства состава (Пруст, 1799-1803)
Молекулярные химические соединения независимо от способа их получения имеют постоянный состав и свойства.
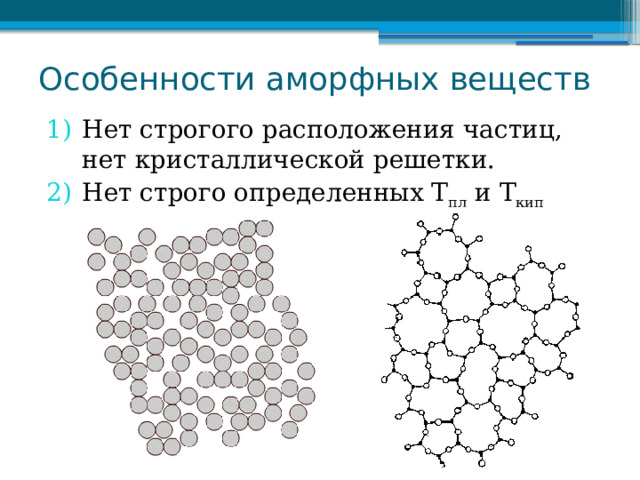
Особенности аморфных веществ
- Нет строгого расположения частиц, нет кристаллической решетки.
- Нет строго определенных Т пл и Т кип

Аморфные вещества

Аморфные вещества

Аморфные вещества

Аморфные вещества

Аморфные вещества

Аморфные вещества

Аморфные вещества

Задание. Определите тип кристаллической решетки в веществах
KNO 3
NO 2
CH 4
Si
Fe
NaF
As

Домашнее задание:













































