Просмотр содержимого документа
«Презентация на тему: "Растворы"»

Растворы – это интересно
Заседание кружка
«Химия для любознательных»
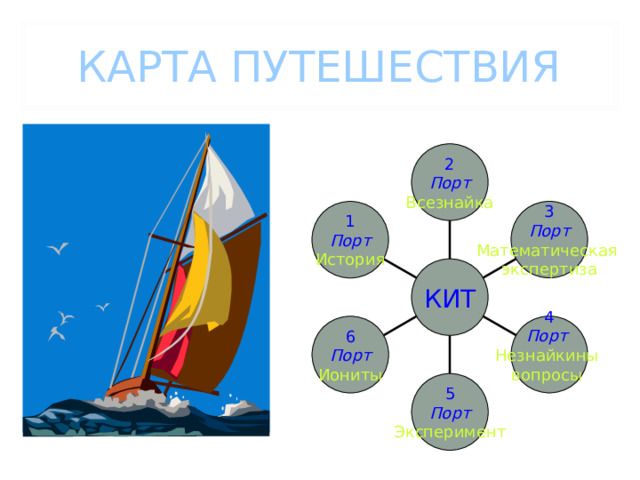
КАРТА ПУТЕШЕСТВИЯ
2
Порт
Всезнайка
3
Порт
Математическая
экспертиза
1
Порт
История
КИТ
4
Порт
Незнайкины
вопросы
6
Порт
Иониты
5
Порт
Эксперимент


1859-1927 гг
- Теория Электролитической диссоциации (1887 г.)
- Лауреат Нобелевской премии (1903 г.)

1834-1907г.г.
- Периодический закон и ПСХЭ
- Сольватная теория растворов

1853 - 1932 г.г.
- "закон разбавления", названный его именем
- основал первую в мире кафедру физической химии в Лейпцигском университете
- Лауреат Нобелевской премии по химии (1909 год)

1857-1942 г.г.
- Гидратная теория растворов (1891 г)
CuSO 4 x 5H 2 O


Задание №1
- Выполняя практическую работу, ученик прилил к раствору карбоната калия раствор хлорида кальция, затем последовательно добавлял в эту пробирку соляную кислоту, растворы нитрата серебра, сульфата железа ( III ) и гидроксида натрия. Потом он попытался понять, что же у него в пробирке?
- Какие вещества оказались в пробирке?
- Напишите уравнения реакций.

Задание № 2
- В конце Х I Х века молодые ученые И.А.Каблуков и, независимо от него, В.А Кистяковский пришли к выводу, что ионы при движении увлекают с собой некоторое количество воды, и чем меньше радиус иона, тем большее количество воды он может удержать вокруг себя, следовательно его размеры увеличиваются.
- Как называется явление, которое
описали Каблуков и Кистяковский?


а) в воду;
б) в гидроксид натрия;
в) в азот;

а) выдвинул идею о гидратации ионов в растворе
б) сформулировал основные положения теории электролитической диссоциации
в)экспериментально определил размер некоторых ионов в растворе.

а) процесс растворения вещества в воде
б) реакция обмена, в которой участвует вода
в) взаимодействие атомов или ионов с молекулами воды.

а) сформулировал основные положения теории электролитической диссоциации
б) открыл химическую сущность процесса растворения
в) выдвинул идею о гидратации ионов в растворе
г) объединил теорию растворов с представлениями об электролитической диссоциации.

а) в состав которых входит химически связанная вода
б) растворимые в воде
в) реагирующие с водой

а) анионы движутся в растворе хаотично
б) анионы заряжены отрицательно
в) анионы не имеют заряда

а) Н + и SO 4 2- б) Ва 2+ и SO 4 2- в) Н + и NO 3 - г) Na + + и SO 4 2-

а) 25% всех молекул кислоты не диссоцирует на ионы
б) 25% всех частиц в растворе – молекулы
в) 25% всех молекул диссоциирует на ионы

а) СаС l 2 б ) HCl в ) Al 2 (SO 4 ) 3 г ) H 2 SO 4

а ) HNO 3 = H + + 3NO - б ) HNO 3 = H - + NO 3 + в ) HNO 3 = H + + NO 3 - г ) HNO 3 = H + + NO 3-

а) BaCl 2 б) AgNO 3 в) H 2 S г) HNO 3

а) Fe ( OH ) 3 и HCl
б) FeCl 3 и AgNO 3
в ) K 2 CO 3 и HCl
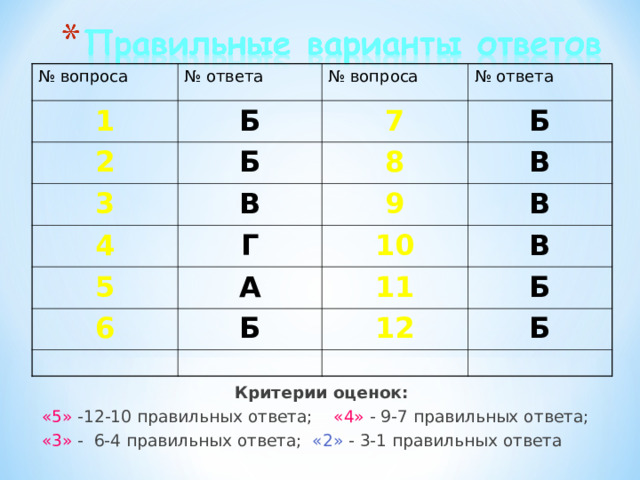
№ вопроса
№ ответа
1
№ вопроса
Б
2
3
№ ответа
7
Б
В
Б
4
8
5
Г
9
В
В
10
А
6
В
11
Б
Б
12
Б
Критерии оценок:
«5» -12-10 правильных ответа; «4» - 9-7 правильных ответа;
«3» - 6-4 правильных ответа; «2» - 3-1 правильных ответа



- Задание №1 .
- Даны реактивы: растворы сульфата меди ( II ), гидроксида натрия, хлорида бария, серной кислоты, хлорида железа ( III ). Используя выданные вам вещества, получите:
- а) три осадка – голубой, белый и бурый;
- Напишите уравнения реакций в молекулярной и ионной форме.
- Задание №2.
- Даны реактивы: соляная кислота, растворы сульфата меди ( II ), гидроксида натрия, нитрат серебра, фенолфталеина. Используя выданные вам вещества, получите:
- а) бесцветный раствор – раствор малинового цвета – бесцветный раствор – осадок белого цвета;
- Напишите уравнения реакций в молекулярной и ионной форме.


- Ионный обмен
- Деминерализация воды
- Серебро из сточных вод
















































