Просмотр содержимого документа
«Презентация на тему " Свойства оснований"»

Физические и химические свойства оснований

Цель урока:
- Рассмотреть физические и химические свойства оснований

НАЗОВИТЕ ОСНОВАНИЯ:
- Cu(OH)2
- Fe(OH)3
- Ca(OH) 2
- NaOH
- Zn(OH) 2

СОСТАВЬТЕ ФОРМУЛЫ ОСНОВАНИЙ:
лития
бария
железа (II)
меди(I)
алюминия
КАКИЕ ИЗ НИХ ОТНОСЯТСЯ К ЩЕЛОЧАМ?
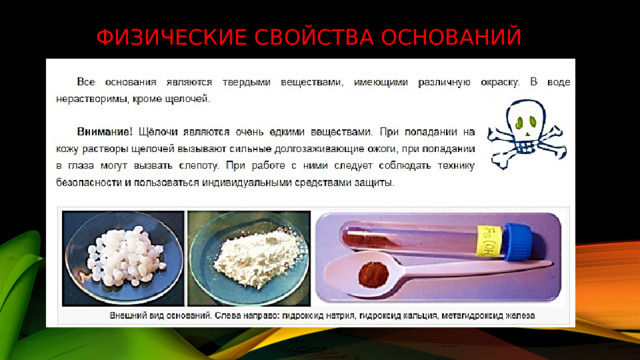
Физические свойства оснований

Соблюдайте правила ТБ при обращении с основаниями
В случае попадания щелочи на одежду или участок кожи следует немедленно сообщить учителю о случившемся и сделать следующее: тщательно и обильно промыть участок кожи водой из-под крана, затем обработать это место нейтрализующим раствором борной кислоты, вновь промыть водой и смазать место ожога вазелиновым маслом. Обязательно обратиться в медпункт школы для наблюдения и оказания дальнейшей медицинской помощи.
Химические свойства оснований
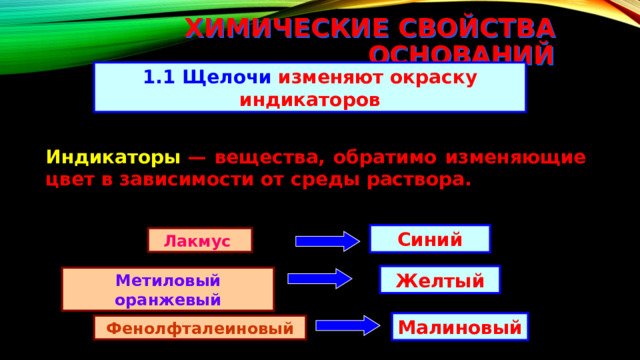
1.1 Щелочи изменяют окраску индикаторов
Индикаторы — вещества, обратимо изменяющие цвет в зависимости от среды раствора.
Синий
Лакмус
Желтый
Метиловый оранжевый
Малиновый
Фенолфталеиновый

1.2 Взаимодействие щелочей с кислотными оксидами
NB!Для написания реакции необходимо знать, какая кислота соответствует кислотному оксиду.

Щелочи реагируют с кислотными оксидами
Соответствующая кислота
Кислотный остаток в соли
Кислотный оксид
SO 2
Me SO 3 (II) сульфит
H 2 SO 3
Me SO 4 (II) сульфат
SO 3
H 2 SO 4
P 2 O 5
Me PO 4 (III) фосфат
H 3 PO 4
N 2 O 5
Me NO 3 (I) нитрат
H NO 3
Me CO 3 (II) карбонат
CO 2
H 2 CO 3
Me SiO 3 (II) силикат
SiO 2
H 2 SiO 3

1.2 Взаимодействие щелочей с кислотными оксидами
Кислотный оксид
+
+
Щелочь
Вода
Соль
реакция нейтрализации
Me a OH +НеМеО→ Me a R +H 2 O
Me активный – Ме I-II групп,главных подгрупп
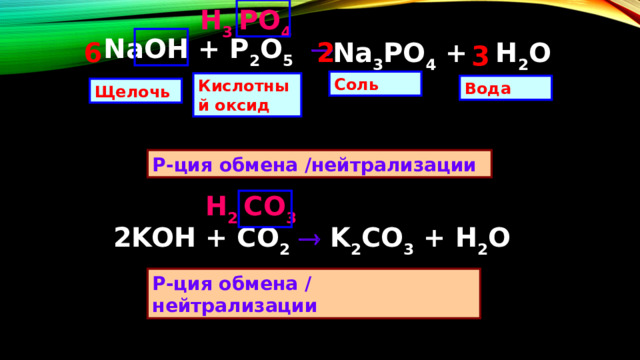
Н 3 PO 4
2
6
Na 3 PO 4 + H 2 O
3
NaOH + P 2 O 5
Соль
Кислотный оксид
Вода
Щелочь
Р-ция обмена /нейтрализации
Н 2 CO 3
2KOH + CO 2 K 2 CO 3 + H 2 O
Р-ция обмена / нейтрализации
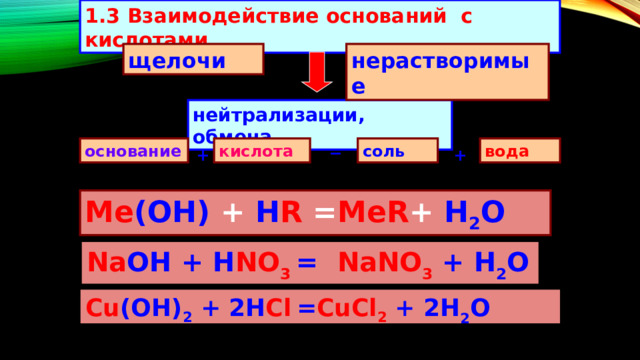
1.3 Взаимодействие оснований с кислотами
щелочи
нерастворимые
нейтрализации, обмена
=
вода
кислота
соль
основание
+
+
Me (OH) + H R = MeR + H 2 O
Na OH + H NO 3 … + …
Na OH + H NO 3 = NaNO 3 + H 2 O
Cu (OH) 2 + H Cl … + …
Cu (OH) 2 + 2H Cl = CuCl 2 + 2H 2 O

1.4 Взаимодействие щелочей с солями
нераств.
основание
+
=
+
Щелочь
Соль 2
соль 1
Me › а (OH) + Me ‹a R = MeR ↓ + H 2 O
Na OH + Сu( NO 3 ) 2 NaNO 3 + Cu(OH) 2 ↓
р
р
н
3K OH + Al Cl 3 = 3KCl + Al(OH) 3 ↓

Закрепление
1. Что такое основание, общая формула?
2. Какими по растворимости бывают основания?
3. Как называются основания хорошо растворимые в воде?
4. Дать определение индикаторам.
5. Выбрать основания и назвать их:
LiOH, K 2 O, BaO, Ca(OH) 2 .

Тест «Пятерочка»
- 1 . Выберите формулу оснований:
- а) SO 3 б) Mg(OH) 2 в) H 2 SO 4 г) СаО
- 2. К каждому из ниже указанных веществ прибавили фенолфталеин. С каким веществом появится малиновое окрашивание?
- а) BaO б) HNO 3 в) КОН
- 3. Гидроксид-ион (OH) ⁻ входит в состав:
- а) оксидов б) оснований в) углекислого газа
- 4.Окраска индикаторов под действием раствора гидроксида калия меняется следующим образом:
- а) лакмус синеет б) Метилоранж краснеет
- в) фенолфталеин бесцветный
- 5. Выберите формулу щелочи
- а) КОН б) H 2 S в) Сu(ОН) 2








































