Просмотр содержимого документа
«Презентация "Основания"»

Класс неорганических соединений
основания
Автор: Колесникова Н.А., учитель химии, биологии МБОУ «СОШ п.Дебин»

ЦЕЛИ УРОКА:
1 ) сформировать понятие об основаниях как электролитах;
2) рассмотреть классификацию оснований по различным признакам;
3) познакомить практически с химическими свойствами оснований в свете теории электролитической диссоциации;
4) развивать умения и навыки работы с химическими реактивами и химическим оборудованием;
5) учить сравнивать, анализировать, делать выводы;
6) совершенствовать умения и навыки в написании формул веществ и уравнений химических реакций.

Основания - это сложные вещества, в которых атом металла связан с одной или несколькими гидроксогруппами (ОН).
:
Названия оснований состоят из двух слов:
гидроксид + название металла в родительном падеже .
Если металл образует соединения с разными степенями окисления, то степень окисления указывается после названия металла в скобках римской цифрой:
Fe(OH) 2 ___ гидроксид железа ( II)
КОН ___ гидроксид калия
Mg(OH) 2 ___ гидроксид магния
LiOH ___ гидроксид лития
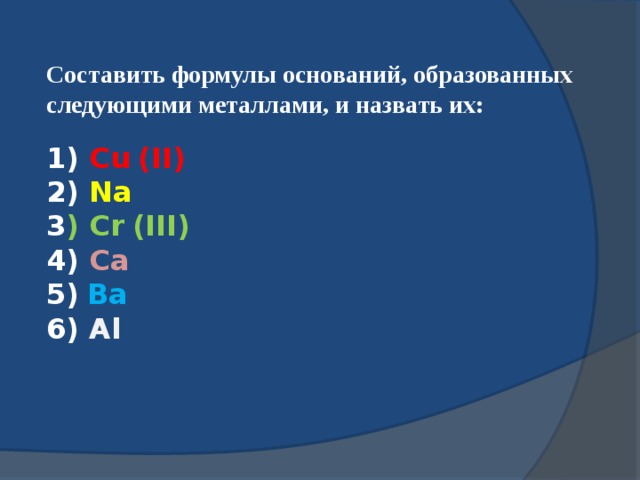
Составить формулы оснований, образованных следующими металлами, и назвать их:
1) Cu (II)
2) Na
3 ) Cr (III)
4) Ca
5) Ba
6) Al
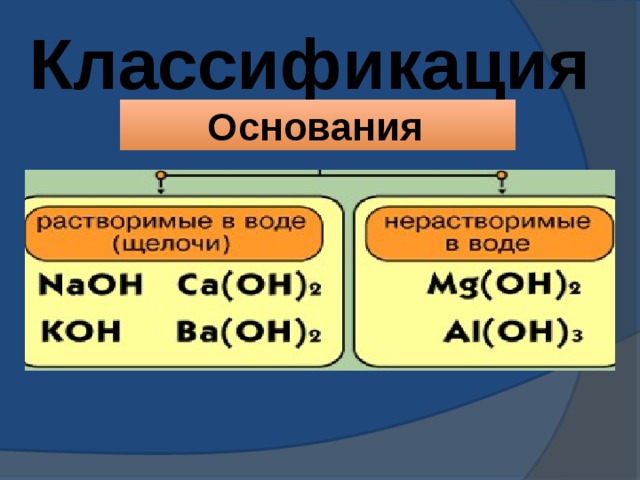
Классификация
Основания
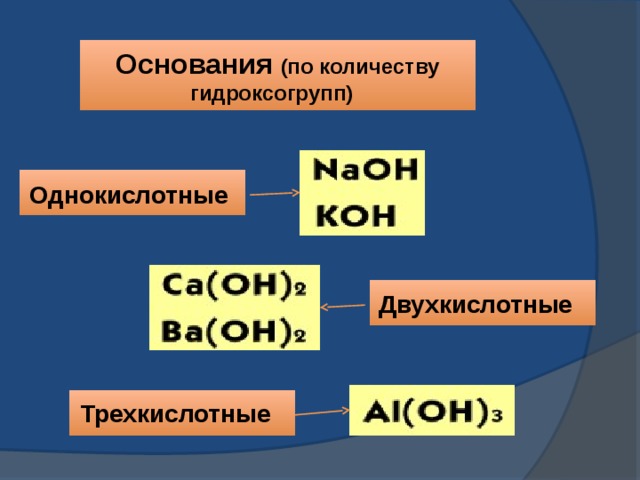
Основания (по количеству гидроксогрупп)
Однокислотные
Двухкислотные
Трехкислотные
KOH
BaO P 2 O 5 HCl
Mg(OH) 2
H 2 SO 4 NaCl H 2 O
MgOHCl K 2 O
NO AgNO 3 CaO Al 2 O 3
LiOH
Fe(OH) 3
Ba(OH) 2
Al(OH) 3
Ca(OH) 2
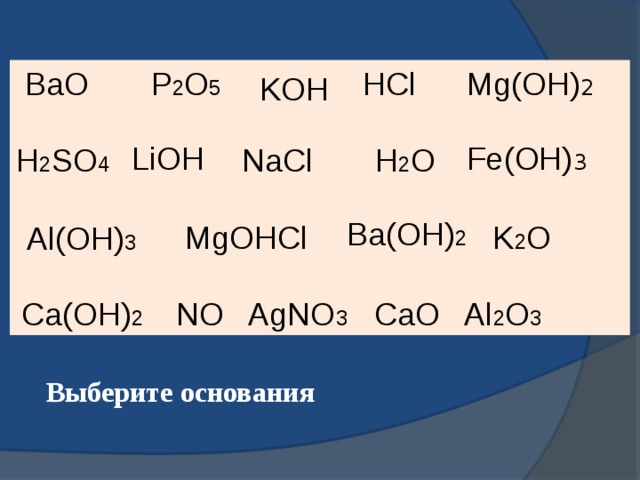
Выберите основания
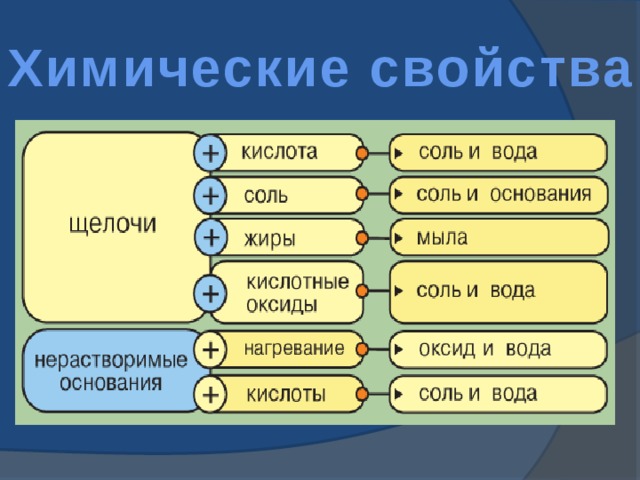
Химические свойства

ЗАПОМНИТЕ!
Основания ─ сложные вещества, состоящие из атома металла и одной или нескольких гидроксогрупп.
Гидроксогруппа ─ ОН – .
Растворимые в воде основания ─ щелочи .
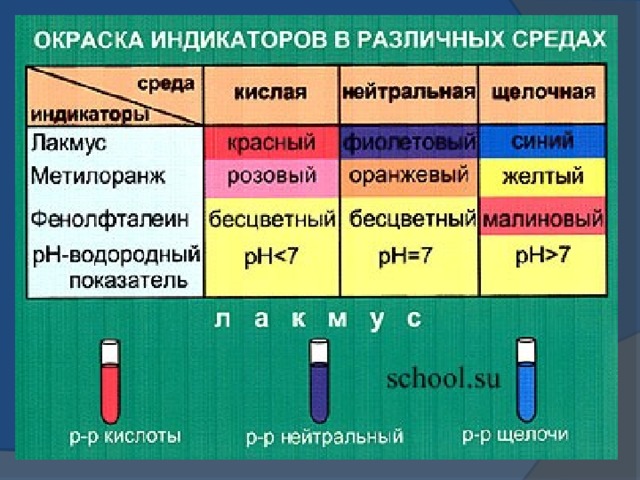
При контакте со щелочами фенолфталеин окрашивается в малиновый цвет, метилоранж ─ в желтый, универсальный индикатор и лакмус ─ в синий.
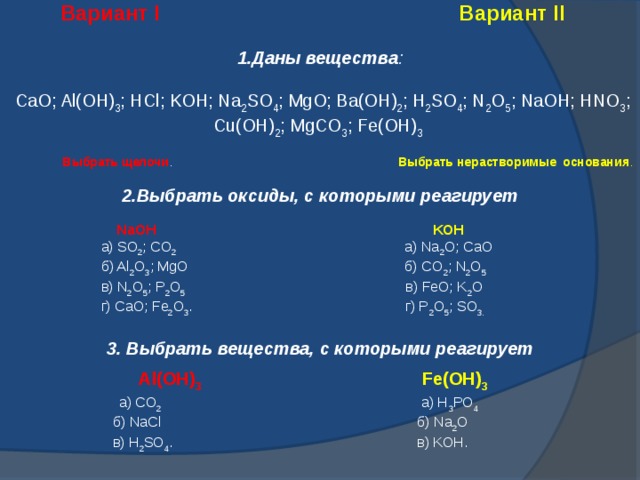
Вариант I Вариант II
1.Даны вещества :
CaO; Al(OH) 3 ; HCl; KOH; Na 2 SO 4 ; MgO; Ba(OH) 2 ; H 2 SO 4 ; N 2 O 5 ; NaOH; HNO 3 ; Cu(OH) 2 ; MgCO 3 ; Fe(OH) 3
Выбрать щелочи . Выбрать нерастворимые основания .
2.Выбрать оксиды, с которыми реагирует
NaOH KOH
а) SO 2 ; CO 2 а) Na 2 O; CaO
б) Al 2 O 3 ; MgO б) CO 2 ; N 2 O 5
в) N 2 O 5 ; P 2 O 5 в) FeO; K 2 O
г) CaO; Fe 2 O 3 . г) P 2 O 5 ; SO 3.
3. Выбрать вещества, с которыми реагирует
Al(OH) 3 Fe(OH) 3
а) CO 2 а) H 3 PO 4
б) NaCl б) Na 2 O
в) H 2 SO 4 . в) KOH.
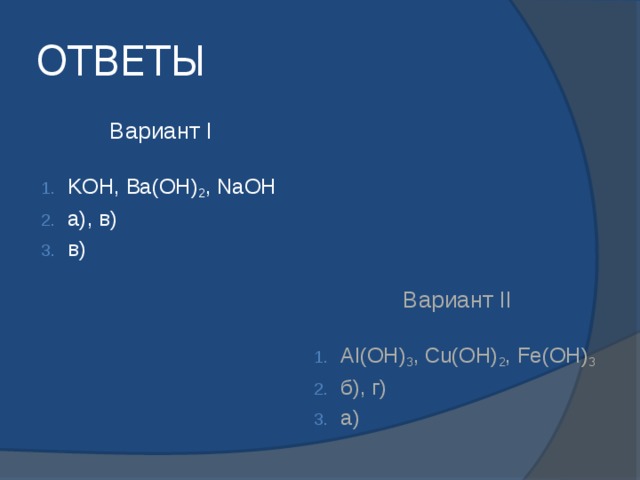
ОТВЕТЫ
Вариант I
Вариант II
- KOH, Ba(OH) 2 , NaOH
- а), в)
- в)
- Al(OH) 3 , Cu(OH) 2 , Fe(OH) 3
- б), г)
- а)
Дом.задание § 31
Спасибо за урок






































