
Важнейшие соединения кальция. Жесткость воды

 CaAl 2 O 4 + Ca При этом кальций получается в виде пара. Затем этот пар конденсируется. " width="640"
CaAl 2 O 4 + Ca При этом кальций получается в виде пара. Затем этот пар конденсируется. " width="640"
Получение
В промышленности кальций можно получить с помощью электролиза расплавленного хлорида кальция CaCl 2 .
- CaCl 2 = Ca + Cl 2
- Кальций также получают из оксидов с помощью алюминотермического восстановления .
4CaO + 2Al - CaAl 2 O 4 + Ca
При этом кальций получается в виде пара. Затем этот пар конденсируется.

Химические свойства

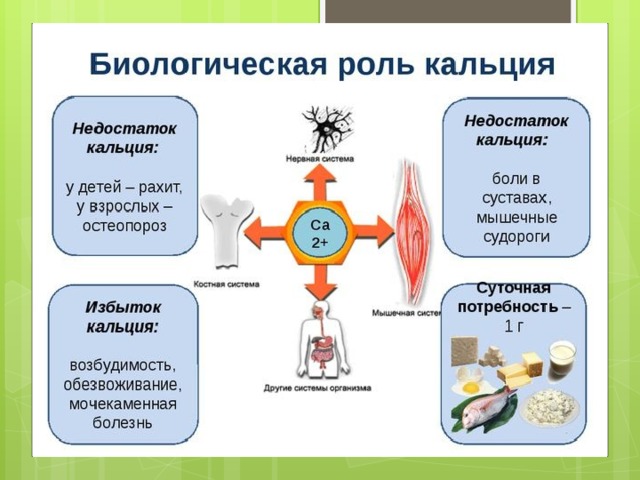
Соединения кальция

Применение Ca и его соединений

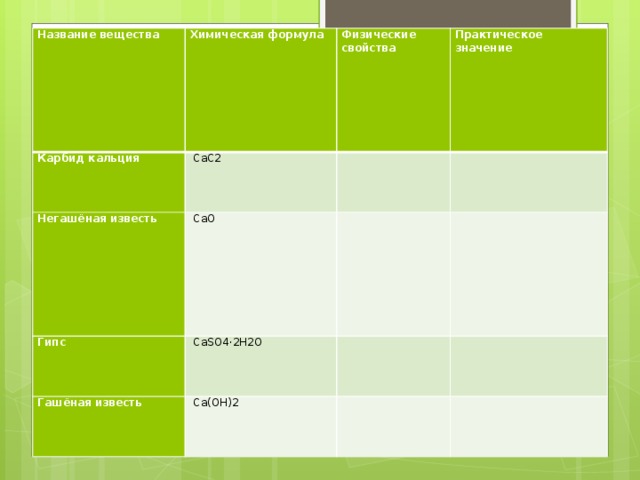
Название вещества
Химическая формула
Карбид кальция
Физические свойства
Негашёная известь
CaC2
Практическое значение
Гипс
CaO
CaSO4·2H2O
Гашёная известь
Ca(OH)2

Жесткость воды

Жесткость воды.
1. Жёсткость воды с точки зрения химии — совокупность физических процессов в воде, связанных с содержанием в ней растворённых солей щёлочноземельных металлов, главным образом, кальция и магния, так называемых, «солей жесткости».
Присутствие ионов Са 2+ и Mg 2+
2. Показатели жесткости воды
- Белые хлопья в воде Накипь и известковые отложения на бытовой технике Пленка на чае
- Белые хлопья в воде Накипь и известковые отложения на бытовой технике Пленка на чае
- Белые хлопья в воде
- Накипь и известковые отложения на бытовой технике
- Пленка на чае
3

Образование жесткости воды в природе
Подземные воды – подземные залежи известняков, гипса, доломитов жесткость воды.
Поверхностные воды – сезонные колебания.
Морская и океанская вода – высокая жесткость.
Пресные природные водоемы – минимум жесткости в период паводка.
4
 8.3) бикарбонатов кальция и магния - Са(HCO 3 ) 2 и Mg(HCO 3 ) 2 . Постоянная – некарбонатная жесткость , характеризуется присутствием сульфатных, нитратных и хлоридных анионов . CaCl 2 ; CaSO 4 ; MgCl 2 , MgSO 4 Общая жесткость определяется как суммарная величина наличия солей магния и кальция в воде, то есть суммой карбонатной и некарбонатной жесткости Типы жесткости воды. 5 почти полностью устраняется при кипячении воды, поэтому называется временной жесткостью. соли кальция и магния при кипячении не устраняются (постоянная жесткость). " width="640"
8.3) бикарбонатов кальция и магния - Са(HCO 3 ) 2 и Mg(HCO 3 ) 2 . Постоянная – некарбонатная жесткость , характеризуется присутствием сульфатных, нитратных и хлоридных анионов . CaCl 2 ; CaSO 4 ; MgCl 2 , MgSO 4 Общая жесткость определяется как суммарная величина наличия солей магния и кальция в воде, то есть суммой карбонатной и некарбонатной жесткости Типы жесткости воды. 5 почти полностью устраняется при кипячении воды, поэтому называется временной жесткостью. соли кальция и магния при кипячении не устраняются (постоянная жесткость). " width="640"
Временная – карбонатная жесткость , обусловлена присутствием в воде (при рН8.3) бикарбонатов кальция и магния - Са(HCO 3 ) 2 и Mg(HCO 3 ) 2 .
Постоянная – некарбонатная жесткость , характеризуется присутствием сульфатных, нитратных и хлоридных анионов . CaCl 2 ; CaSO 4 ; MgCl 2 , MgSO 4
Общая жесткость
определяется как суммарная величина наличия солей магния и кальция в воде, то есть суммой карбонатной и некарбонатной жесткости
Типы жесткости воды.
5
почти полностью устраняется
при кипячении воды, поэтому
называется временной жесткостью.
соли кальция и магния при кипячении не устраняются
(постоянная жесткость).

Устранение временной жесткости
I. Термоумягчение . (Кипячением воды.)
Ca(HCO 3 ) 2 = CaCO 3 ↓ + CO 2 + H 2 O .
II. Реагентное умягчение.
1. Добавлением кальцинированной соды.
Ca(HCO 3 ) 2 + Na 2 CO 3 = CaCO 3 ↓ + 2NaHCO 3 .
2. Добавлением гашеной извести.
Ca(HCO 3 ) 2 + Ca(OH) 2 = 2CaCO 3 ↓ + 2H 2 O.
6
![Устранение постоянной жесткости Реагентное умягчение . (Добавлением кальцинированной соды.) Реагентное умягчение . (Добавлением кальцинированной соды.) CaCl 2 + Na 2 CO 3 = CaCO 3 ↓ + 2NaCl. CaCl 2 + Na 2 CO 3 = CaCO 3 ↓ + 2NaCl. CaCl 2 + Na 2 CO 3 = CaCO 3 ↓ + 2NaCl. 2MgSO 4 + 2Na 2 CO 3 + H 2 O = =[Mg(OH)] 2 CO 3 ↓ + CO 2 ↑ + 2Na 2 SO 4 . 2MgSO 4 + 2Na 2 CO 3 + H 2 O = =[Mg(OH)] 2 CO 3 ↓ + CO 2 ↑ + 2Na 2 SO 4 . 2MgSO 4 + 2Na 2 CO 3 + H 2 O = =[Mg(OH)] 2 CO 3 ↓ + CO 2 ↑ + 2Na 2 SO 4 . 7](https://fsd.multiurok.ru/html/2019/03/20/s_5c9210d42eb4d/img14.jpg)
Устранение постоянной жесткости
- Реагентное умягчение . (Добавлением кальцинированной соды.)
- Реагентное умягчение . (Добавлением кальцинированной соды.)
- CaCl 2 + Na 2 CO 3 = CaCO 3 ↓ + 2NaCl.
- CaCl 2 + Na 2 CO 3 = CaCO 3 ↓ + 2NaCl.
- CaCl 2 + Na 2 CO 3 = CaCO 3 ↓ + 2NaCl.
- 2MgSO 4 + 2Na 2 CO 3 + H 2 O = =[Mg(OH)] 2 CO 3 ↓ + CO 2 ↑ + 2Na 2 SO 4 .
- 2MgSO 4 + 2Na 2 CO 3 + H 2 O = =[Mg(OH)] 2 CO 3 ↓ + CO 2 ↑ + 2Na 2 SO 4 .
- 2MgSO 4 + 2Na 2 CO 3 + H 2 O = =[Mg(OH)] 2 CO 3 ↓ + CO 2 ↑ + 2Na 2 SO 4 .
7

8

Влияние жесткости воды
на быт и здоровье человека.
- Сухость кожи Ломкость волос Шелушение, зуд Горьковатый вкус воды и негативное воздействие на органы пищеварения Плохие потребительские свойства Способствует образованию мочевых камней
- Сухость кожи Ломкость волос Шелушение, зуд Горьковатый вкус воды и негативное воздействие на органы пищеварения Плохие потребительские свойства Способствует образованию мочевых камней
- Сухость кожи
- Ломкость волос
- Шелушение, зуд
- Горьковатый вкус воды и негативное воздействие на органы пищеварения
- Плохие потребительские свойства
- Способствует образованию мочевых камней
- Перерасход на 30-50%
- Перерасход на 30-50%
- Перерасход на 30-50%
- Перерасход на 30-50%
- Перерасход на 30-50%
- Перерасход на 30-50%
- Перерасход на 30-50%
- Перерасход на 30-50%
- Перерасход на 30-50%
моющих средств
9
Проблема секущихся кончиков
волос

Влияние жесткости воды на бытовые и промышленные системы
Для современной бытовой техники,
автономных систем горячего водоснабжения и отопления,
новейших образцов сантехники жесткость воды –
катастрофа!
10









 CaAl 2 O 4 + Ca При этом кальций получается в виде пара. Затем этот пар конденсируется. " width="640"
CaAl 2 O 4 + Ca При этом кальций получается в виде пара. Затем этот пар конденсируется. " width="640"









 8.3) бикарбонатов кальция и магния - Са(HCO 3 ) 2 и Mg(HCO 3 ) 2 . Постоянная – некарбонатная жесткость , характеризуется присутствием сульфатных, нитратных и хлоридных анионов . CaCl 2 ; CaSO 4 ; MgCl 2 , MgSO 4 Общая жесткость определяется как суммарная величина наличия солей магния и кальция в воде, то есть суммой карбонатной и некарбонатной жесткости Типы жесткости воды. 5 почти полностью устраняется при кипячении воды, поэтому называется временной жесткостью. соли кальция и магния при кипячении не устраняются (постоянная жесткость). " width="640"
8.3) бикарбонатов кальция и магния - Са(HCO 3 ) 2 и Mg(HCO 3 ) 2 . Постоянная – некарбонатная жесткость , характеризуется присутствием сульфатных, нитратных и хлоридных анионов . CaCl 2 ; CaSO 4 ; MgCl 2 , MgSO 4 Общая жесткость определяется как суммарная величина наличия солей магния и кальция в воде, то есть суммой карбонатной и некарбонатной жесткости Типы жесткости воды. 5 почти полностью устраняется при кипячении воды, поэтому называется временной жесткостью. соли кальция и магния при кипячении не устраняются (постоянная жесткость). " width="640"

![Устранение постоянной жесткости Реагентное умягчение . (Добавлением кальцинированной соды.) Реагентное умягчение . (Добавлением кальцинированной соды.) CaCl 2 + Na 2 CO 3 = CaCO 3 ↓ + 2NaCl. CaCl 2 + Na 2 CO 3 = CaCO 3 ↓ + 2NaCl. CaCl 2 + Na 2 CO 3 = CaCO 3 ↓ + 2NaCl. 2MgSO 4 + 2Na 2 CO 3 + H 2 O = =[Mg(OH)] 2 CO 3 ↓ + CO 2 ↑ + 2Na 2 SO 4 . 2MgSO 4 + 2Na 2 CO 3 + H 2 O = =[Mg(OH)] 2 CO 3 ↓ + CO 2 ↑ + 2Na 2 SO 4 . 2MgSO 4 + 2Na 2 CO 3 + H 2 O = =[Mg(OH)] 2 CO 3 ↓ + CO 2 ↑ + 2Na 2 SO 4 . 7](https://fsd.multiurok.ru/html/2019/03/20/s_5c9210d42eb4d/img14.jpg)













