
Оксиды (знакомство с оксидами)
Презентация для учащихся 8-ых классов.

Что такое оксиды?
Оксиды – это сложные вещества, состоящие из двух элементов, один из которых кислород.
Общая формула:
Е m O n

Образцы оксидов
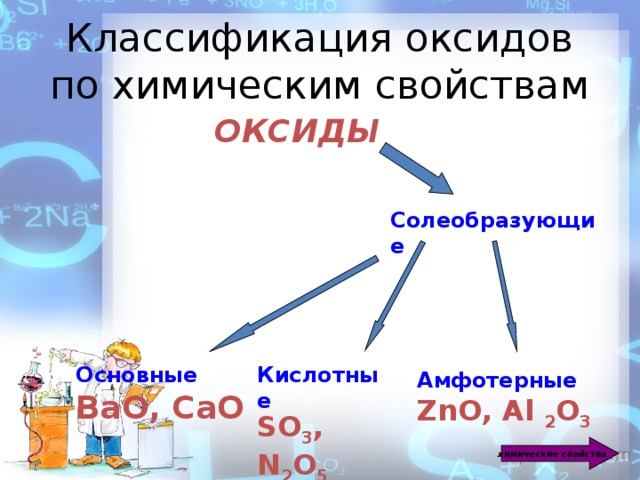
Классификация оксидов по химическим свойствам
ОКСИДЫ
Солеобразующие
Основные
Кислотные
ВаО, СаО
SO 3 , N 2 O 5
Амфотерные
ZnO, Al 2 O 3
химические свойства

Названия оксидов
Оксид алюминия Al 2 O 3
Оксид калия K 2 O
Оксид бария BaO
В случае, если элемент обладает переменной валентностью, то обязательно в скобках указывают валентность этого элемента в оксиде.
Оксид меди ( II ) С uO
Оксид серы ( VI) SO 3
Оксид углерода ( IV) CO 2

Какие элементы образуют кислотные и основные оксиды?
Основные оксиды образуют металлы, которые проявляют валентность I , II , III .
Примеры: Na 2 O, MgO, CaO, CuO, K 2 O, FeO.
Кислотные оксиды образуют неметаллы и металлы, которые проявляют валентность VI , VII (например М n 2 O 7 , С rO 3 ) .
SO 2 , P 2 O 5 , CO 2 , SiO 2 , N 2 O 5

Получение основных оксидов.
- Взаимодействие металлов с кислородом (горение)
2Mg + O 2 = 2MgO

Получение кислотных оксидов
Взаимодействие неметаллов с кислородом (горение)
S + O 2 = SO 2

Получение кислотных оксидов
Взаимодействие неметаллов с кислородом (горение)
4P + 5O 2 =2P 2 O 5

Химические свойства основных оксидов
Взаимодействие с водой:
Правило: при взаимодействии основных оксидов с водой образуются растворимые основания ( щелочи).
Примеры: Li 2 O + H 2 O = 2LiOH
Na 2 O + H 2 O = 2NaOH
K 2 O + H 2 O = 2KOH
BaO + H 2 O = Ba(OH) 2
CaO + H 2 O = Ca(OH) 2

Химические свойства основных оксидов
Обратите внимание! С водой взаимодействуют только оксиды активных металлов (лития, натрия, калия, бария, кальция )!

Химические свойства основных оксидов
Взаимодействие с кислотными оксидами:
Правило: при взаимодействии основных оксидов с кислотными оксидами образуется соль.
Примеры: Са О + N 2 O 5 = Ca (NO 3 ) 2
соль
Na 2 O + SO 3 = Na 2 SO 4
соль
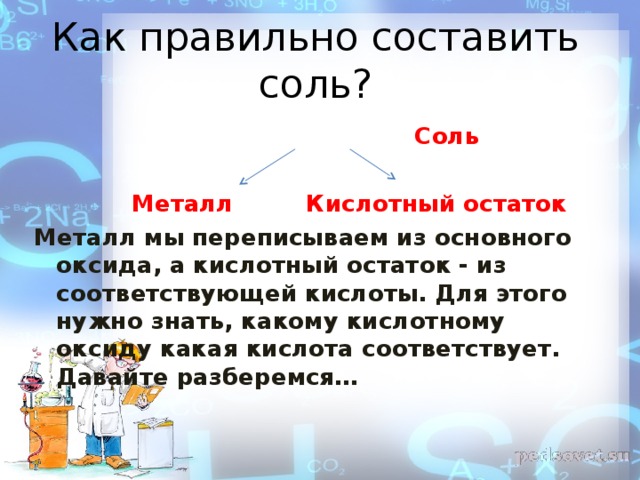
Как правильно составить соль?
Соль
Металл Кислотный остаток
Металл мы переписываем из основного оксида, а кислотный остаток - из соответствующей кислоты. Для этого нужно знать, какому кислотному оксиду какая кислота соответствует. Давайте разберемся…
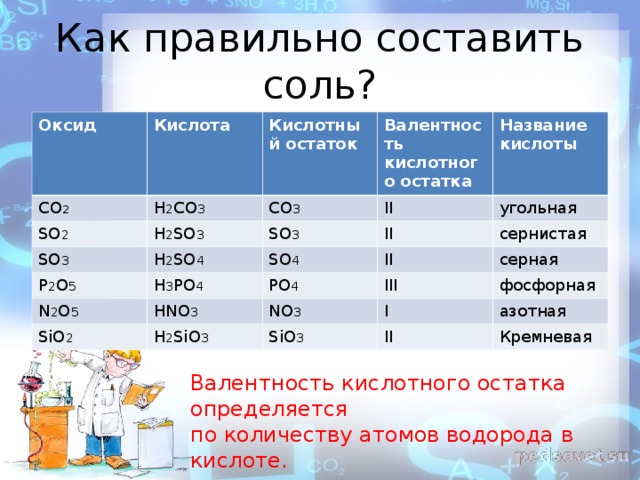
Как правильно составить соль?
Оксид
Кислота
СО 2
Н 2 СО 3
SO 2
Кислотный остаток
H 2 SO 3
Валентность кислотного остатка
SO 3
СО 3
Название кислоты
II
Р 2 О 5
SO 3
H 2 SO 4
II
Н 3 РО 4
SO 4
N 2 O 5
угольная
SiO 2
HNO 3
II
РО 4
сернистая
III
H 2 SiO 3
серная
NO 3
фосфорная
I
SiO 3
II
азотная
Кремневая
Валентность кислотного остатка определяется
по количеству атомов водорода в кислоте.

Как правильно составить соль?
Итак, рассмотрим алгоритм действий и составим соль в уравнении:
Са О + Р 2 О 5 =
- Выписываем металл ( Са) и рядом кислотный остаток, который соответствует вашему кислотному оксиду (РО4)
Са РО 4
2. Подписываем валентности металла и кислотного остатка
II III
Ca PO 4
3 . Находим НОК и уравновешиваем левую и правую часть формулы соли: Са 3 (РО 4 ) 2

Химические свойства основных оксидов
Взаимодействие с кислотами
Правило: При взаимодействии основных оксидов с кислотами образуются соль и вода.
Примеры: Ва О + 2H NO 3 = Ва ( NO 3 ) 2 + H 2 O
соль
3 K 2 O + 2H 3 PO 4 = 2 K 3 PO 4 + 3H 2 O
соль

Химические свойства кислотных оксидов
Правило: При взаимодействии кислотных оксидов с водой образуются кислоты (исключение составляет оксид кремния SiO 2 – речной песок не растворяется в воде)
Примеры: SO 3 + H 2 O = H 2 SO 4 ( серная кислота)
СО 2 + Н 2 О = Н 2 СО 3 (угольная кислота )

Химические свойства кислотных оксидов
2. Взаимодействие кислотных оксидов с основными оксидами (см. выше)
3. Взаимодействие с растворимыми основаниями.
Правило: При взаимодействии кислотных оксидов с растворимыми основаниями образуются соль и вода.

Химические свойства кислотных оксидов
Примеры: SO 2 + 2 Na OH = Na 2 SO 3 + H 2 O
соль
P 2 O 5 +3 Ba (OH) 2 = Ba 3 (PO 4 ) 2 +3H 2 O
соль

Закрепление пройденного материала

HCl
MgCl 2
CaO
Na 2 O
H 2 SO 4
HNO 3
Zn
Fe 2 O 3
SO 3
Выбери оксиды
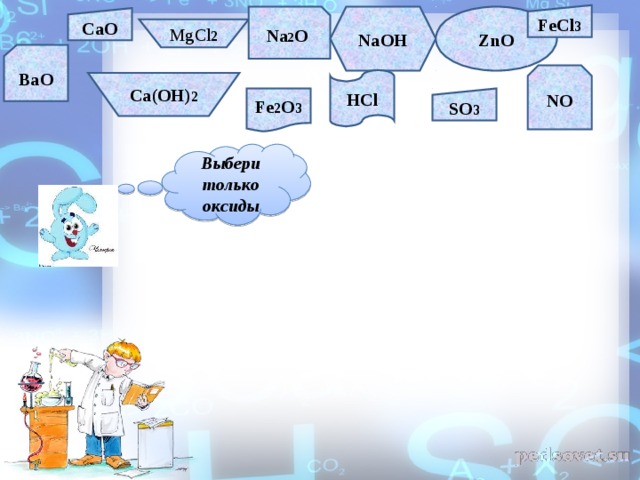
FeCl 3
Na 2 O
NaOH
ZnO
CaO
MgCl 2
BaO
NO
HCl
Ca(OH) 2
Fe 2 O 3
SO 3
Выбери только оксиды

2. Составьте формулы оксидов элементов
Магния
Калия
Алюминия
Фосфора ( V )
Хлора ( VII )
Железа ( III )
Углерода ( IV )
Серы ( VI )
Выпишите в два столбика оксиды металлов и неметаллов.

3 . Напишите уравнения реакций получения оксидов:
Оксида кальция
Оксида алюминия
Оксида серы ( IV)
Оксида фосфора ( V )
Оксида углерода ( IV)

4. Написать формулы оснований и кислот , которые соответствуют данным оксидам:
- SO 3 ,
- N 2 O 5 ,
- Al 2 O 3 ,
- CO 2 ,
- BaO,
- CaO
5 . С каким из веществ взаимодействует оксид меди (II ):
КОН
H 2 SO 4
N 2 O 5
H 2 O
HCl
Напишите реакции, которые идут

6. Закончите уравнения реакций которые идут и расставьте коэффициенты
FeO + H 2 O =
CO 2 + H 2 O =
SO 2 + Na 2 O =
Mg(OH) 2 + N 2 O 5 =
H 3 PO 4 + CaO =
Al 2 O 3 + HCl =
KOH + SO 3 =
SiO 2 + H 2 O =











































