
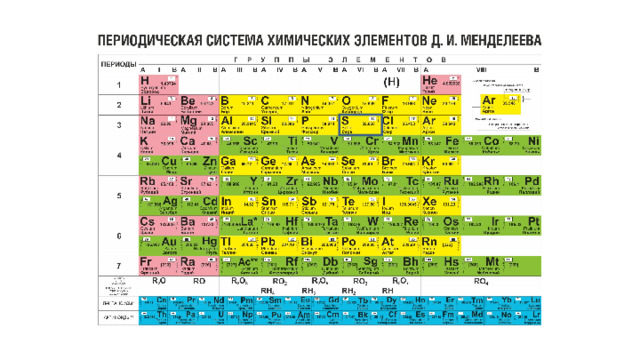
Сера.
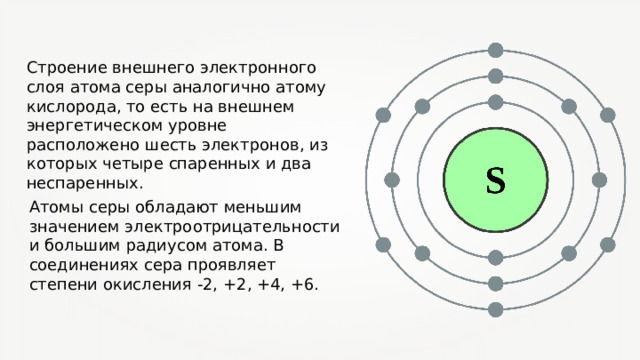
Строение внешнего электронного слоя атома серы аналогично атому кислорода, то есть на внешнем энергетическом уровне расположено шесть электронов, из которых четыре спаренных и два неспаренных.
Атомы серы обладают меньшим значением электроотрицательности и большим радиусом атома. В соединениях сера проявляет степени окисления -2, +2, +4, +6.
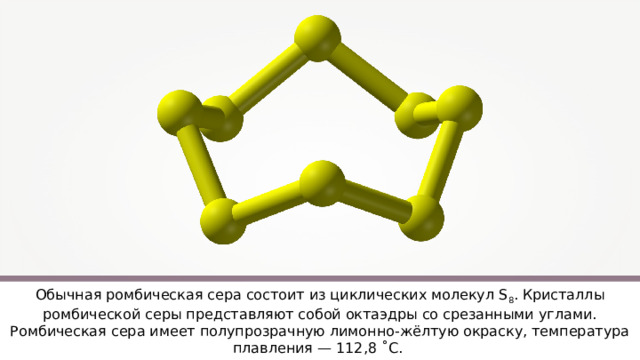
Обычная ромбическая сера состоит из циклических молекул S 8 . Кристаллы ромбической серы представляют собой октаэдры со срезанными углами. Ромбическая сера имеет полупрозрачную лимонно-жёлтую окраску, температура плавления — 112,8 ˚ С.

Пластическая сера


Сера не растворяется в воде.
Кристаллы серы в воде тонут, а порошок плавает по поверхности.
Сера хорошо растворима в
сероуглероде.

Сера и роман А. Дюма «Граф Монте-Кристо».

+2
-2
0
0
t
Реакции с металлами
Ca + S = CaS
Сульфид
кальция
Ca – восстановитель.
S – окислитель.
Ca
0
-2
0
+2
S
t
Hg + S = HgS
Сульфид
ртути (II)
Демеркуризация — удаление и обезвреживание ртути и её соединений с помощью серы.
Hg – восстановитель.
S – окислитель.
0
0
+1
-2
t
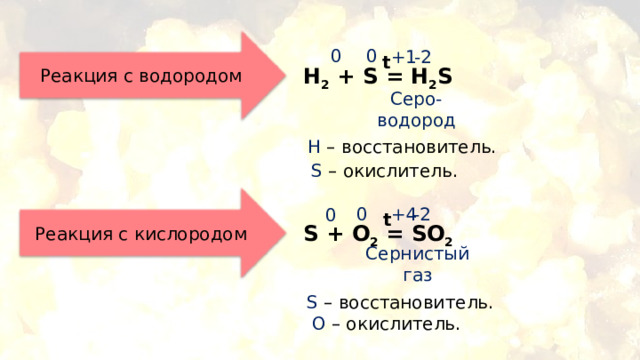
Реакция с водородом
H 2 + S = H 2 S
Серо-
водород
H – восстановитель.
S – окислитель.
0
+4
-2
0
t
Реакция с кислородом
S + O 2 = SO 2
Сернистый
газ
S – восстановитель.
O – окислитель.
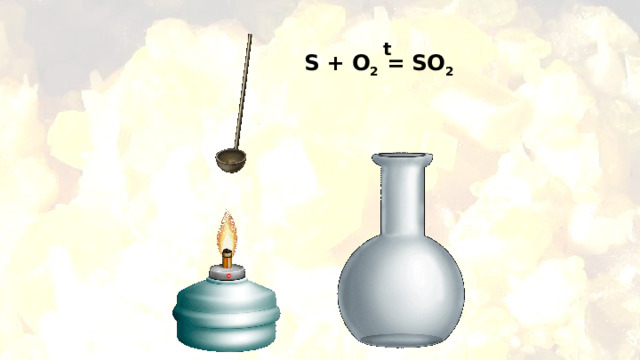
t
S + O 2 = SO 2

Химические свойства серы
С остальными металлами сера реагирует при нагревании:
Zn + S = ZnS
Окислительные свойства сера проявляет при взаимодействии с некоторыми неметаллами:
H 2 + S = H 2 S
11

Химические свойства серы
Взаимодействует со многими металлами, кроме золота и платины:
Mg + S = MgS
2Al + 3S = Al 2 S 3
Взаимодействует со всеми щелочными, щёлочноземельными металлами, а также медью, ртутью и серебром при обычных условиях:
Cu + S = CuS
Hg + S = HgS
11

Химические свойства серы
Из неметаллов с серой не реагируют только азот, йод и благородные газы. При взаимодействии с кислородом сера проявляет восстановительные свойства:
S + O 2 = SO 2
11

В природе сера встречается как в виде самородной серы, так и в
составе минералов и горных пород, таких как сульфиды и сульфаты.
15

C еры много в белках волос, шерсти, ногтей, рогов. Сера также является
важной составной частью некоторых витаминов и гормонов.

Если организму недостаточно серы,
то наблюдается хрупкость и ломкость костей, а также выпадение волос.


Продукты, содержащие серу

Применение серы
– производство серной кислоты;
– в качестве горючего вещества входит в состав чёрного пороха и спичечных головок;
– в сельском хозяйстве для борьбы с вредителями растений;
– в медицине для лечения кожных заболеваний;
– производство бумаги, красок, резины, косметических препаратов.

Установил элементарную природу серы 1 ноября 1772 г. в опытах по сжиганию.
Антуан Лоран Лавуазье
1 743 –1 794 гг.

Название « сера » восходит к лат. sera — « воск » или лат. serum — « сыворотка ». Лат. « sulphur» предположительно восходит к индоевропейскому корню « swelp » — « гореть ».

Применение серы

С запахом горящей серы, удушающим действием сернистого газа и отвратительным
запахом сероводорода человек познакомился ещё в доисторические времена.













































