
« Вода… Ты не имеешь ни вкуса ,ни цвета,
ни запаха, тебя невозможно описать – тобой наслаждаешься.
Ты не просто необходима для жизни, ты и есть сама жизнь.
Ты божество, ты совершенство,
ты самое большое богатство на свете »
Антуан де Сент - Экзюпери

Тема урока: «Вода»
Цель урока: рассмотреть распространение воды, изучить состав и строение молекулы воды, физические и химические свойства, рассмотреть экологические проблемы, связанные с загрязнением воды.

Распространение воды.
Вода - это самое распространенное на Земле вещество.
Почти ¾ поверхности земного шара покрыты водой, образующей океаны, моря, реки и озёра. Много воды находится в газообразном состоянии в виде паров в атмосфере, в виде огромных масс снега и льда лежит она круглый год на вершинах высоких гор и в полярных странах.
Природная вода не бывает совершенно чистой. Наиболее чистой является дождевая вода, а морская вода содержит больше всего примесей.

Вода в организме человека
Без воды человек может прожить только 3 дня, в то время как без пищи 30-50 дней.
В разных органах человека содержатся различные доли воды:
Стекловидное тело глаза - 99%
Плазма крови - 92%
Головной мозг – серое вещество 83%, белое вещество 70%;
Почки - 82%
Сердце - 79%
Легкие - 79%
Мышцы - 75%
Спинной мозг - 74,8%
Кожа - 72%
Печень -70%
Скелет - 46%
Зубная эмаль - 0,2%

Физические свойства воды
Вода – жидкость, без цвета, вкуса и запаха. При 0 С переходит в твёрдое состояние (лёд), при 100 С кипит и переходит в газообразное состояние ( водяной пар).
Вода – единственное вещество, которое встречается на Земле во всех трех агрегатных состояниях.
Жидкой водой наполнен Мировой океан, поверхностные воды суши и подземные воды
Твердый лед можно увидеть и в виде снежинок, и в виде инея
Водяной пар входит в состав атмосферы
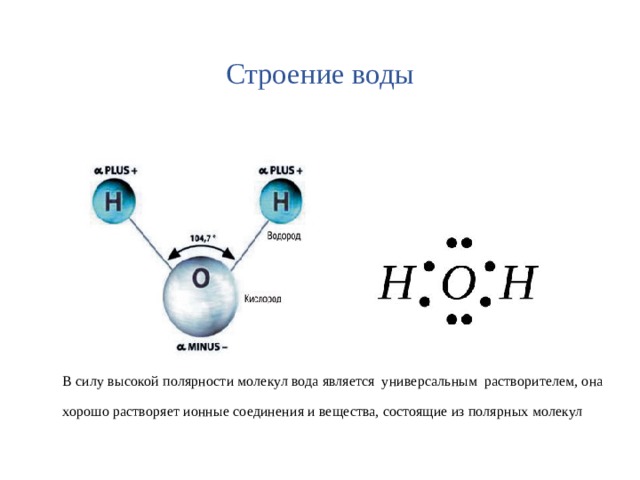
Строение воды
В силу высокой полярности молекул вода является универсальным растворителем, она хорошо растворяет ионные соединения и вещества, состоящие из полярных молекул

Водородная связь
Водородная связь — вид химического взаимодействия атомов в молекулах, отличающийся тем, что существенное участие в нём принимает атом водорода (Н), уже связанный ковалентной связью с другим атомом ( O ). Связи легко разрушаются и быстро восстанавливаются, что делает структуру воды исключительно изменчивой. Именно благодаря этим связям в отдельных микрообъемах воды непрерывно возникают своеобразные ассоциаты воды.

Химические свойства воды
1 . Взаимодействие с металлами:
- С активными металлами
- С менее активными металла
2. Взаимодействие с неметаллами
3. Взаимодействие с оксидами
- С оксидами металлов
- С оксидами неметаллов

Вода - как окислитель: Взаимодействует с активными (щелочными и щелочноземельными металлами)
Na + Н 2 О = ?
При нагревании возможно взаимодействие воды
и с менее активными металлами, например с
магнием.
Mg+ Н 2 О t°C ?

Вода - как восстановитель
Взаимодействует с таким окислителем
как фтор (вода горит во фторе).
2 F 2 +2H 2 O = 4HF+ O 2

Реакция разложения воды:
При t= 1500 °C или при пропускании электрического тока вода разлагается на простые вещества – кислород и водород
2 Н 2 О 2Н 2 + О 2
эл. ток


Применение воды
Гидроэлектростанция
Строительство
Машиностроение
Сельское хозяйство
В быту
Рефлексия
– Что нового вы узнали сегодня о воде?
– Можно ли считать, что ваши цели на урок достигнуты?
– Оцените свою деятельность на уроке, дайте оценку полученным знаниям, их значимости в дальнейшей деятельности.
Я понял, что … Я приобрел…
Я научился … Я научился…
Мне необходимо … У меня получилось…
Теперь я могу… Я смог…
Я почувствовал, что… Я попробую…
Меня удивило…
-Как вы оцениваете свои знания, полученные на уроке?
- Как вы оцениваете урок в целом?
4 балла
3 балла
5 балла

Домашнее задание
§ 20 , упр. 1-6
































