Реакции ионного обмена
6. Электролити-
ческая диссоциация
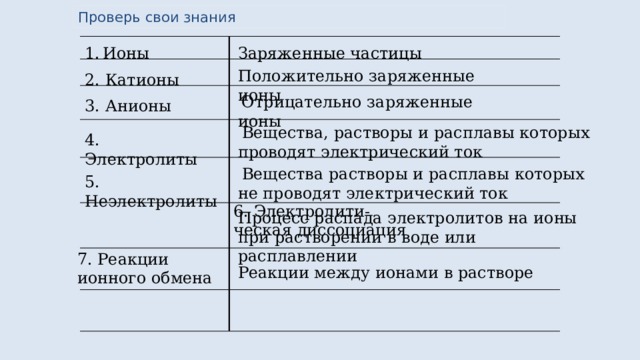
Проверь свои знания
Заряженные частицы
Положительно заряженные ионы
2. Катионы
Отрицательно заряженные ионы
3. Анионы
Вещества, растворы и расплавы которых проводят электрический ток
4. Электролиты
Вещества растворы и расплавы которых не проводят электрический ток
5. Неэлектролиты
Процесс распада электролитов на ионы при растворении в воде или расплавлении
7. Реакции ионного обмена
Реакции между ионами в растворе

Если выделится __________ – это раз,
И получится __________ – это два.
А ещё нерастворимый осаждается продукт.
«Есть ____________ », - говорим мы.
Это третий важный пункт.
Химик правила обмена не забудет никогда:
В результате непременно будет _____ или _____,
Выпадет _________ – вот тогда порядок!
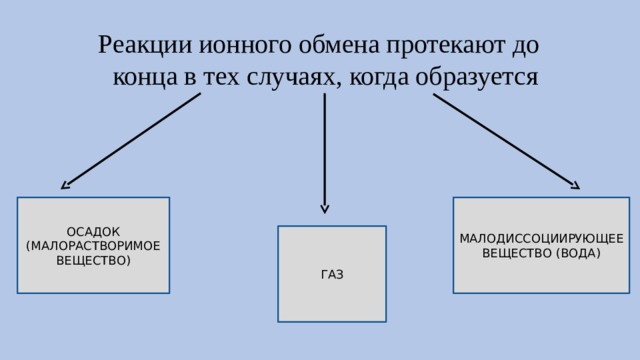
Реакции ионного обмена протекают до конца в тех случаях, когда образуется
ОСАДОК
МАЛОДИССОЦИИРУЮЩЕЕ ВЕЩЕСТВО (ВОДА)
(МАЛОРАСТВОРИМОЕ ВЕЩЕСТВО)
ГАЗ

Применение реакций ионного обмена
- Разрыхлители теста.
- Определение качества воды.
- Устранение жесткости воды.
- Определение качества продуктов питания.
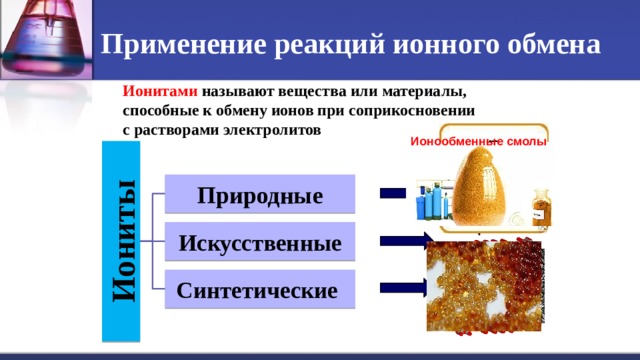
Иониты
Применение реакций ионного обмена
Ионитами называют вещества или материалы,
способные к обмену ионов при соприкосновении
с растворами электролитов
Ионообменные смолы
Природные
Цеолит
Искусственные
Синтетические

Применение ионитов
Очистка воды
- Для уменьшения жёсткости воды.
- Для обессоливания воды, при этом удаляются и катионы, и анионы путём последовательного прохождения воды через катионит и анионит.
- Удаление ионов железа.
- Очистка сточных вод промышленных предприятий.

Применение ионитов
В пищевой промышленности:
1. В производстве сахара.
2. В производстве дрожжей, фруктовых соков,
глицерина, глюкозы, сгущенного молока, какао,
кофе со сгущенным молоком.

Применение ионитов
Для извлечения металлов
С помощью ионитов извлекаются
редкие и рассеянные элементы из
полиметаллических руд.
В сельском хозяйстве иониты
используются для доставки
растениям необходимых им
элементов.
Mo
W

Применение ионитов
В медицине:
1. Для увеличения сроков хранения крови.
2. Для производства, выделения и очистки антибиотиков.
3. Использование ионитов, извлекающих
вредные вещества из крови человека.

Лабораторный опыт №8. Реакции между растворами электролитов.
С правилами ТБ ознакомлен(а) _____________
Цель: опытным путём изучить условия протекания ионных реакций.

- Ты в химкабинет пришел, Так запомни, кроха: Безопасность – хорошо! Быть безруким – плохо!
Ход работы
1
Что наблюдали
Уравнения реакций
№
Ход работы
2
Что наблюдали
Уравнения реакций
№
Ход работы
3
Что наблюдали
Уравнения реакций
№
Вывод:
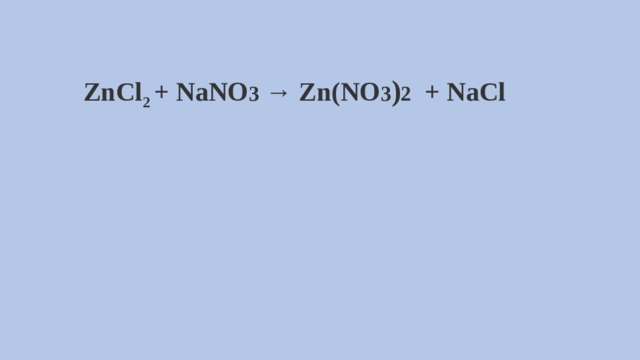
ZnCl 2 + NaNO 3 → Zn(NO 3 ) 2 + NaCl

Укажите ряд, в котором ионы каждой пары взаимодействуют в растворах с образованием осадка:
AgCl
1.SO 4 2- и H + ; Ag + и Cl -
Fe(OH) 2
2.Cl - и Fe 2+ ; Fe 2+ и OH -
Cu(OH) 2
3.OH - и Cu 2+ ; Na + и SiO 3 2-
BaSO 4
Cu(OH) 2
4.Ba 2+ и SO 4 2- ; Cu 2+ и OH -
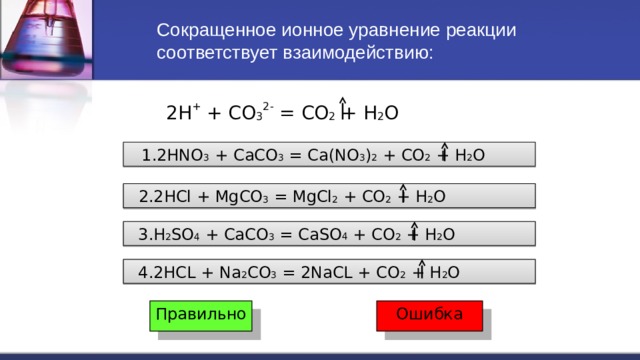
Сокращенное ионное уравнение реакции соответствует взаимодействию:
2H + + CO 3 2- = CO 2 + H 2 O
1.2HNO 3 + CaCO 3 = Ca(NO 3 ) 2 + CO 2 + H 2 O
2.2HCl + MgCO 3 = MgCl 2 + CO 2 + H 2 O
3.H 2 SO 4 + CaCO 3 = CaSO 4 + CO 2 + H 2 O
4.2HCL + Na 2 CO 3 = 2NaCL + CO 2 + H 2 O
Правильно
Ошибка

Сокращенное ионное уравнение реакции соответствует взаимодействию:
Al 2 O 3 + 6H + = 2Al 3+ + 6H 2 O
1.Al 2 O 3 + 3CO 2 = Al 2 (CO 3 ) 3
2.Al(NO 3 ) 3 + 3KOH = 3KNO 3 + Al(OH) 3
3.Al 2 O 3 + 3H 2 SO 4 = Al 2 (SO 4 ) 3 + 6H 2 O
4.AlCL 3 + H 2 O = AlOHCl 2 + + HCl
Правильно
Ошибка

§9,
карточка
(задания )

Лестница успеха
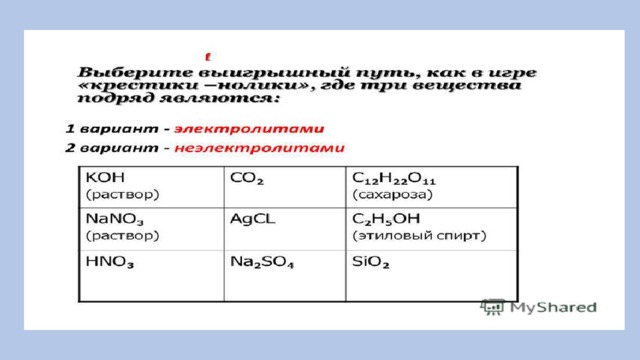
Выберите свой уровень успеха
5
4
3


1 . Реакции ионного обмена – это реакции: А. Разложения. В. Обмена Б. Замещения. Д. Соединения
2. Укажите уравнение реакции ионного обмена:
А. 2Al + 6HCl = 2AlCl 3 + 3H 2 Б. 2NaNO 3 = 2NaNO 2 + O 2 В. Аl 2 (SO 4 ) 3 + 6KOH = 2Al(OH) 3 + 3K 2 SO 4 Д. 3Ba + N 2 = Ba 3 N 2
3. Реакцией нейтрализации является реакция между парой веществ:
А. Сa(OH) 2 и NaCO 3 Б. MgSO 4 и BaCl 2 В. К 2 СO 3 и НCl Д. NaOH и Н 3 PO 4
4. Электролитом является каждое вещество в ряду: А. ВaO; H 2 SO 4 ; HNO 3 Б. AgCl; H 3 PO 4 ; CuSO 4 В. FeSO 4 ; AlCl 3 ; H 2 SO 4 Д. K 2 SO 4 ; H 2 ; MgCl 2
5. Формулы веществ, при
взаимодействии которых образуется вода: А. Fe(OH) 2 и HNO 3 Б. КOH и HNO 3 В. КOH и Zn(NO 3 ) 2 Д.MgCO 3 и Ba(NO 3 ) 2