
Состав ядра. Ядерные силы
Строение атома
Конкретные представления о строении атома развивались по мере накопления физикой фактов о свойствах вещества. Открыли электрон, измерили его массу. Мысль об электронном строении атома, впервые высказанную В. Вебером в 1896 г., развил Х. Лоренц. Именно он создал электронную теорию:
электроны входят в состав атома.
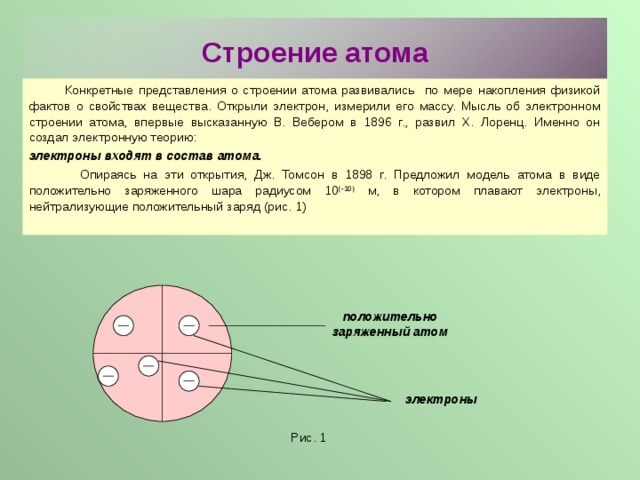
Опираясь на эти открытия, Дж. Томсон в 1898 г. Предложил модель атома в виде положительно заряженного шара радиусом 10 (-10) м, в котором плавают электроны, нейтрализующие положительный заряд (рис. 1)
положительно заряженный атом
электроны
Рис. 1
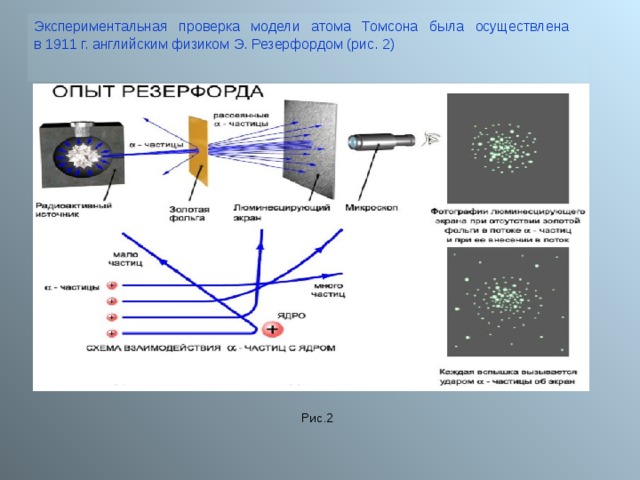
Экспериментальная проверка модели атома Томсона была осуществлена в 1911 г. английским физиком Э. Резерфордом (рис. 2)
Рис.2

Пропуская пучок Альфа- частиц через тонкую золотую фольгу, Э. Резерфорд обнаружил, что какая-то часть частиц отклоняется на довольно значительный угол от своего первоначального направления, а небольшая часть – отражается от фольги. Но согласно модели атома Томсона, частицы могли отклоняться только на углы около 2 0 (рис.3)
Резерфорд показал, что модель Томсона находится в противоречии с его опытами. Обобщая результаты своих опытов.
Резерфорд предложил ядерную ( планетарную) модель строения атома (рис.4)
- Атом имеет ядро, размеры которого малы по сравнению с размерами самого атома (рис. 5)
- В ядре сконцентрирована почти вся масса атома.
- Отрицательный заряд всех электронов распределен по всему объему атома.
Рис.3
Рис.4
Рис. 5
Открытие нейтрона
Идея о существовании тяжелой нейтральной частицы казалась Резерфорду настолько привлекательной, что он незамедлительно предложил группе своих учеников во главе с Дж. Чедвиком заняться поиском такой частицы.
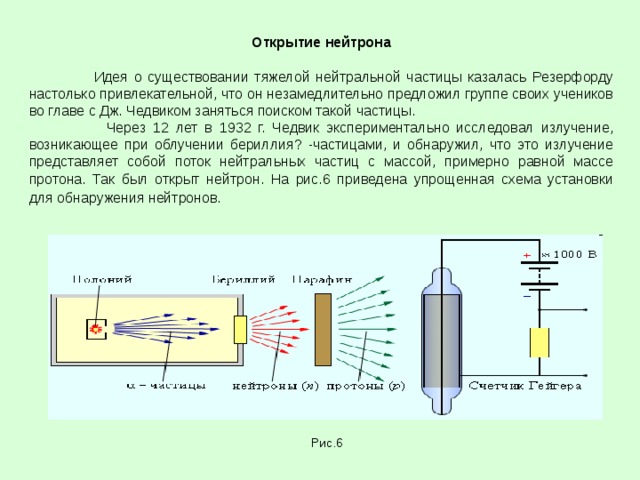
Через 12 лет в 1932 г. Чедвик экспериментально исследовал излучение, возникающее при облучении бериллия? -частицами, и обнаружил, что это излучение представляет собой поток нейтральных частиц с массой, примерно равной массе протона. Так был открыт нейтрон. На рис.6 приведена упрощенная схема установки для обнаружения нейтронов.
Рис.6
Нейтрон – это элементарная частица .
Это не протон -электронная пара, как первоначально предполагал Резерфорд.
По современным измерениям, масса нейтрона mn = 1,67493·10 –27 кг = 1,008665 а.е.м.
В энергетических единицах масса нейтрона равна 939,56563 МэВ .
Масса нейтрона приблизительно на две электронные массы превосходит массу протона.
Протон-нейтронная модель ядра
Сразу же после открытия нейтрона российский ученый Д. Д. Иваненко и немецкий физик В. Гейзенберг выдвинули гипотезу о протонно-нейтронном строении атомных ядер , которая полностью подтвердилась последующими исследованиями (рис. 7)
По современным измерениям, положительный заряд протона в точности равен элементарному заряду e = 1,60217733·10–19 Кл,
то есть равен по модулю отрицательному заряду электрона. В настоящее время равенство зарядов протона и электрона проверено с точностью 10 –22 . Такое совпадение зарядов двух непохожих друг на друга частиц вызывает удивление и остается одной из фундаментальных загадок современной физики.
Масса протона, по современным измерениям, равна mp = 1,67262·10-27 кг .
Протоны и нейтроны в ядре
принято называть нуклонами.
Рис. 7
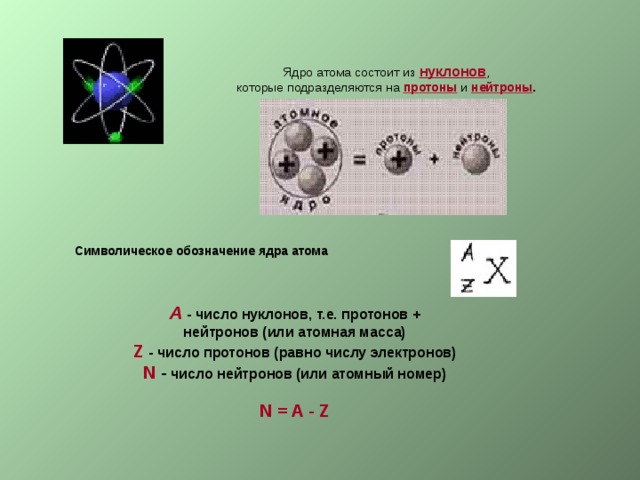
Ядро атома состоит из нуклонов ,
которые подразделяются на протоны и нейтроны .
Символическое обозначение ядра атома
А - число нуклонов, т.е. протонов + нейтронов (или атомная масса) Z - число протонов (равно числу электронов) N - число нейтронов (или атомный номер)
N = A - Z
Рис.8
Для того, чтобы атомные ядра были устойчивыми, протоны и нейтроны должны удерживаться внутри ядер огромными силами, во много раз превосходящими силы кулоновского отталкивания протонов. Силы, удерживающие нуклоны в ядре, называются ядерными ( рис.8)
Особенности ядерных сил:
- Ядерные силы примерно в 100 раз превосходят электростатические силы и на десятки порядков превосходят силы гравитационного взаимодействия нуклонов.
2. Важной особенностью ядерных сил является их короткодействующий характер. Ядерные силы заметно проявляются, как показали опыты Резерфорда по рассеянию
a-частиц, лишь на расстояниях порядка размеров ядра (10 –14 –10 –15 м). Ядерные силы очень быстро спадают с расстоянием. Радиус их действия порядка 0,000 000 000 000 001 метра .
Для этой сверхмалой длины, характеризующей размеры атомных ядер, ввели специальное обозначение Фм (в честь итальянского физика Э. Ферми, 1901-1954)
Все ядра имеют размеры нескольких Ферми.
Радиус ядерных сил равен размеру нуклона, поэтому ядра – концентрация и очень плотной материи. Возможно, самой плотной в земных условиях.
Ядерные силы - сильные взаимодействия .
На больших расстояниях проявляется действие сравнительно медленно убывающих кулоновских сил.
На основании опытных данных можно заключить, что протоны и нейтроны в ядре ведут себя одинаково в отношении сильного взаимодействия, т. е. ядерные силы не зависят от наличия или отсутствия у частиц электрического заряда.
ЯДЕРНЫЕ СИЛЫ
- силы притяжения;
- действуют между всеми нуклонами в ядре;
- короткодействующие.
.

ЗНАЕШЬ ЛИ ТЫ ? В середине XX века теория ядра предсказала существование стабильных элементов с порядковыми номерами Z = 110 -114 В Дубне был получен 114-й элемент с атомной массой А = 289, который "жил" всего 30 секунд, что невероятно долго для атома с ядром такого размера. Сегодня теоретики уже обсуждают свойства сверхтяжелых ядер массой 300 и даже 500.

Атомы с одинаковыми атомными номерами называют изотопами : в таблице Менделеева они расположены в одной клеточке (по-гречески «изос» - равный, «топос» – место (рис. 9). Химические свойства изотопов почти тождественны. Если элементов всего в природе - около 100, то изотопов - более 2000. Многие из них неустойчивы, то есть радиоактивны, и распадаются, испуская различные виды излучений. Изотопы одного и того же элемента по составу отличаются лишь количеством нейтронов в ядре.
Рис. 9

Решение задач:
- Сколько нуклонов, протонов и нейтронов содержится в ядрах следующих элементов:
11 Na 23
A = 23 N = 23 – 11 = 12 Z = 11
11 Na 21
A = 21 N = 21 – 11 = 9 Z = 11
4 B 9
A = 9 N = 9 – 4 = 5 Z = 4
Самостоятельно: 8 O 16 3 Li 7 6 C 12 7 N 14 9 F 19 13 Al 27 92 U 235 82 Pb 207
2. Чем отличаются следующие элементы:
8 О 17 и 8 О 16 92 U 235 и 92 U 239


























