
Исследование
проблемы коррозии
медных скульптур
кровли
Зимнего дворца
города Санкт-Петербурга

Как восстановить и сохранить медные скульптуры кровли Зимнего дворца города Санкт-Петербурга, которые подвергаются коррозии?

Найденные способы позволят восстановить и защитить от коррозии медные скульптуры кровли Зимнего дворца города Санкт-Петербурга.

Объектная область, объект, предмет исследования
Объектная область исследования –
электрохимия, материаловедение, история архитектуры.
1
Объект исследования – медные скульптуры кровли
Зимнего дворца города Санкт-Петербурга.
2
Предмет исследования – коррозия медных изделий.
3
В презентации рекомендуется делать не более 5-6 разделов. Оптимально 2-4.
Для того чтобы ввести название разделов, необходимо ввести название в соответствующей строке.
Хорошем стилем является наличие навигации по презентации (переход на нужный раздел из оглавления). Это возможно с помощью добавления гиперссылок. Для этого щелкните правой кнопкой мыши на серый прямоугольник, выберите из контекстного меню пункт «Гиперссылка». В открывшемся окне выберете пункт «местном в документе» (слева). И справа, в этом же окне, выберете интересующий слайд, после чего щелкните ОК. Гиперссылка добавлена. Аналогично проделайте с остальными прямоугольниками.

Объектная область, объект, предмет исследования
Объектная область исследования –
электрохимия, материаловедение, история архитектуры.
1
Объект исследования – медные скульптуры кровли
Зимнего дворца города Санкт-Петербурга.
2
Предмет исследования – коррозия медных изделий.
3
В презентации рекомендуется делать не более 5-6 разделов. Оптимально 2-4.
Для того чтобы ввести название разделов, необходимо ввести название в соответствующей строке.
Хорошем стилем является наличие навигации по презентации (переход на нужный раздел из оглавления). Это возможно с помощью добавления гиперссылок. Для этого щелкните правой кнопкой мыши на серый прямоугольник, выберите из контекстного меню пункт «Гиперссылка». В открывшемся окне выберете пункт «местном в документе» (слева). И справа, в этом же окне, выберете интересующий слайд, после чего щелкните ОК. Гиперссылка добавлена. Аналогично проделайте с остальными прямоугольниками.

Найти способы, которые позволят восстановить и защитить от коррозии медные скульптуры кровли Зимнего дворца города Санкт-Петербурга.

- познакомиться с историей Зимнего дворца и скульптур на его кровле;
- найти и изучить информацию о свойствах меди;
- найти и изучить информацию о коррозии металлов, в частности меди;
- найти и изучить информацию о способах защиты от коррозии металлов;
- изучить материалы по практическому проведению экспериментов по коррозии металлов;
- провести эксперименты по изучению коррозии меди и защите от коррозии;
- найти эффективные способы защиты медных скульптур от коррозии.

«Наука и искусство – это два подхода к познанию мира. Чтобы лучше развить в себе творческое начало и интуицию, которые необходимы для решения научных задач, учёный должен отдать часть своей души искусству – живописи, музыке, литературе. Искусство возвышает душу любого человека, а учёному,
в качестве «побочного эффекта», увеличивает творческие силы в профессиональной области».
Дмитрий Иванович Менделеев



Император
Пётр I

Архитектор Ф.Б. Растрелли
Императрица
Анна Иоановна

Императрица
Елизавета Петровна

Императрица
Екатерина II


Архитектор А.П. Брюллов
Архитектор В.П. Стасов
Скульптурное убранство кровли Зимнего дворца состоит из 176 фигур, выполненных из вальцованной красной листовой меди.

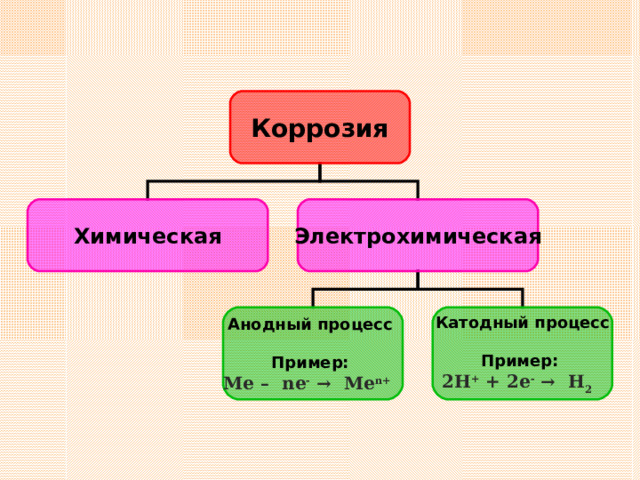
Коррозия
Химическая
Электрохимическая
Анодный процесс
Пример:
Катодный процесс
Пример:
Me – nе - → Ме n+
2Н + + 2е - → Н 2

↓
↑↓ ↑↓ ↑↓ ↑↓ ↑↓
↑↓ ↑↓ ↑↓
↑↓
↑↓ ↑↓ ↑↓
↑↓
↑↓
Слово патина (итальянское patina ) обозначает плёнку различных оттенков, образующуюся на поверхности меди и медьсодержащих сплавов под воздействием атмосферных факторов при естественном или искусственном старении.
Первая серия опытов Исследование процесса электролитической коррозии меди
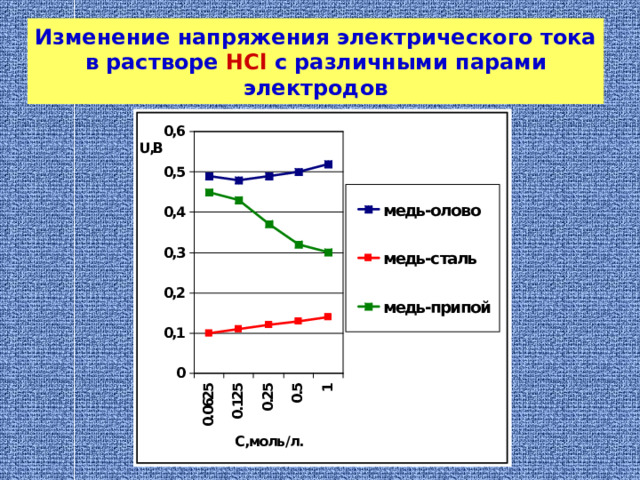
Изменение напряжения электрического тока в растворе HCl с различными парами электродов

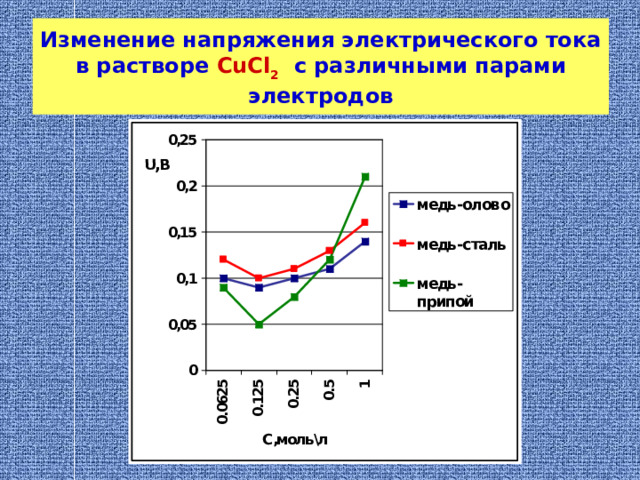
Изменение напряжения электрического тока в растворе CuCl 2 с различными парами электродов

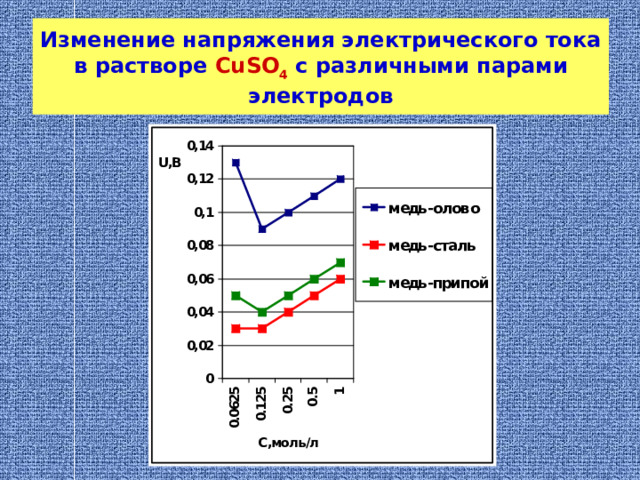
Изменение напряжения электрического тока в растворе CuSO 4 с различными парами электродов

Скачок на графиках зависимости напряжения от концентрации электролита объясняется следующими факторами:
- затруднением ионизации металла при данной концентрации электролита;
- сдерживанием диффузии образованных ионов металла в раствор;
- образованием на поверхности металла тонких плёнок, электронных слоёв.

Вторая серия опытов Исследование состава патины
(CuOH) 2 CO 3 ↓ = H 2 O + CO 2 ↑ + CuO
CO 2 + Ca(OH) 2 = CaCO 3 + H 2 O
CuO + H 2 SO 4 = CuSO 4 + H 2 O
CuSO 4 Cu 2+ + SO 4 2-
Ag + + Cl - = AgCl↓

Определение карбонат-ионов CO 3 2-
и ионов меди Cu 2+
Взаимодействие полученного оксида
меди ( II ) с раствором серной кислоты
Определение хлорид-ионов Cl -
с помощью раствора нитрата серебра

Исследования образца патины показало, что в её состав вход я т
лазурно-голубой азурит Cu 3 (CO 3 ) 2 (OH) 2 ,
зелёный паратакамит Cu 2 Cl(OH) 3 .

Третья серия опытов Очистка меди от загрязнений
Очистка мед и кальцинированной содой Na 2 CO 3 ,
тринатрийфосфатом Na 3 PO 4 •12 H 2 O .
Промывка водой
м едной пластинки .

Четвёртая серия опытов Окрашивание меди

Пятая серия опытов Обработка очагов активной коррозии окисью серебра
2С uCl + Ag 2 O = Cu 2 O + 2 AgCl
Очаги активной коррозии на медной пластинке,
покрытой патиной после обработки оксидом серебра.
Очаги активной коррозии
на медной пластинке,
покрытой патиной.

Шестая серия опытов Патинирование серной печенью
Нагревание смеси
серы и поташа.
Патинирование медной
пластинки серной печенью.

Подведение итогов
- Слово патина (итальянское patina) обозначает плёнку различных оттенков, образующуюся на поверхности меди и медьсодержащих сплавов под воздействием атмосферных факторов при естественном или искусственном старении.
- В естественных условиях зелёная патина образуется на поверхности медного кровельного листа в течение 5-25 лет, в зависимости от климата и химического состава атмосферы и осадков.

- Исследования образца патины показало, что в её состав входит лазурно-голубой азурит Cu 3 (CO 3 ) 2 (OH) 2 , зелёный паратакамит Cu 2 Cl(OH) 3 .
- Проведены эксперименты по очистке меди.
- Проведены эксперименты по защите меди от коррозии:
- окрашивание меди; б)обработка очагов активной коррозии окисью серебра; в)патинирование серной печенью.
6. Получены устойчивые защитные покрытия для меди.


























































