Просмотр содержимого документа
«Презентация урока по химии 8 класс "Относительная атомная масса химических элементов" УМК Рудзитис Г.Е.»
Простые и сложные вещества
Тест

1. Простое вещество – это вещество,
А)которое не имеет постоянный состав
Б)которое нельзя выделить из смеси
В)содержащее атомы одного химического элемента
Г)содержащее атомы разных химических элементов

2.Сложное вещество-это вещество,
А) содержащее атомы разных химических элементов
Б)содержащее атомы одного химического элемента
В)которое не содержит примеси
Г)которое редко встречается в природе

3. Простым веществом будет
А)нитрат меди
Б)медный купорос
В)медь
Г)оксид меди

4. Сложным веществом будет
А)кислород
Б)водород
В)марганец
Г)оксид марганца
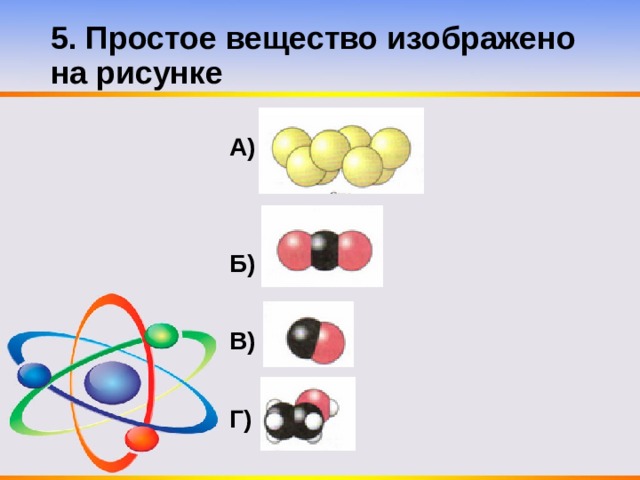
5. Простое вещество изображено на рисунке
А)
Б)
В)
Г)
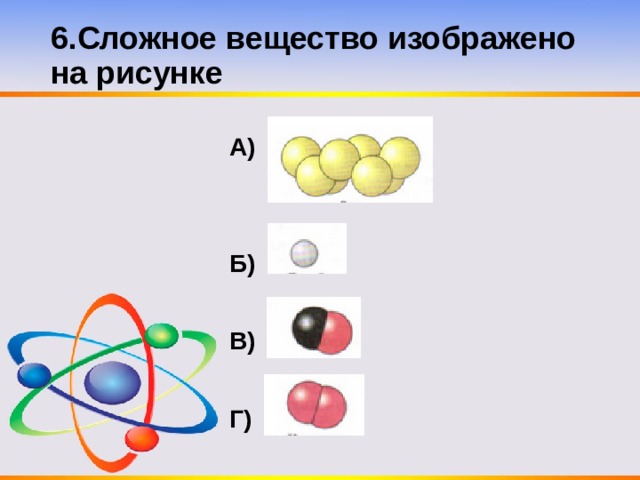
6.Сложное вещество изображено на рисунке
А)
Б)
В)
Г)


Правильные ответы
1-в
2-а
3-в
4-г
5-а
6-в
Оценка
«5»- 0 ошибок
«4»- 1 ошибка
«3»-2-3 ошибки
«2»- 4 и более

Относительная атомная масса химических элементов

Цель урока
Познакомиться с понятиями:
-масса атома
-атомная единица массы
-относительная атомная масса

Химический элемент
- это определенный вид атомов
- Известно 114 элементов они «живут» в Периодической Системе Д.И.Менделеева
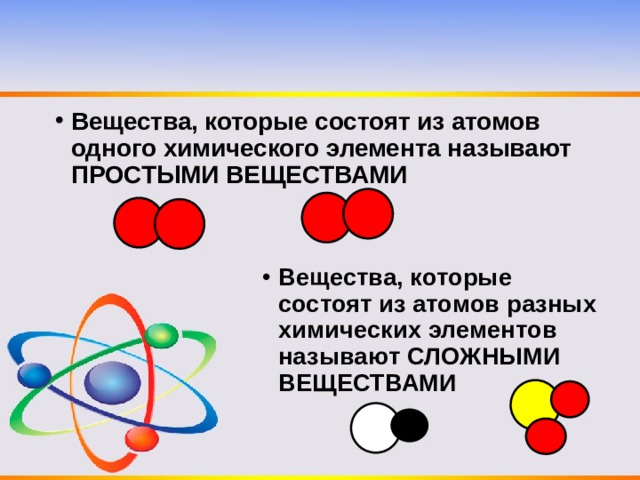
- Вещества, которые состоят из атомов одного химического элемента называют ПРОСТЫМИ ВЕЩЕСТВАМИ
- Вещества, которые состоят из атомов разных химических элементов называют СЛОЖНЫМИ ВЕЩЕСТВАМИ

Размеры и массы молекул очень малы, а атомов еще меньше.
Самым легким является атом водорода.
Масса атома водорода (Н)=1,67375 · 10 –24 г,
Масса атома кислорода (О)=2,656812 · 10 -23 г,
Масса атома углерода (С)=1,9927 · 10 –23 г.

- Число атомов водорода в 1 см 3 при Т= 0 °С и Р= 1 атм. так велико, что если мы будем считать их со скоростью два атома в секунду, то, чтобы пересчитать все, понадобится около 900 миллиардов лет.
Производить расчеты с такими числами неудобно!

Тогда придумали Единицу сравнения
это -
Атомная Единица Массы (а.е.м.)
1 а.е.м. = 1/12 массы атома углерода
(изотопа 12).
Ее масса тоже равна 1,66057 ▪ 10 -24 г.

Все истинные массы поделили на единицу сравнения
и получили относительную атомную массу, которая обозначается Аr и измеряется в условных единицах (усл.ед)
1,66057 ▪ 10 - 24 г
1,66057▪10 -24 г
Аr (Н)=
= 1усл.ед.
2,66▪10 -23 г
1,66057▪10 -24 г
= 16усл.ед.
Аr (О)=
Эти величины изображены в клеточке каждого элемента Периодической Системы Д.И.Менделеева

Выполни задание
Найти:
- Аr(N) =
- Аr(Р) =
- Аr(С) =
- Аr(I) =
- Аr(Zn) =
- Аr(Au) =
- Аr(Fe) =
- Аr(Сa) =
- Аr(Al) =
- Аr(Si) =

Выполни задание
Могут ли существовать в природе:
- 14 усл.ед.N
- 64 усл.ед. О
- 36 усл.ед. Mg
- 80 усл.ед. S
- 6 усл.ед. C

Домашнее задание
- §10, 11, упр.3(п) стр.41.
- §9.




































