
Monday, March 21, 2022
ВЫЧИСЛЕНИЯ
по химическим формулам. Массовая доля химического элемента в соединении.

Домашнее задание:
Из § 15 проработать примеры 1-3,
у.1,2,3(а)
1
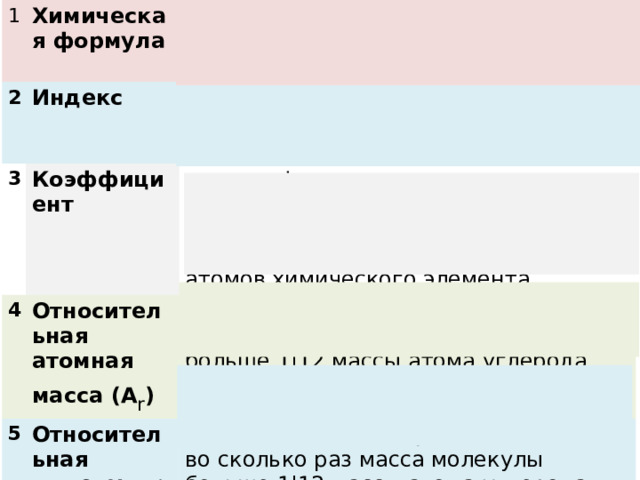
Химическая формула
2
– условная запись состава вещества с помощью символов химических элементов и цифр – индексов
Индекс
3
4
- это цифра, стоящая внизу справа от химического символа в формуле, показывает число атомов в молекуле.
Коэффициент
5
Относительная атомная масса (А r )
- это цифра, если стоит перед химической формулой, показывает число молекул; если перед химическим знаком – число свободных атомов химического элемента.
- это величина, которая показывает, во сколько раз масса данного атома больше 1|12 массы атома углерода
Относительная молекулярная масса (М r )
- это величина, которая показывает, во сколько раз масса молекулы больше 1|12 массы атома углерода
03/21/2022

Чтение химических формул
Пример:
Al(OH) 3 – 1 молекула алюминий о аш трижды состоит из одного атома алюминия , трех атомов кислорода и трех атомов водорода .
Аl 2 ( SO 4 ) 3
P 2 O 5
Ca(OH) 2
(NH 4 ) 3 PO 4
AgNO 3
Fe 2 O 3
C 8 H 18
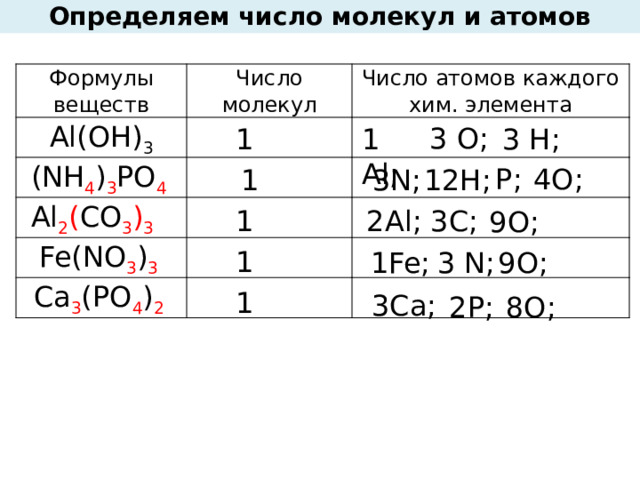
Определяем число молекул и атомов
Формулы веществ
Аl(ОН) 3
Число молекул
Число атомов каждого хим. элемента
(NH 4 ) 3 PO 4
Al 2 ( CO 3 ) 3
Fe(NO 3 ) 3
Ca 3 (PO 4 ) 2
3 О;
1
3 Н;
1 Аl;
4О;
Р;
12Н;
1
3N;
1
3С;
2Аl;
9О;
1
3 N;
1Fe;
9О;
1
3Ca;
8О;
2Р;

у. 4.c.49 Что означает запись?
4Н
4 отдельных атомов водорода
2Н 2
2 молекулы простого вещества образованы двумя атомами водорода
НgО
1 молекула сложного вещества образована 1 атомом ртути и 1 атомом кислорода
5FeS
5 молекул сложного вещества образованы 1 атомом железа и 1 атомом серы
3Н 2 SО 4
3 молекулы сложного вещества образованы 2 атомами водорода, 1 атомом серы и 4 атомами кислорода

Относительная молекулярная масса М r
Из атомов складываются молекулы, а из относительных атомных масс - относительные молекулярные массы (Mr).
Величина, которая показывает, во сколько раз масса молекулы больше 1/12 массы атома углерода , называют относительной молекулярной массой ( М r )
31 + 1 · 3 = 34
А r (Н) · 3 =
А r (Р) +
M r (РН 3 ) =
M r (N 2 ) =
14 · 2 = 28
M r ( Al ( ОН ) 3 ) =
27 + 48 + 3 =
78
+ 1 · 3 =
+16 · 3
27
M r ( Н 2 CО 3 ) =
1 · 2 +
12 +
62
16 · 3 =

Вычислите относительные молекулярные массы для В1 (А-Д)
M r (NН 3 ) =
14 + 1 · 3 = 17
M r (SiS 2 ) =
28 + 32 · 2 = 28 + 64 = 92
M r (CaSО 4 ) =
40 + 32 + 16 · 4 = 136
M r (К 2 SО 4 ) =
39 · 2 + 32 + 16 · 4 = 174
M r (Fe 2 (SО 3 ) 3 =
56 · 2 + 32 · 3 + 16 · 9 = = 112 + 96 + 144 = 352

Какую информацию несет формула вещества?
1. Название вещества
Н 2 SO 4
1) Серная кислота
2) Качественный состав: атомы каких элементов входят в состав молекулы (простое или сложное вещество)
2) Состоит из атомов 3 хим. элементов Н, S, О; сложное в-во.
3) Количественный состав: сколько атомов каждого элемента
3) Состоит из 2 атомов Н, 1 атома S, 3 атомов О; сложное вещество.

4) Относительная молекулярная масса
M r (Н 2 SO 4 )
= 1 · 2 + 32 + 16 · 4 =
98
= 2 + 32+ 64 =
5) Массовые отношения химических элементов в сложном веществе
m(Н) : m(S) : m(О) =
1· 2 :
32
: 16· 4 =
= 2 : 32 : 64 =
1 : 16 : 32
6) Массовые доли ( w «омега») химических элементов в сложном веществе
1 · 2
16· 4
w (О)=
w (Н) =
= 0,65
= 0,02 (2%)
98
98
(65%)

6. Вычисление массовой доли ( w «омега») элемента по химической формуле
S
32
n · A r (Э)
w (Э) =
1
M r
1
Пример: рассчитайте массовые доли элементов в Н 2 S
M r (Н 2 S)
= 34
= 1 · 2
= 2 + 32
+ 32
1 · 2
w (Н) =
6%
w% (Н) =
= 0,06
= 0,05 8
34
32
w (S) =
= 0,94 1
w% (S) = 94%
34
6% +94% = 100%
Проверка:

КMnO 4
Выполните упр. 5 стр. 49
1) Качественный состав: атомы каких элементов входят в состав молекулы (простое или сложное вещество)
1) Состоит из атомов 3 хим. элементов К, Mn, О;
сложное в-во.
2) Количественный состав: сколько атомов
каждого элемента, массовые соотношения
элементов, отн. молекулярную массу
2) Состоит из 1 атомов К, 1 атома Mn, 4 атомов О;
M r (КМnО 4 ) =
39 + 55 + 16 ∙ 4 = 158
39 : 55 : ( 4 ∙ 16) =
m(К) : m( Мn) : m( 4 О) =
= 39 : 55 : 64

Вычисление массовой доли w «омега» элемента по химической формуле

6. Вычисление массовой доли ( w «омега») элемента по химической формуле
S
32
n · A r (Э)
w (Э) =
1
M r
1
Пример: рассчитайте массовые доли элементов в Н 2 S
M r (Н 2 S)
= 34
= 1 · 2
= 2 + 32
+ 32
1 · 2
w (Н) =
6%
w% (Н) =
= 0,06
= 0,05 8
34
32
w (S) =
= 0,94 1
w% (S) = 94%
34
6% +94% = 100%
Проверка:

Вычисление массовой доли ( w) элемента в веществе по химической формуле
n · A r (Э)
Массовая доля – w «омега»
w (Э) =
M r
n – число атомов в молекуле (индекс)
Пример: рассчитайте массовые доли элементов кальция, кислорода и углерода в СаСО 3
= 40 + 12 + 16 · 3 =
40 + 12 + 48 = 100
M r (СаСО 3 )
A r (Са) · 1
40 · 1
= 0, 4
(0,4 · 100% = 40%)
w (Са) =
=
100
M r (CaСO 3 )
A r (О) · 3
16 · 3
= 0,48 (48%)
=
w (О) =
100
M r (CaСO 3 )
12
= 0,12 (12%)
=100%
48% +
12%
40% +
w (С) =
100
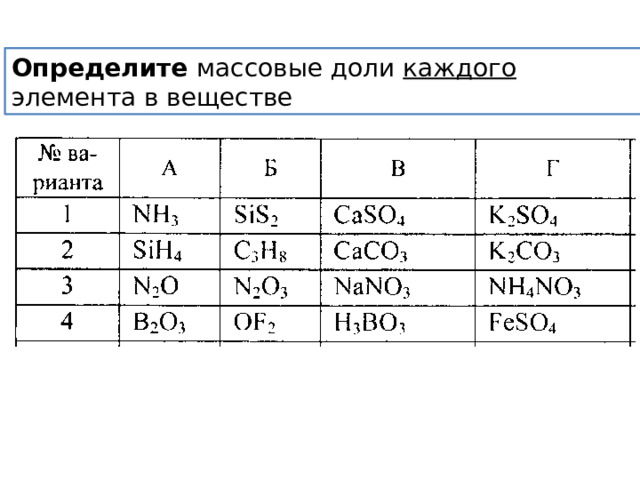
Определите массовые доли каждого элемента в веществе

































