
Цель:
- Познакомить с классификацией, химическими свойствами,
Распространением в природе и биологической ролью углеводов: моно-,
ди-, полисахаридов.
Все углеводы подразделяются на 2 группы
Углеводы
простые углеводы сложные углеводы
(моносахариды, моноза) (полисахариды, полиозы)
альдозы кетозы низкомолекулярные высокомолекулярные
несахароподобные сахароподобные

Простыми углеводами (моносахаридами, монозами) называются
Такие углеводы, которые не способны гидролизоваться с
образованием более простых углеводов. Общая формула С mH2nOn .
Если моносахарид содержит альдегидную группу, то его называют
альдозой, если кетонную-кетозой. Сложными углеводами
(полисахаридами, или полиозами) называются такие углеводы,
которые способны гидролизоваться с образованием простых
углеводов. Общая формула С mH2nOn .
Олигосахариды при гидролизе рпспадаются на 2-8 молекулы
моносахаридов. Высокомолекулярные полисахариды при гидролизе
распадаются на очень большое число моносахаридов. В их составе
может содержаться до нескольких десятков тысяч моносахаридов.
Полисахариды, построенные из остатков одного и того же
простого сахара, называются гомополисахаридами.
Гетерополисахариды построены из остатков разных моносахаридов.

C n H 2 n O n Моносахариды (монозы)
Важнейшие и типичные представители моноз-глюкоза (виноградный сахар) и
фруктоза (фруктовый сахар). Они изомерны друг к другу и имеют молекулярную формулу C 6 H 12 O 6 .
Структурная формула:
О СН 2 – ОН
С
Н
Н С ОН Н С ОН
ОН С Н ОН С Н
Н С ОН Н С ОН
Н С ОН Н С ОН
СН 2 ОН СН 2 ОН
глюкоза фруктоза
альдегексоза кетогексоза
альдоза кетоза
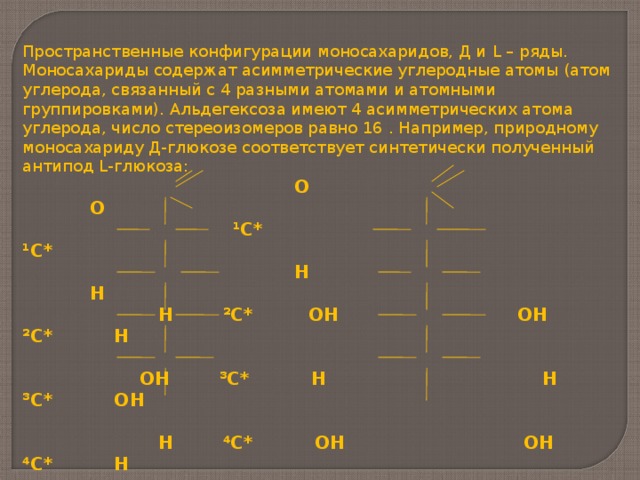
Пространственные конфигурации моносахаридов, Д и L – ряды. Моносахариды содержат асимметрические углеродные атомы (атом углерода, связанный с 4 разными атомами и атомными группировками). Альдегексоза имеют 4 асимметрических атома углерода, число стереоизомеров равно 16 . Например, природному моносахариду Д-глюкозе соответствует синтетически полученный антипод L -глюкоза:
О О
¹С* ¹С*
Н Н
Н ²С* ОН ОН ²С* Н
ОН ³С* Н Н ³С* ОН
Н ⁴С* ОН ОН ⁴С* Н
Н ⁵С* ОН ОН ⁵С* Н
⁶ СН 2 ОН ⁶СН 2 ОН
Д-глюкоза L -глюкоза
(антиподы)
Нумерацию цепи принято вести, начиная от альдегидной группы в альдозах, а в кетозах – начиная от того конца, к которому ближе кетогруппа.
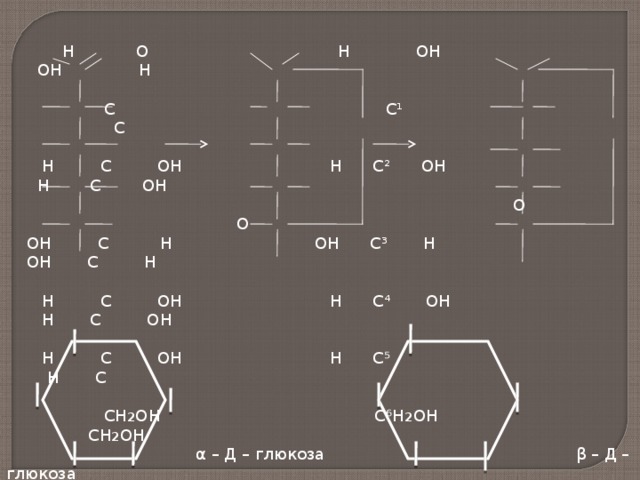
Н О Н ОН ОН Н
С С¹ С
Н С ОН Н С² ОН Н С ОН
О О
ОН С Н ОН С³ Н ОН С Н
Н С ОН Н С⁴ ОН Н С ОН
Н С ОН Н С⁵ Н С
СН 2 ОН С⁶Н 2 ОН СН 2 ОН
α – Д – глюкоза β – Д – глюкоза
⁶
СН 2 ОН СН 2 ОН
О О
СН ⁵ Н
Н Н Н ОН
ОН ОН- R ОН ⁴ ¹ Н
ОН Н ОН Н
³ ²
Н ОН Н ОН
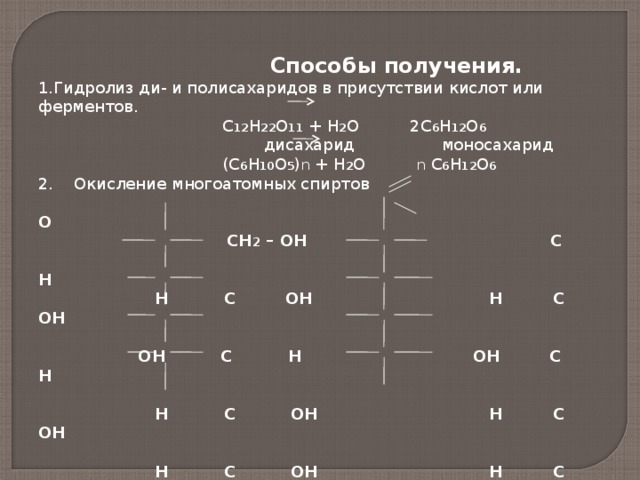
Способы получения.
- Гидролиз ди- и полисахаридов в присутствии кислот или ферментов.
С 12 Н 22 О 11 + Н 2 О 2С 6 Н 12 О 6
дисахарид моносахарид
(С 6 Н 10 О 5 ) n + Н 2 О n С 6 Н 12 О 6
2. Окисление многоатомных спиртов
О
СН 2 – ОН С
Н
Н С ОН Н С ОН
ОН С Н ОН С Н
Н С ОН Н С ОН
Н С ОН Н С ОН
СН 2 ОН СН 2 ОН
Д-сорбит Д-глюкоза
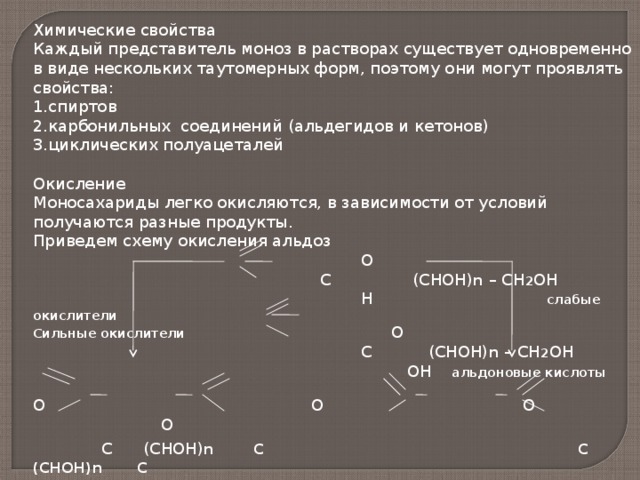
Химические свойства
Каждый представитель моноз в растворах существует одновременно в виде нескольких таутомерных форм, поэтому они могут проявлять свойства:
- спиртов
- карбонильных соединений (альдегидов и кетонов)
- циклических полуацеталей
Окисление
Моносахариды легко окисляются, в зависимости от условий получаются разные продукты.
Приведем схему окисления альдоз
О
С (СНОН) n – СН 2 ОН
Н слабые окислители
Сильные окислители О
С (СНОН) n – СН 2 ОН
ОН альдоновые кислоты
О О О О
С (СНОН) n С С (СНОН) n С
ОН ОН Н ОН
сахарные кислоты уроновые кислоты
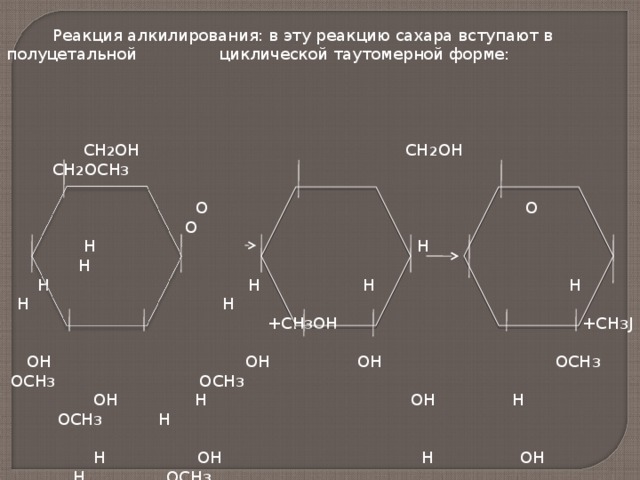
Реакция алкилирования: в эту реакцию сахара вступают в полуцетальной циклической таутомерной форме:
СН 2 ОН СН 2 ОН СН 2 ОСН 3
О О О
Н Н Н
Н Н Н Н Н Н
+СН 3 ОН +СН 3 J
ОН ОН ОН ОСН 3 ОСН 3 ОСН 3
ОН Н ОН Н ОСН 3 Н
Н ОН Н ОН Н ОСН 3
пентаметил- метилглюкозид глюкоза
α –
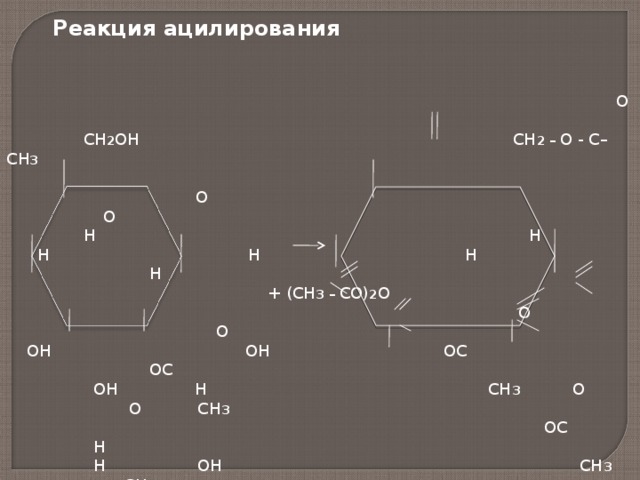
Реакция ацилирования
О
СН 2 ОН СН 2 – О - С– СН 3
О О
Н Н
Н Н Н Н
+ (СН 3 – СО) 2 О
О О
ОН ОН ОС ОС
ОН Н СН 3 О О СН 3
ОС Н
Н ОН СН 3 СН 3
Н ОС
Пентаацетилглюкоза
![Брожение сахаров А) спиртовое С 6 Н 12 О зимаза С 2 Н 5 ОН + 2СО 2 Б) маслянокислое О С 6 Н 12 О СН3 СН 2 СН 2 С + 2СО 2 + 2Н 2 О Н О В) С 6 Н 12 О 2СН 3 СН С Н ОН молочная кислота Г) лимонное брожение О ОН О [о] С6Н12О С – СН2 – С – СН2 – С + 2Н2О О ОН С ОН Н](https://static.multiurok.ru/multiurok/html/2018/06/11/s_5b1ed526f1306/img10.jpg)
Брожение сахаров
А) спиртовое
С 6 Н 12 О зимаза С 2 Н 5 ОН + 2СО 2
Б) маслянокислое О
С 6 Н 12 О СН3 СН 2 СН 2 С + 2СО 2 + 2Н 2 О
Н
О
В) С 6 Н 12 О 2СН 3 СН С
Н
ОН
молочная кислота
Г) лимонное брожение
О ОН О
[о]
С6Н12О С – СН2 – С – СН2 – С + 2Н2О
О
ОН С ОН
Н
![Реакция серебреного зеркала О О С С Н ОН Н С ОН Н С ОН ОН С Н [О] ОН С Н Н С ОН Н С ОН Н С ОН Н С ОН СН 2 ОН СН 2 ОН глюкоза глюконовая кислота](https://static.multiurok.ru/multiurok/html/2018/06/11/s_5b1ed526f1306/img11.jpg)
Реакция серебреного зеркала
О О
С С
Н ОН
Н С ОН Н С ОН
ОН С Н [О] ОН С Н
Н С ОН Н С ОН
Н С ОН Н С ОН
СН 2 ОН СН 2 ОН
глюкоза глюконовая кислота

Биологическая роль углеводов
Среди углеводов есть вещества низкомолекулярные, кристаллические и аморфные, растворимые и нерастворимые в воде, способные легко окисляться и устойчивые к действию окислителей, гидролизуемые и негидролизуемые и т. д., что обуславливает разнообразие их биологических функций в живых организмах. При окислении углеводов выделяется энергия, используемая в биохимических реакциях. Промежуточные продукты процессов окисления служат исходными веществами для синтеза многих других образований, выполняющих в организме опорные, защитные и иные функции.
Так, триозы играют роль промежуточных продуктов в процессах дыхания, фотосинтеза и других процессах углеводного обмена.

Углеводы выполняют и защитные функции в организме. Например, гепарин ингибирует процесс свертывания крови (содержится в крови и соединительной ткани млекопитающих). Камеди (вязкие гели или клейкие растворы) и слизи (более жидкие гели или слизистые массы) представляют собой смеси сахаров и сахарных кислот. Они образуются в ответ на повреждение, а также способствуют удержанию влаги в растениях, тем самым повышая их засухоустойчивость. Слизи
и камеди используют как смягчающее и обволакивающее лечебное средство, для защиты слизистой оболочки ротовой полости, желудочно-кишечного тракта, бронхов. В этих целях можно использовать льняное семя, корень алтея, листья подорожника, цветки липы и др.

Углеводы и правильное питание
Подсчитано, что во время голода организм человека расходует 100 единиц энергии, при питании углеводами – 106,4, жирами – 114,5, белками – 140. Следовательно, самый экономичный источник питания – углеводы, а наименее выгодный – белки.
















![Брожение сахаров А) спиртовое С 6 Н 12 О зимаза С 2 Н 5 ОН + 2СО 2 Б) маслянокислое О С 6 Н 12 О СН3 СН 2 СН 2 С + 2СО 2 + 2Н 2 О Н О В) С 6 Н 12 О 2СН 3 СН С Н ОН молочная кислота Г) лимонное брожение О ОН О [о] С6Н12О С – СН2 – С – СН2 – С + 2Н2О О ОН С ОН Н](https://static.multiurok.ru/multiurok/html/2018/06/11/s_5b1ed526f1306/img10.jpg)
![Реакция серебреного зеркала О О С С Н ОН Н С ОН Н С ОН ОН С Н [О] ОН С Н Н С ОН Н С ОН Н С ОН Н С ОН СН 2 ОН СН 2 ОН глюкоза глюконовая кислота](https://static.multiurok.ru/multiurok/html/2018/06/11/s_5b1ed526f1306/img11.jpg)













