
АМИНОКИСЛОТЫ
10 класс
5klass.net

- Определение класса
- Классификация
- Изомерия
- Свойства
- Получение
- Применение
План характеристики:

- Органические соединения, в молекулах которых содержатся карбоксильная группа СООН и аминогруппа NH 2 , связанные углеводородным радикалом R

- Аминокислоты – производные карбоновых кислот, которые можно рассматривать как продукты замещения одного или более атомов водорода в их радикалах на одну или более аминогрупп

Аминокислоты – гетерофункциональные(бифункциональные) соединения, которые обязательно содержат две функциональные группы: аминогруппу – NH2 и карбоксильную группу – COOH , связанные с углеводородным радикалом
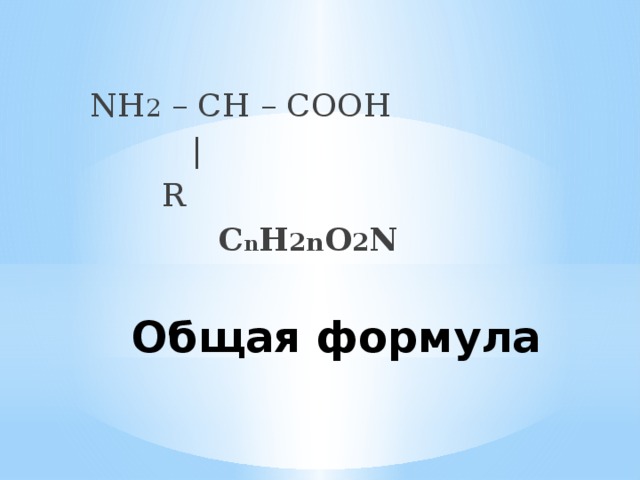
NH 2 – CH – COOH
|
R
С n H 2n O 2 N
Общая формула

- По взаимному расположению функциональных групп:
α
С – С- С – С – СООН
| β α
NH2 С – С- С – С – СООН
| NH2
γ β α
С – С- С – С – СООН
|
NH2
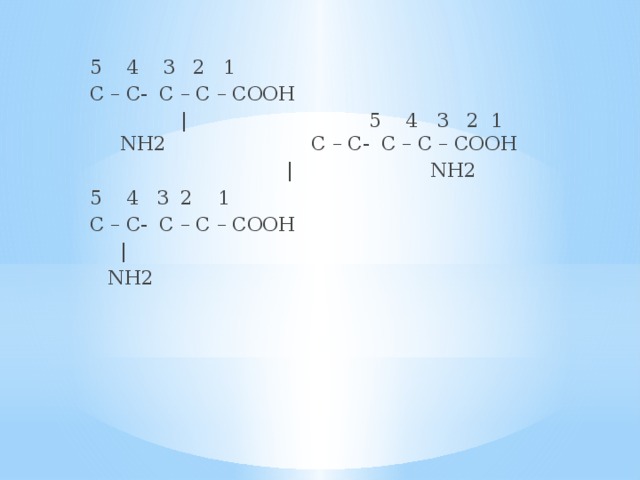
5 4 3 2 1
С – С- С – С – СООН
| 5 4 3 2 1 NH2 С – С- С – С – СООН
| NH2
5 4 3 2 1
С – С- С – С – СООН
|
NH2

- По количеству функциональных групп :
-моноаминомонокарбоновые
-диаминомонокарбоновые
С-С-С-С-С –СООН
׀ ׀
NH2 NH2
лизин

- изомерия углеродного скелета
- изомерия положения NH 2
- оптическая изомерия:
изомерия

Аминокислоты
Природные Синтетические
(в живых организмах) (синтезированы)
протеиногенные
всего около 20 незаменимые
(около половины из)
поступают с пищей
не синтезируются в организме
 200 0 , растворимы, сладкие, горькие, безвкусные (от состава радикала) Физические свойства: " width="640"
200 0 , растворимы, сладкие, горькие, безвкусные (от состава радикала) Физические свойства: " width="640"
- Б/ц кристаллические вещества, температура плавления 200 0 , растворимы, сладкие, горькие, безвкусные (от состава радикала)
Физические свойства:

- Аминокислоты – амфотерые соедиения
1) Как кислоты
а) с основаниями
NH 2 -CH- COOH + NaOH → NH 2 -CH- COONa + H 2 O
| |
R R
натриевая соль
аминокислоты

б) со спиртами
NH 2 -CH- COOH +С 2 Н 5 ОН → NH 2 -CH- COOС 2 Н 5 + H 2 O
| |
R R
этиловый эфир
аминокислоты
![2) Как основания а) с кислотами NH 2 – CH – COOH +HCl → [ NH 3 – CH – COOH] + Сl - | | R R хлороводородная соль аминокислоты](https://fsd.multiurok.ru/html/2017/02/21/s_58abea11b7b6a/img14.jpg)
2) Как основания
а) с кислотами
NH 2 – CH – COOH +HCl → [ NH 3 – CH – COOH] + Сl -
| |
R R
хлороводородная соль
аминокислоты
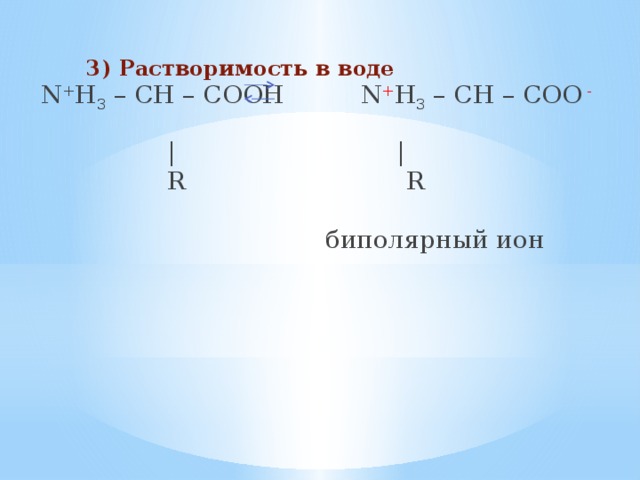
3) Растворимость в воде
N + H 3 – CH – COOH N + H 3 – CH – COO -
| |
R R
биполярный ион

NH 2 –CH 2 –COOH + NH 2 –CH 2 –COOH
→ NH 2 –CH 2 – CO-NH –CH 2 –COOH+Н 2 О
пептидная связь
полипептид
4) Специфическое - взаимодействие между собой (Реакция поликонденсации)
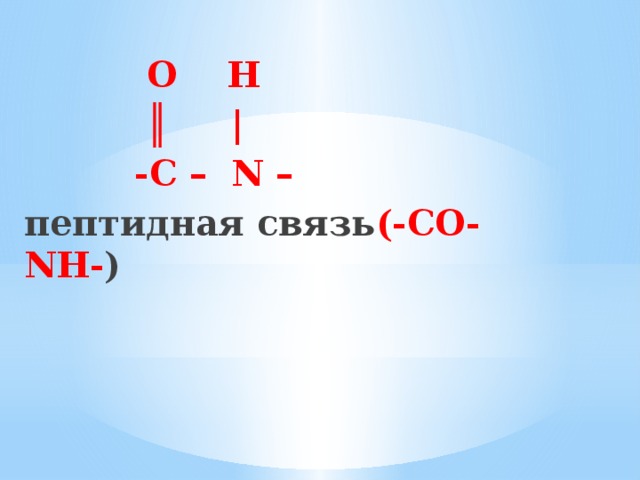
O H
║ |
-C – N –
пептидная связь (-СО-NH- )

Аминокислота1+ Аминокислота2=дипепидид
Аминокислота1+Аминокислота2+Аминокислота3=трипептид…
- Вывод: α-аминокислоты – элементарные частицы природных полимеров- белков
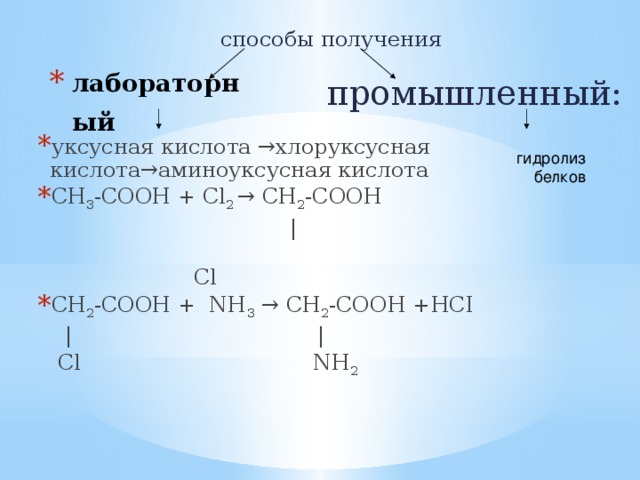
способы получения
промышленный:
- уксусная кислота →хлоруксусная кислота→аминоуксусная кислота
- СН 3 -СООН + Сl 2 → СН 2 -СООН
|
Cl
- СН 2 -СООН + NH 3 → СН 2 -СООН +HCI
| |
Сl NH 2
гидролиз белков

1806г. Луи Воклен и Пьер Робике
Сок спаржи выделили белое кристаллическое вещество – аспарагин (первая аминокислота, выделенная химиками из природных объектов)
1848г. Рафаэль Пириа
Гидролиз аспарагина аспарагиновая кислота
НО-С-СН 2 -СН-СООН
║ |
О NH 2

- В живых организмах:
- Природные аминокислоты (около 150)
- Протеиногенные аминокислоты (около 20) в белках
валин, лейцин, лизин, треонин, цистеин и др.
- Антибиотики (пенициллин)
- Полиамидные смолы (капрон, нейлон)
- *Добавка к корму

1909г. К. Икеда
Сушеные водоросли – усиливают аромат и вкус пищи – пищевые добавки.
Е 621, Е 620, Е 622-625
Назвать кислоту, записать уравнения реакций взаимодействия данной аминокислоты с кислотой, основанием, спиртом
СН 3 – СН - СООН
|
NH 2
NH 2 – С 2 Н 4 - СООН
(аланин)

- Жизнь – это форма существования белковых тел
- Белок – это мышцы, соединительные ткани (сухожилия, связки, хрящи).
- Белковые молекулы включены в состав костной ткани.
- Из особых форм белка сотканы волосы, ногти, зубы, кожный покров.
- Из белковых молекул образуются отдельные очень важные гормоны, от которых зависит здоровье.
- Большинство ферментов также включают белковые фрагменты, а от ферментов зависит качество и интенсивность происходящих в организме физиологических и биохимических процессов.
- Содержание белков в различных тканях человека неодинаково. Так, мышцы содержат до 80% белка, селезенка, кровь, легкие – 72%, кожа – 63%, печень – 57%, мозг – 15%, жировая ткань, костная и ткань зубов – 14–28%.

Белки – это высокомолекулярные органические соединения,представляющиесобой биополимер, состоящий из мономе ров,которыми являются аминокислоты соединенные пептидной связью

В состав белков входят:
Гемоглобин - С 3032 H 4816 O 872 N 780 S 8 Fe 4
Mr белка яйца = 36 000,
Mr белка мышц = 1 500 000.
водород
углерод
азот
кислород
фосфор
сера
железо
другие элементы

Основными структурными компонентами белков являются аминокислоты .

- В начале 20 века Э.Фишер в результате гидролиза белковых
- молекул получил смесь аминокислот и выдвинул
- полипептидную теорию.
- H 2 N – CH – COОН + Н – N – CH - COOH →
- │ │ │
- CH 3 H CH 3
- аланин аланин
- H 2 N – CH – C – N – CH – COOH + Н2О
│ ║ | │
CH 3 О Н CH 3 дипептид

- БЕЛКИ - это высокомолекулярные азотсодержащие органические вещества, структурным компонентом которых являются α-аминокислоты, связанные пептидными связями.
- В состав белков входит 20 различных аминокислот.
- Кроме понятия «белок», в химии встречается термины « ПЕПТИД » и « ПОЛИПЕПТИД ».
- Белки подразделяют на протеины (простые белки) и протеиды (сложные белки).
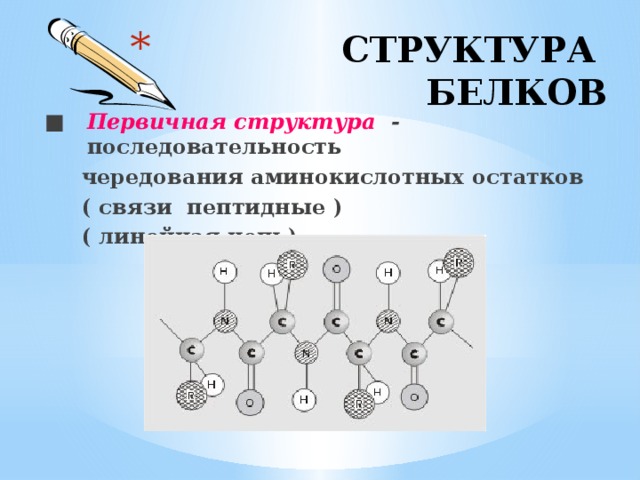
■ Первичная структура - последовательность
чередования аминокислотных остатков
( связи пептидные )
( линейная цепь)
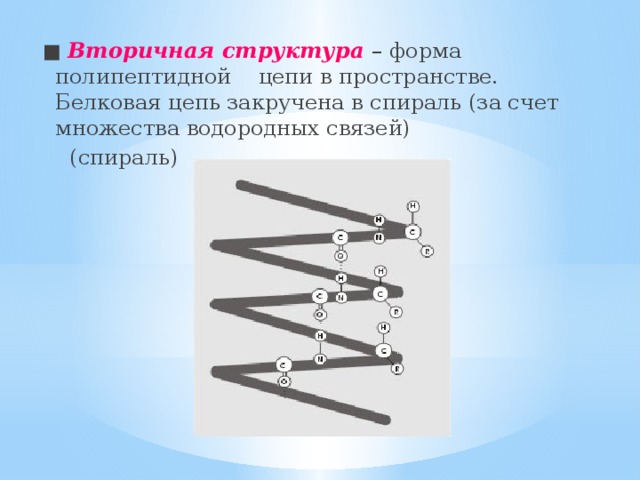
■ Вторичная структура – форма полипептидной цепи в пространстве. Белковая цепь закручена в спираль (за счет множества водородных связей)
(спираль)

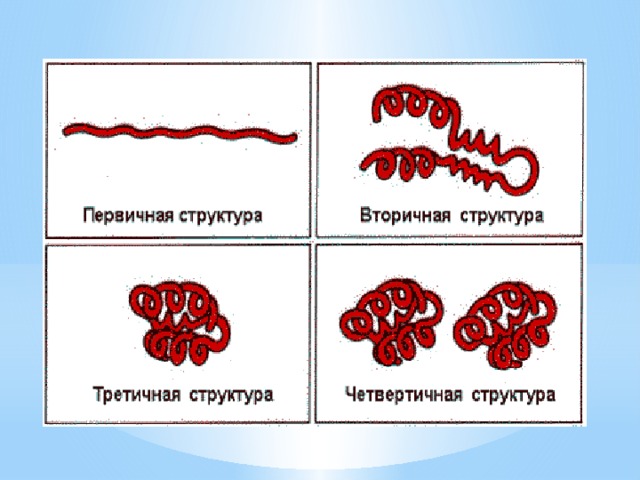
- Третичная структура – реальная трехмерная конфигурация, которую принимает в пространстве закрученная спираль (за счет гидрофобных связей), у некоторых белков – S–S-связи (бисульфидные связи)
(клубок)

- Четвертичная структура – соединенные друг с другом макромолекулы белков образуют комплекс.
(Несколько цепей)

► Строительная – белки участвуют в образовании оболочки клетки, органоидов и мембран клетки. Из белков построены кровеносные сосуды, сухожилия, волосы
► Каталитическая – все клеточные катализаторы –
белки (активные центры фермента).
► Двигательная – сократительные белки вызывают
всякое движение.
► Транспортная – белок крови гемоглобин присоединяет кислород и разносит его по всем тканям.
► Защитная – выработка белковых тел и антител для обезвреживания чужеродных веществ.
► Энергетическая – 1 г белка эквивалентен 17,6 кДж.
► Рецепторная – реакция на внешний раздражитель.
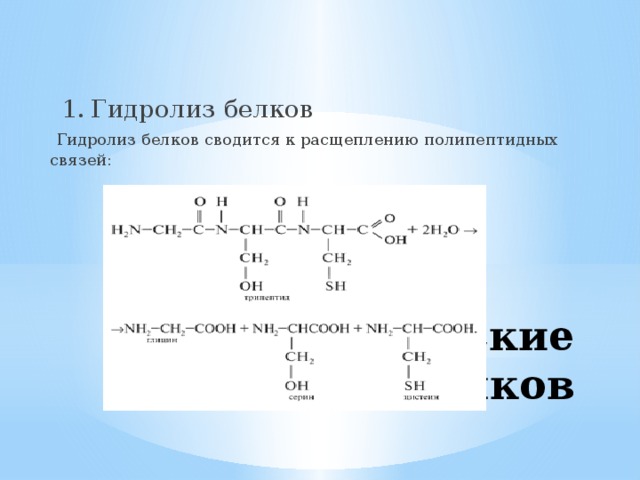
1. Гидролиз белков
Гидролиз белков сводится к расщеплению полипептидных связей:
- Химические свойства белков

2. Денатурация белков
Денатурация – нарушение природной структуры белка под действием нагревания и химических реагентов.
а) высокая или низкая температура
б) механическое воздействие;
в) облучение;
г) яды;
д) действие спирта;
б) действие солей тяжелых металлов (Pb, Hg и др.)

3. Цветные качественные реакции белков
а) Биуретовая реакция (Cu(OH) 2 );
б) ксантопротеиновая реакция (HNO 3 конц.);
в) взаимодействие белка с ацетатом свинца
при нагревании.
г) горение белка

- Превращения белков в организме

- Отдельные белки находят применение в народном хозяйстве, например белки шерсти, шелка, кожи и рогов животных.
- Выяснение структуры белков, их многообразных функций в организме позволяет понять механизм наследственности, что в свою очередь, имеет большое значение для выведения высокопродуктивных пород животных и сортов растений.
- Изучение белков важно и для выяснения природы заболеваний, наблюдаемых у человека и животных

- Какие атомы входят в состав белков?
- Какой ученый и как объяснил строение белков?
- Определение белков.
- Как подразделяются белки?
- Какие структуры может иметь белок,как можно охарактеризовать каждую структуру, тип связи в каждой структуре.
- Функции белков.
- Химические свойства белков
- Значение белков.
















 200 0 , растворимы, сладкие, горькие, безвкусные (от состава радикала) Физические свойства: " width="640"
200 0 , растворимы, сладкие, горькие, безвкусные (от состава радикала) Физические свойства: " width="640"


![2) Как основания а) с кислотами NH 2 – CH – COOH +HCl → [ NH 3 – CH – COOH] + Сl - | | R R хлороводородная соль аминокислоты](https://fsd.multiurok.ru/html/2017/02/21/s_58abea11b7b6a/img14.jpg)











































