Просмотр содержимого документа
«презентация Ионная связь»

ГОКУ АО «Общеобразовательная школа при учреждениях исполнения наказания» ФКУ ИК-8
ИОННАЯ СВЯЗЬ
Выполнила учитель химии и биологии
I квалификационной категории И. А. Трухина
г. Благовещенск

Химическая связь - это взаимное сцепление атомов в молекуле и кристаллической решётке в результате действия между атомами электрических сил притяжения

Ионная связь – это химическая связь, которая осуществляется за счет электростатического взаимодействия противоположно заряженных ионов – катионов и анионов Ион – это частица, образующаяся в результате отдачи или принятия электрона
Эл 0 – n е - = Эл n+
Эл 0 + n е - = Эл n-
-
-
-
-
+ 11
+17
-
-
-
-
ион-катион
ион-анион

Когда внешние электронные слои полностью заполнены, общая энергия атомов понижается. Например, атом натрия, имеющий на внешнем слое один электрон, охотно отдает этот электрон. И наоборот, атом хлора, которому не хватает одного электрона для заполнения внешнего слоя, стремится присоединить электрон для завершения уровня. Когда атомы натрия и хлора оказываются рядом, натрий отдает электрон, а хлор его принимает. При этом атом натрия, потеряв отрицательный заряд, становится положительно заряженным ионом натрия, а атом хлора, получив дополнительный электрон, становится отрицательно заряженным ионом хлора. По закону Кулона между двумя ионами возникает электростатическое притяжение, приводящее к образованию химической связи, которая и удерживает атомы вместе. С этой реакцией связано одно из чудес химии: бурно реагирующее вещество натрий и сильно ядовитый газ хлор, соединяясь, образуют обычную поваренную соль, широко применяемую в питании.
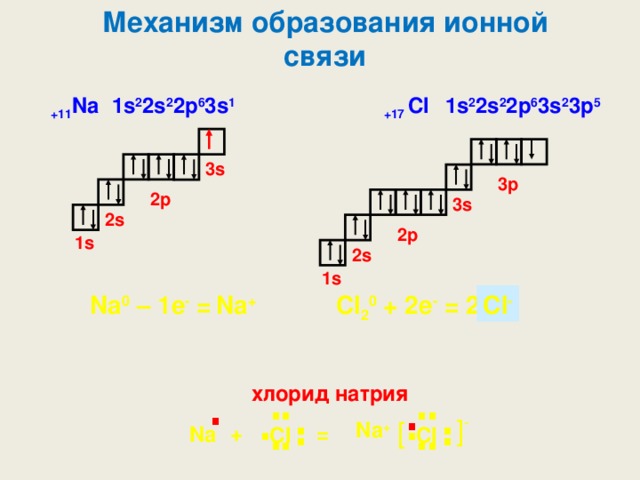
Механизм образования ионной связи
- [
+17 Cl
+11 Na
1s 2 2s 2 2p 6 3s 2 3p 5
1s 2 2s 2 2p 6 3s 1
3s
3p
2p
3s
2s
2p
1s
2s
1s
Cl 2 0 + 2e - = 2
Na +
Cl -
Na 0 – 1e - =
хлорид натрия
.
.
.
.
.
.
.
.
.
.
.
.
[
.
.
.
.
Na +
=
+
Na
Cl
Cl
 1,7 – ионная химическая связь; Например, NaCl א (Na) = 1,01; א (Cl) = 2,83; Δ א = 2,83 – 1,01 = 1,82 , т.е. ионная химическая связь IA IIA H Li 2,10 IIIA IVA 0,97 Be Na 1,47 Mg K 1,01 B VA 0,91 Ca 1,23 2,01 VIA C Al Rb 1,04 2,50 Cs N VIIA Si 0,89 Sr Ga 1,47 Ge 1,82 0,99 Ba O 0,86 3,07 2,25 In P 3,50 0,97 2,02 Tl As 2,32 S 1,49 Sn F 2,10 Se 1,44 4,10 2,60 1,72 Pb Cl Sb 2,48 1,55 Te 1,82 Br Bi 2,83 Po 1,67 2,01 2,74 I 1,76 2,21 At 1,90 " width="640"
1,7 – ионная химическая связь; Например, NaCl א (Na) = 1,01; א (Cl) = 2,83; Δ א = 2,83 – 1,01 = 1,82 , т.е. ионная химическая связь IA IIA H Li 2,10 IIIA IVA 0,97 Be Na 1,47 Mg K 1,01 B VA 0,91 Ca 1,23 2,01 VIA C Al Rb 1,04 2,50 Cs N VIIA Si 0,89 Sr Ga 1,47 Ge 1,82 0,99 Ba O 0,86 3,07 2,25 In P 3,50 0,97 2,02 Tl As 2,32 S 1,49 Sn F 2,10 Se 1,44 4,10 2,60 1,72 Pb Cl Sb 2,48 1,55 Te 1,82 Br Bi 2,83 Po 1,67 2,01 2,74 I 1,76 2,21 At 1,90 " width="640"
Ионная связь образуется между атомами металлов и неметаллов, то есть между атомами с очень сильно отличающейся электроотрицательностью. Электроотрицательность - способность атомов одних химических элементов притягивать электроны в соединениях от атомов других химических элементов
Δ א – разница электроотрицательностей:
Δ א 1,7 – ионная химическая связь;
Например, NaCl
א (Na) = 1,01;
א (Cl) = 2,83;
Δ א = 2,83 – 1,01 = 1,82 , т.е. ионная химическая связь
IA
IIA
H
Li
2,10
IIIA
IVA
0,97
Be
Na
1,47
Mg
K
1,01
B
VA
0,91
Ca
1,23
2,01
VIA
C
Al
Rb
1,04
2,50
Cs
N
VIIA
Si
0,89
Sr
Ga
1,47
Ge
1,82
0,99
Ba
O
0,86
3,07
2,25
In
P
3,50
0,97
2,02
Tl
As
2,32
S
1,49
Sn
F
2,10
Se
1,44
4,10
2,60
1,72
Pb
Cl
Sb
2,48
1,55
Te
1,82
Br
Bi
2,83
Po
1,67
2,01
2,74
I
1,76
2,21
At
1,90

Ионы
По заряду
По составу
отрицательные:
положительные: Ca 2+ , Na+
OH-, SO42-
простые:
сложные:
Na + , Ca 2+ , Cl -
OH - , SO 4 2- , No 3 -
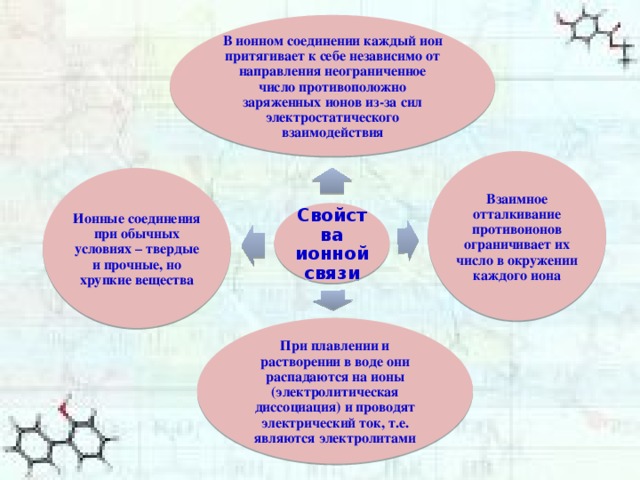
В ионном соединении каждый ион притягивает к себе независимо от направления неограниченное число противоположно заряженных ионов из-за сил электростатического взаимодействия
Взаимное отталкивание противоионов ограничивает их число в окружении каждого иона
Ионные соединения при обычных условиях – твердые и прочные, но хрупкие вещества
Свойства ионной связи
При плавлении и растворении в воде они распадаются на ионы (электролитическая диссоциация) и проводят электрический ток, т.е. являются электролитами












 1,7 – ионная химическая связь; Например, NaCl א (Na) = 1,01; א (Cl) = 2,83; Δ א = 2,83 – 1,01 = 1,82 , т.е. ионная химическая связь IA IIA H Li 2,10 IIIA IVA 0,97 Be Na 1,47 Mg K 1,01 B VA 0,91 Ca 1,23 2,01 VIA C Al Rb 1,04 2,50 Cs N VIIA Si 0,89 Sr Ga 1,47 Ge 1,82 0,99 Ba O 0,86 3,07 2,25 In P 3,50 0,97 2,02 Tl As 2,32 S 1,49 Sn F 2,10 Se 1,44 4,10 2,60 1,72 Pb Cl Sb 2,48 1,55 Te 1,82 Br Bi 2,83 Po 1,67 2,01 2,74 I 1,76 2,21 At 1,90 " width="640"
1,7 – ионная химическая связь; Например, NaCl א (Na) = 1,01; א (Cl) = 2,83; Δ א = 2,83 – 1,01 = 1,82 , т.е. ионная химическая связь IA IIA H Li 2,10 IIIA IVA 0,97 Be Na 1,47 Mg K 1,01 B VA 0,91 Ca 1,23 2,01 VIA C Al Rb 1,04 2,50 Cs N VIIA Si 0,89 Sr Ga 1,47 Ge 1,82 0,99 Ba O 0,86 3,07 2,25 In P 3,50 0,97 2,02 Tl As 2,32 S 1,49 Sn F 2,10 Se 1,44 4,10 2,60 1,72 Pb Cl Sb 2,48 1,55 Te 1,82 Br Bi 2,83 Po 1,67 2,01 2,74 I 1,76 2,21 At 1,90 " width="640"












