

« Просто знать - еще не все, знания необходимо еще использовать»
немецкий естествоиспытатель Гёте

Вещества
Простые
Сложные
Оксиды
Неметаллы
Металлы
?
Основание
Кислоты

ТЕСТ
- Определите ряд формул состоящих
только из:
кислотных оксидов ( I вариант)
основных оксидов: (II вариант)
а) Na 2 O, N 2 O, CuO;
б) CO 2 , P 2 O 5 , Cl 2 O 7 ;
в) MgO, BaO, K 2 O;
г) Li 2 O, CaO, CO.

ТЕСТ
- 2. Выберите из списка веществ формулы: только кислот (I вариант), формулы только оснований (II вариант):
а) НСI, AICI 3 , CO 2 , H 2 SO 4
б) H 2 SO 4 , HCI, HNO 3 , HF
в) NaOH, BaCI 2 , CO, Ca(OH) 2
г) AI(OH) 3 , NaOH, KOH, Ba(OH) 2

ТЕСТ
- 3. Выберите формулу оксида серы (IV) – I вариант
- Выберите формулу оксида углерода (II) –
II вариант:
а)H 2 S б) CO в) HNO 3 г) ZnO д) SO 2

ТЕСТ
4. * Выберите формулу серной кислоты – I вариант
* Выберите формулу сернистой кислоты –II вариант
а) H 2 SiO 3 б) H 2 SO 4 в) H 2 SO 3 г) H 2 S

ТЕСТ
5. * Выберите формулу гидроксида калия –
I вариант
* Выберите формулу гидроксида кальция -
II вариант
а) Ba(OH) 2 , б) NaOH, в) KOH, г)Ca(OH) 2.

ТЕСТ
6. * Выберите формулы растворимых в воде оснований – I вариант
* Выберите формулы нерастворимых в воде оснований – II вариант
а)C u (OH) 2, б) KOH, в) LiOH,
г) AI(OH) 3.

ТЕСТ
7. * Выберите формулы, в которых
лакмус меняет свой цвет
на красный – I вариант
Выберите формулы, в которых
лакмус меняет свой цвет на
синий – II вариант
а) НСI , б) H 2 SO 4, в) NaOH , г) KOH .

Ответы к тесту.
I вариант II вариант
1. б 1. в
2. б 2. г
3. д 3. б
4. б 4. в
5. в 5. г
6. б, в 6. а, г
7. а, б 7. в, г

Критерии оценивая.
- Оценка «5» - одна
- ошибка
- Оценка «4» - две ошибки
- Оценка «3» - три ошибки
- Оценка «2» - четыре ошибки и больше.
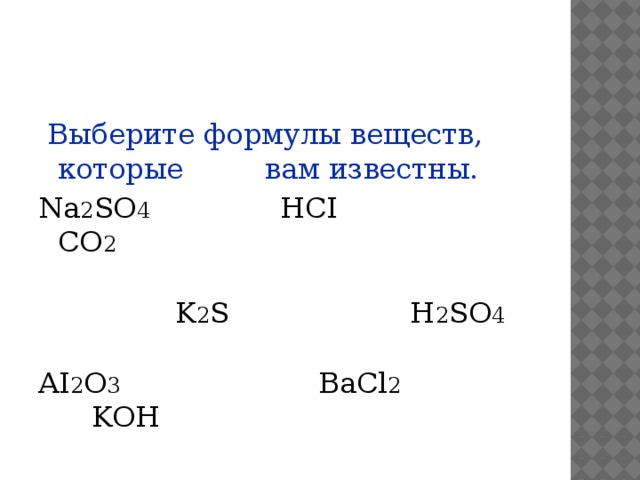
Выберите формулы веществ, которые вам известны.
Na 2 SO 4 HCI CO 2
K 2 S H 2 SO 4
AI 2 O 3 ВаCl 2 KOH

Тема урока : соли как производные кислот и оснований.

- Цель урока : Выяснить почему соли являются производными кислот и оснований?
- Задачи урока: 1 .Дать определение солей.
- 2. Рассмотреть состав и название солей.
- 3. Продолжить обучение определять степени окисления в сложных соединениях.
- 4. Научиться, составлять формулы солей.
- 5. Познакомиться с физическими свойствами солей, их классификацией.
- 6. Значение и применение солей.

СОЛИ
Cоли – это сложные вещества, состоящие из атомов металла и кислотного остатка.

Соли
- Гипс – кристаллогидрат сульфата кальция
- СаSO 4 * 2H 2 O

Соли
- Кристаллогидрат сульфата меди (II)
- СuSO 4 * 5H 2 O
Безводный сульфат меди(II)

Соли
* Кристаллогидрат железа или железный купорос
FeSO 4 * 7H 2 O
* Сульфат магния –горькая английская соль
MgSO 4

КАРБОНАТ КАЛЬЦИЯ

Фосфат кальция
- основа минералов
фосфоритов и апатитов

Соли
С уверенностью можно сказать, что, по крайней мере, одно химическое соединение в довольно чистом виде имеется в каждом доме, в каждой семье. Это – поваренная соль или как ее называют химики – хлорид натрия NaCl.

NaCl

"Среди всех природных минеральных солей, самая главная та, которую мы называем просто “соль” А.Е.Ферсман

За 4 года человек съедает пуд соли
(в год человек с пищей потребляет 3-5,5 кг соли)

Соль в геральдике российских городов
Герб Бахмута
Герб Солигалича
Герб
Сольвычегодска
Герб Усолья-
Сибирского
Герб Дрогобыча
Герб Энгельса

Минералы карбоната кальция находятся в горных породах:

Меловые горы

Соли
- Из мрамора (СаСО 3 ) сделан дворец в Индии
Тадж- Махал

Мрамор – строительный материал
Единственное в России здание, полностью построенное из
нешлифованного мрамора — железнодорожный вокзал в городе Слюдянка Иркутской области

КАРБОНАТ КАЛЬЦИЯ CaCO 3

Моллюски, раки, радиолярии, кораллы – все имеют известковый скелет

Большой Барьерный риф в Австралии

Лабораторная работа
- «Знакомство с образцами солей»

Физминутка

Алгоритм составления формул и названий солей
- 1.Записываем ионы, из которых состоит соединение.
- 2.Определяем заряды ионов.
- 3.Находим наименьшее общее кратное для зарядов ионов.
- 4.Делим наименьшее общее кратное на заряды ионов. Получаем индексы
- 5.Составляем химическую формулу, вписывая индексы.
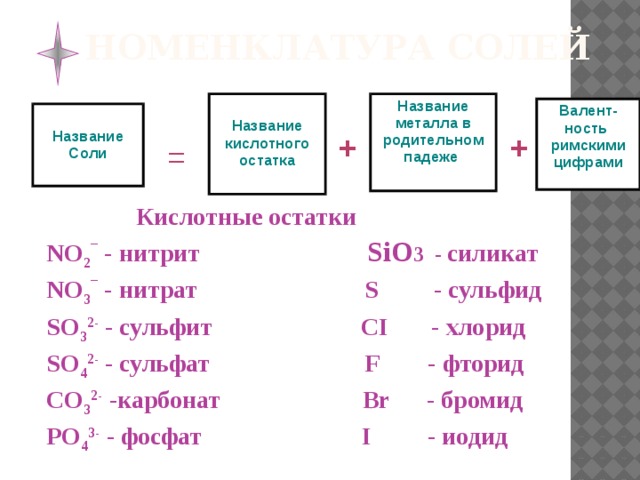
Номенклатура солей
Название металла в родительном падеже
Название кислотного остатка
Валент-ность
римскими цифрами
Название
Соли
+
+
=
Кислотные остатки
NO 2 ¯ - нитрит SiO 3 - силикат
NO 3 ¯ - нитрат S - сульфид
SO 3 2- - сульфит СI - хлорид
SO 4 2- - сульфат F - фторид
СO 3 2- -карбонат Br - бромид
РO 4 3- - фосфат I - иодид
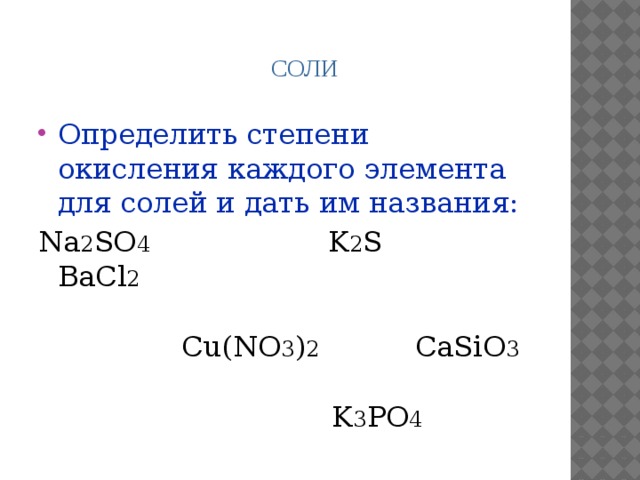
СОЛИ
- Определить степени окисления каждого элемента для солей и дать им названия:
Na 2 SO 4 K 2 S ВаCl 2
Cu(NO 3 ) 2 CaSiO 3
K 3 PO 4

Классификация
Соли
Средние Кислые Основные
Все атомы водорода в молекулах кислоты замещены на атомы металла.
Атомы водорода в кислоте замещены атомами металла частично.
Гидроксогруппы основания (OH) частично замещены кислотными остатками.
Например:
Например:
Например:
Na 2 CO 3 , CuSO 4
KHCO 3 , Ca(HCO 3 ) 2
CaOHCl
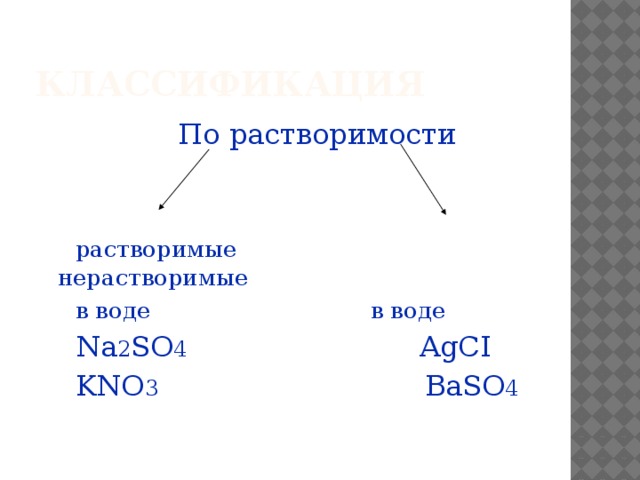
Классификация
По растворимости
растворимые нерастворимые
в воде в воде
Na 2 SO 4 AgCI
KNO 3 BaSO 4

Домашнее задание:
- 1 уровень (для всех ): параграф 21упр.1,2 , выучить название кислотных остатков по таблице на стр. 109, (памятка)
- 2 уровень : Используя дополнительные источники информации, найдите примеры солей имеющих наибольшее применение в сферах жизни и ответьте на вопросы: Почему соли разные на вкус? Какие соли имеют цвет? Какие соли есть в нашем организме?

Рефлексивный экран
- занятия дали мне для жизни…

Релаксация
Хвалилки
Положите правую руку себе на голову, погладьте и скажите: «Ах, какой я молодец!»
А теперь положите руку соседу на голову, погладьте и скажите: «Ах, какой ты молодец!»





























































