
ТЕМА Предельные одноатомные спирты. Алкоголизм и его последствия

С пирты -производные углеводородов, содержащих одну или несколько гидроксильных групп .

Классификация спиртов
По строению
углеводородного
радикала
По числу
гидроксильных
групп
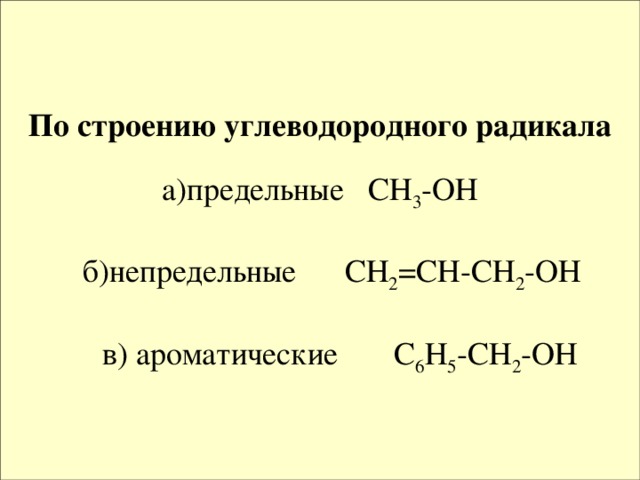
По строению углеводородного радикала
а)предельные СН 3 -ОН
б)непредельные СН 2 =СН-СН 2 -ОН
в) ароматические С 6 Н 5 -СН 2 -ОН

а)одноатомные С 2 Н 5 -ОН
б)двухатомные НО-СН 2 -СН 2 -ОН
в)трехатомные СН 2 -СН-СН 2
ОН ОН ОН
г)многоатомные
По числу гидроксильных групп

Функциональной
называют группу атомов,которая
определяет наиболее характерные
свойства вещества
и его принадлежность
к определенному классу соединений

Общая формула С n Н 2 n +1 ОН (алканолы) С n Н 2 n +2 О R-O б- -H б+ R- Углеводородный радикал СН 3 – метил С 2 Н 5 - этил С 3 Н 7 - пропил С 4 Н 9 - бутил

Номенклатура
1.Выбираем главную цепь,к котрой присоединена -ОН группа
2. Нумеруем цепь с той стороны,к которой ближе группа-ОН
3. Указываем положение и название заместителей (радикалов),число атомов углерода в главной цепи с суффиксом – ан .,после этого идет суффикс – ол ,обозначающий гидроксильную группу и номер атома углерода,у которого эта группа

1.СН 3 – СН 2 – СН 2 – СН 2 – ОН
2. СН 3 –СН– СН – СН 3 ОН СН 3
СН 3 3. СН 3 –– С – СН 2 – ОН СН 3

ВИДЫ
ИЗОМЕРИИ
УГЛЕРОДНОГО
СКЕЛЕТА
ПОЛОЖЕНИЕ
ФУНКЦИОНАЛЬНОЙ
ГРУППЫ
МЕЖКЛАССОВАЯ
ИЗОМЕРИЯ

А)1.СН 3 – СН 2 – СН 2 – СН 2 – ОН
2. СН 2 – СН – СН 3
ОН СН 3
Б)1.СН 3 - СН 2 – СН 2 – О Н
2.СН 3 – СН – СН 3
ОН
В) 1.СН 3 – СН 2 – ОН
2. СН 3 - О – СН 3

Физические свойства
- С 1 – С 3 специфический алкогольный запах,хорошо растворимы в воде
- С 4 – С 5 сладковатый удушливый запах,плохо растворимы
- С 6 – С 11 неприятный запах,с С 8 не растворимы
- С 12 твердые вещества,без запаха.

1.Гомологический ряд предельных одноатомных спиртов не содержит газообразных веществ. 2.С увеличением молекулярной массы(длины углеводородного радикала) растворимость спиртов уменьшается , а температура кипения увеличивается

У спиртов имеется межмолекулярная связь,
которая образуется
за счет взаимодействия
положительно заряженного
атома водорода одной молекулы
и отрицательно заряженного атома
кислорода другой молекулы.
Такая связь называется водородной.


ХИМИЧЕСКИЕ СВОЙСТВА
Взаимодействие
с органическими
кислотами
(реакция этерификации.
Взаимодействие
со щелочными и
щелочно-земельными
металлами
ДЕГИДРАТАЦИЯ
ОКИСЛЕНИЕ

ВЗАИМОДЕЙСТВИЕ СО ЩЕЛОЧНЫМИ И ЩЕЛОЧНО-ЗЕМЕЛЬНЫМИ МЕТАЛЛАМИ
А Л К О Г О Л Я Т Ы
2 C 2 H 5 - O - H + 2 N а 2 C 2 H 5 -O-Na + H 2

Взаимодействие с
органическими кислотами
ЭТЕРИФИКАЦИЯ
СЛОЖНЫЕ ЭФИРЫ
H 2 SO 4 (конц.)
О
О
СН 3 - С
+ Н-О-С 2 Н 5
СН 3 – С
+ Н 2 О
ОС 2 Н 5
ОН

Внутримолекулярная
Алкены
ДЕГИДРАТАЦИЯ
Межмолекулярная
Простые эфиры
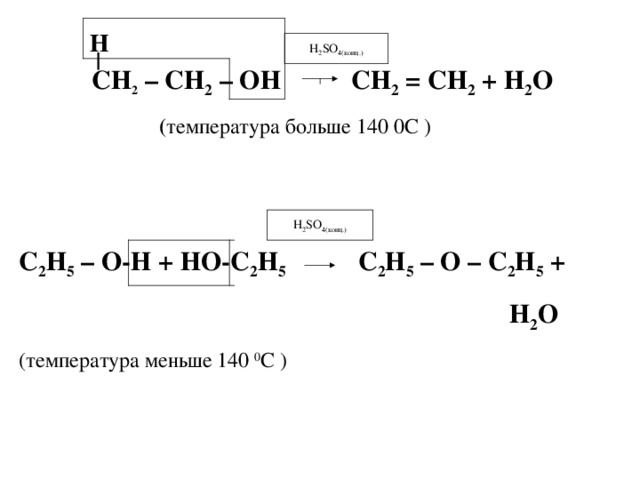
Н
H 2 SO 4 (конц.)
СН 2 – СН 2 – ОН СН 2 = СН 2 + Н 2 О
( температура больше 140 0С )
H 2 SO 4 (конц.)
С 2 Н 5 – О-Н + НО-С 2 Н 5 С 2 Н 5 – О – С 2 Н 5 +
Н 2 О
(температура меньше 140 0 С )

ГОРЕНИЕ
Углекислый газ и вода
ОКИСЛЕНИЕ
Окислительное
дегидрирование
Альдегиды

С 2 Н 5 -ОН + 3О 2 2СО 2 + 3Н 2 О
О
СН 3 -СН –О-Н + С u О СН 3 – С + Н 2 О + Cu
Н
Н

П О Л У Ч Е Н И Е
СПИРТОВОЕ
БРОЖЕНИЕ
ГЛЮКОЗЫ
ГИДРАТАЦИЯ
АЛКЕНОВ
CH 2 =CH 2 +H 2 O C 2 H 5 -OH
C 6 H 12 O 6 2C 2 H 5 - OH +2CO 2

Применяется в производстве лаков и красок





печень
желудок
С 2 Н 5 –О Н
Головной мозг
сердце

Потребление абсолютного спирта на чел. в год




Медицинское обследование 819 детей,родившихся в 215 семьях алкоголиков
- 16-мертворожденные
- 37-родились недоношенными и погибли
- 121- умерли в младенчестве
- 38-родились с физическими нарушениями и были нетрудоспособны
- 145-оказались психически неполноценными
- 55- с ослабленным иммунитетом и заболели туберкулезом или другими инфекционными заболеваниями.
- 174-умерли(21%);238-больные(28%)
Жертвы пристрастия родителей к спиртному
А вы хотите иметь таких детей?
Подумайте,прежде чем браться за рюмку!


























































