Просмотр содержимого документа
«Презентация к уроку "Скорость химических реакций"»

Урок по теме «Скорость химических реакций»
Подготовила: Вихарева О.А.
учитель химии ВКК
МКОУ Березковская ООШ
ИНФОРМАЦИОННЫЙ БЛОК
АНАЛИТИЧЕСКИЙ (ПРАКТИЧЕСКИЙ) БЛОК
ОЦЕНОЧНЫЙ БЛОК
РЕФЛЕКСИВНЫЙ БЛОК
Вихарева О.А.
05.12.2015
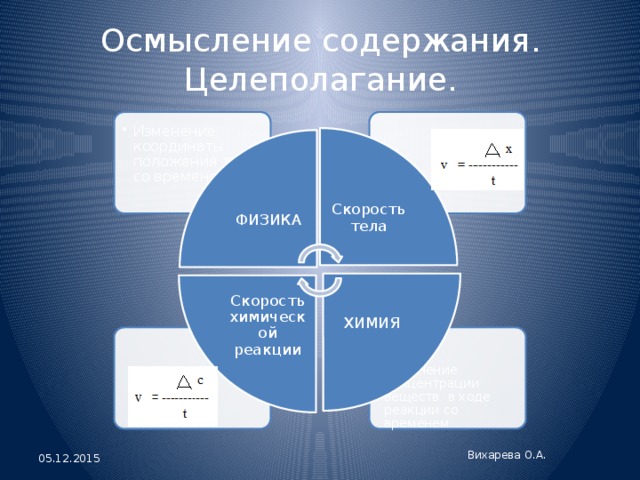
Скорость тела
ХИМИЯ
Скорость химической реакции
Осмысление содержания. Целеполагание.
- Изменение координаты положения тела со временем
- Изменение координаты положения тела со временем
ФИЗИКА
- Изменение концентрации веществ в ходе реакции со временем
- Изменение концентрации веществ в ходе реакции со временем
Вихарева О.А.
05.12.2015

Информационный блок.
Сравнить быстроту протекания реакций ржавления железа и «гашения» пищевой соды уксусом
Предложить количественную характеристику быстроты протекания реакций
Сравнить сущность понятия «скорость» в физике и химии
Вихарева О.А.
05.12.2015

Информационный блок
Проанализировать сущность процессов диффузии веществ в газообразном, жидком и твердом состоянии.
Выдвинуть гипотезу о механизме химического взаимодействия между веществами в различных агрегатных состояниях
Классифицировать реакции из предложенного перечня по характеру взаимодействия реагирующих веществ ( гомогенные и гетерогенные реакции).
05.12.2015
Вихарева О.А.

Изучение зависимости скорости реакций от различных условий
Группа 1.
Группа 2.
Группа 3.
«Природа реагирующих веществ»
«Концентрация»
«Температура»
- Провести опыт по взаимодействию цинка с соляной и уксусной кислотами. Проанализировать результаты. Сделать вывод.
- Провести опыт по взаимодействию цинка с соляной и уксусной кислотами. Проанализировать результаты.
- Сделать вывод.
- Дать объяснение с позиций атомно-молекулярного учения процессам: зависимости скорости реакции от концентрации веществ для гетерогенных и гомогенных реакций Предложить схему процесса
- Дать объяснение с позиций атомно-молекулярного учения процессам:
- зависимости скорости реакции от концентрации веществ для гетерогенных и гомогенных реакций
- Предложить схему процесса
- На основе знаний из курса физики о кинетической и потенциальной энергии объяснить зависимость скорости химических реакций от температуры.
- На основе знаний из курса физики о кинетической и потенциальной энергии объяснить зависимость скорости химических реакций от температуры.
05.12.2015
Вихарева О.А.
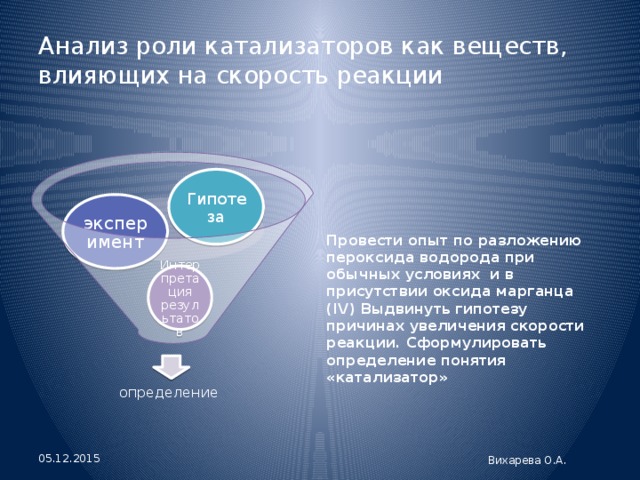
Анализ роли катализаторов как веществ, влияющих на скорость реакции
Провести опыт по разложению пероксида водорода при обычных условиях и в присутствии оксида марганца (IV) Выдвинуть гипотезу причинах увеличения скорости реакции. Сформулировать определение понятия «катализатор»
Гипотеза
эксперимент
Интерпретация результатов
определение
05.12.2015
Вихарева О.А.
Аналитический (практический) блок
Задание.
Возьмите два небольших кусочка мела, один из которых измельчите пестиком в фарфоровой ступке в порошок. В одну пробирку поместите полученный порошок, в другую – кусочек мела целиком. В обе пробирки одновременно добавьте по 2 мл 1%-ной соляной кислоты. Отметьте интенсивность выделения газа в каждом случае.
Провести лабораторный опыт в группе
Составить уравнение реакции в молекулярном и ионном виде
Объяснить, почему скорость выделения газа в этих двух случаях различна
Вихарева О.А.
05.12.2015

Оценочный блок
- Выполнить тест
- 1. При комнатной температуре с наибольшей скоростью протекает реакция между:
- А) Fe и S
- Б) Fe и HCl (раствор)
- В) KBr (раствор) и AgNO3 (раствор)
- Г) CuCO3 и H2
- 2. При комнатной температуре с наименьшей скоростью протекает реакция
- А) Fe и HCl (1%-ый раствор)
- Б) Fe и HCl (10%-ый раствор)
- В) FeCl2 (раствор) и AgNO3(раствор)
- Г) Fe и HCl (30%-ый раствор)
- Ответить на вопрос
- Как изменится скорость химической реакции, температурный коэффициент которой 3, при повышении температуры от 20 С до 40 С?
05.12.2015
Вихарева О.А.

Рефлексивный блок
- Самоанализ
- 1. Выделите формы деятельности, в которых вы принимали участие на уроке.
- 2. Сформулируйте предложение об уроке, которое будет начинаться со слов «Оказывается …», «Я узнал, что …»
- Самооценка
- Закончите фразу:
- Особенно хорошо я усвоил …
- У меня вызвало затруднения …
- Свой результат могу оценить как…
05.12.2015
Вихарева О.А.



























