Просмотр содержимого документа
«Презентация "Кислоты, соли и основания в свете ТЭД"»

Диссоциация кислот, солей и оснований

Вещества в растворах
Электролиты
(водные растворы
проводят эл.ток)
Неэлектролиты (водные растворы не проводят эл. ток )
Вещества с ковалентной неполярной и слабополярной связью
Вещества с ионной и
ковалентной
полярной связью
Все растворимые кислоты, основания (щёлочи) и соли
Все простые вещества, все оксиды и н / р кислоты, основания и соли .

Свойства растворов электролитов определяются свойствами тех ионов, которые они образуют при диссоциации.
По характеру образующихся ионов различают три типа электролитов:
- Кислоты – это электролиты, которые диссоциируют на катионы водорода и анионы кислотного остатка.

Классификации кислот:
- Наличие кислорода в кислотном остатке
- Основность (количество атомов водорода)
- Растворимость в воде
- Летучесть
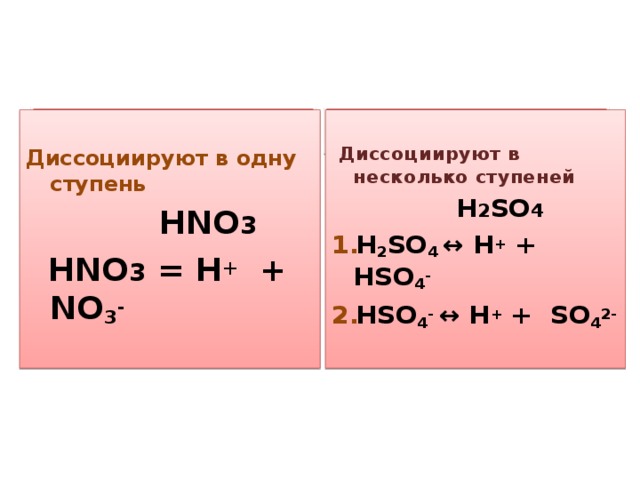
Одноосновные кислоты
Многоосновные кислоты
Диссоциируют в одну ступень
Диссоциируют в несколько ступеней
HNO 3
HNO 3 = H + + NO 3 -
H 2 SO 4
- H 2 SO 4 ↔ H + + HSO 4 -
- HSO 4 - ↔ H + + SO 4 2-

Основания – это электролиты, которые диссоциируют на катионы металла и анионы гидроксогрупп
Классификации оснований:
- По растворимости
- По кислотности (количество гидроксогрупп)
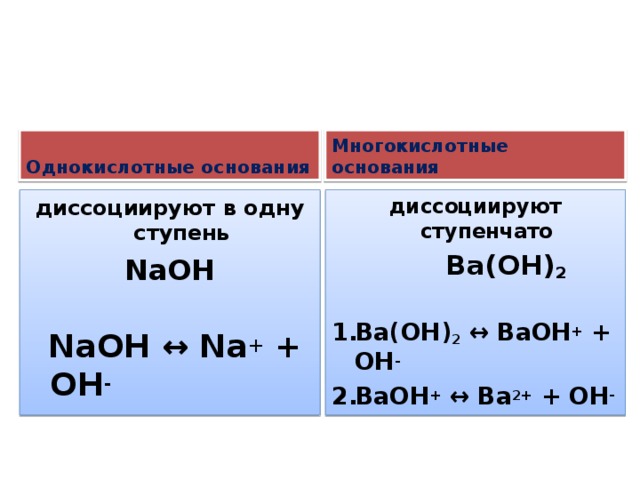
Однокислотные основания
Многокислотные основания
диссоциируют в одну ступень
NaOH
NaOH ↔ Na + + OH -
диссоциируют ступенчато
Ba(OH) 2
- Ba(OH) 2 ↔ BaOH + + OH -
- BaOH + ↔ Ba 2+ + OH -

3. Соли – это электролиты, которые диссоциируют на катионы металла и анионы кислотного остатка
Классификация солей по составу:
- Средние (нормальные) Na 2 CO 3
- Кислые NaHCO 3
- Основные (CuOH) 2 CO 3

Независимо от числа катионов и анионов кислотного остатка средние соли диссоциируют в одну ступень:
Al 2 (SO 4 ) = 2Al 3+ + 3SO 4 2-

Задание
Напишите уравнения диссоциации следующих веществ: HCl, K 2 SO 4 , KOH , Ca(OH) 2

Облако тэгов
# сегодня я узнал…
# было трудно…
# я понял, что…
# я научился…
# я смог…
# мне захотелось…
# было интересно узнать, что…
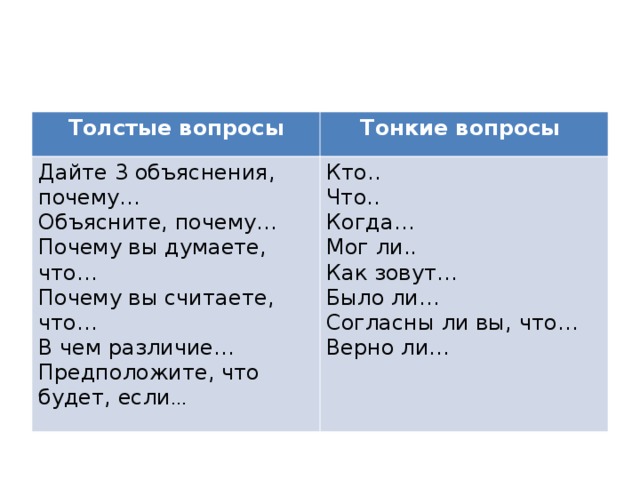
Толстые вопросы
Тонкие вопросы
Дайте 3 объяснения, почему…
Объясните, почему…
Почему вы думаете, что…
Почему вы считаете, что…
В чем различие…
Предположите, что будет, если …
Кто..
Что..
Когда…
Мог ли..
Как зовут…
Было ли…
Согласны ли вы, что…
Верно ли…



























