
Елисеева Г.Н. учитель биологии МБОУ СШ №9
Г. Красноуфимск

Энзимология –
учение о ферментах .
Ферменты – это биологические катализаторы, то есть вещества, которые ускоряют биохимические реакции.
Термин “фермент” (от лат. fermentum – закваска) был предложен в начале XVII века
голландским ученым Ван Гельмондом

- Все ферменты представляют собой глобулярные белки;
- Ферменты увеличивают скорость реакции, но сами в этой реакции не расходуются;
- Присутствие ферментов не влияет ни на природу, ни на свойства конечного продукта реакции;
- Катализируемая реакция обратима;

- Специфичность. Каждый фермент обеспечивает одну или несколько реакций одного типа. Этим обеспечивается тонкая регуляция всех жизненно важных процессов, протекающих в клетке и в организме.
- Благодаря особой пространственной структуре молекулы ферментного белка и определённому расположению аминокислот в нём фермент узнаёт свой субстрат, присоединяет его и ускоряет его превращение.

- Высокая эффективность действия. Очень малое количество фермента вызывает превращение больших количеств субстрата. Например, единственная молекула фермента каталазы может расщепить за секунду до 10000 молекул токсичной для клетки перекиси водорода.
- Способность работать при обычных условиях среды.
- Активность ферментов меняется в зависимости от рН, температуры, давления и от концентраций как субстрата, так и самого фермента;

- Саморегуляция. В белковых молекулах большинства ферментов есть участки, которые узнают конечный продукт. Если такого продукта слишком много, то активность самого начального фермента тормозится им, и наоборот, если продукта мало, то фермент активизируется. Так осуществляется саморегуляция биохимических процессов.

- Почти все ферменты являются белками (но не все белки – ферменты). Представление о том, что ферменты – белки утвердилось не сразу. Для этого надо было научиться их выделять в высоко кристаллической форме. Впервые ферменты в такой форме выделил в 1926 году Дж. Самнер. После этого потребовалось еще 10 лет, в течение которых было получено еще несколько ферментов в кристаллической форме, чтобы представление о белковой природе ферментов стало доказанным и получило всеобщее признание.

У сложных ферментов помимо белковой части имеется добавочная группа небелковой природы . Белковая часть называется апофермент, а небелковая– кофактор (если это простое неорганическое вещество) или кофермент (если речь идёт об органическом соединении)
- Предшественниками многих коферментов являются витамины. Пантатеновая кислота-предшественник коэнзима А; никотиновая кислота-предшественник НАД и НАДФ, участвующих в окислительно-востановительных реакциях.

- В молекуле фермента имеется активный центр .
- Он состоит из двух участков- сорбционного и каталитического . Первый отвечает за связывание фермента с молекулой субстрата, а второй - за протекание собственно акта катализа.


- Согласно гипотезе, выдвинутой Э. Фишером, субстрат подходит к ферменту, как ключ к замку, т.е. пространственные конфигурации активного центра фермента и субстрата точно соответствуют друг другу. Субстрат сравниваем с “ключом”, который подходит к “замку” – ферменту.

Согласно теории активного центра в молекуле каждого фермента имеется один или более участков, в которых происходит катализ за счёт тесного (во многих точках) контакта между молекулами фермента и субстрата. Вокруг молекулы фермента возникает сильное электрическое поле, где становится возможной ориентация молекул субстрата и приобретение ими ассиметричной формы, что приводит к ослаблению химических связей и увеличению скорости реакции.
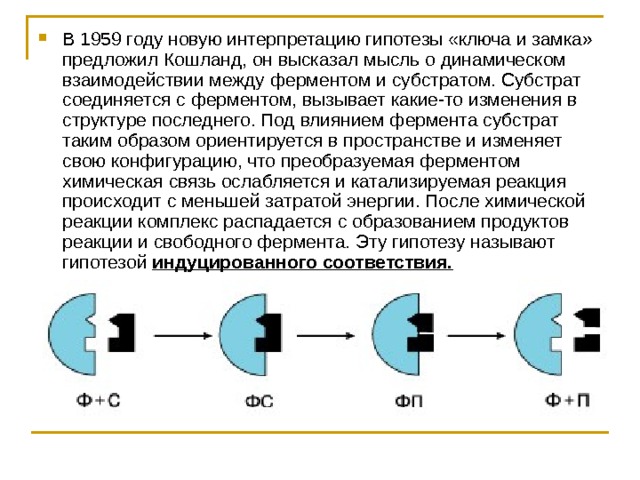
- В 1959 году новую интерпретацию гипотезы «ключа и замка» предложил Кошланд, он высказал мысль о динамическом взаимодействии между ферментом и субстратом. Субстрат соединяется с ферментом, вызывает какие-то изменения в структуре последнего. Под влиянием фермента субстрат таким образом ориентируется в пространстве и изменяет свою конфигурацию, что преобразуемая ферментом химическая связь ослабляется и катализируемая реакция происходит с меньшей затратой энергии. После химической реакции комплекс распадается с образованием продуктов реакции и свободного фермента. Эту гипотезу называют гипотезой индуцированного соответствия.


С возрастанием концентрации фермента растёт и скорость ферментативной реакции


В пределах от 0 до 40 С, при каждом
Повышении температуры на 10 С скорость
ферментативной реакции удваивается.
с повышением температуры движение
молекул ускоряется, и вероятность того,
что реакция между ними произойдёт. За
Пределами этого уровня скорость реакций
снижается,т.к. происходит денатурация
белка.



При постоянной температуре любой фермент
работает наиболее эффективно в узких пределах
рН (6-8). Оптимальным считается то значение рН,
при котором реакция протекает с максимальной
скоростью.
При более высоких и более низких рН активность
фермента снижается, т.к.меняется заряд
ионизированных кислотных и основных групп,
от которого зависит специфичная форма молекул
фермента , а именно меняется форма молекул
активного центра.



- В 1961 году специальной комиссией международного биохимического союза была предложена систематическая номенклатура ферментов. Ферменты были подразделены на 6 групп в соответствии с общим типом реакции, которую они катализируют. Каждый фермент получил систематическое наименование, точно описывающее катализируемую им реакцию.
- Рабочее название складывалось из названия субстрата, типа катализируемой реакции и окончания –аза.
- Например:
Лактат + дегидрогенизация + аза = лактатдегидрогеназа
- Но для давно известных ферментов оставлены прежние названия (пепсин, трипсин).

Группа
Катализируемая реакция
Оксидоредуктазы.( большая роль в энергетических процессах)
Катализирует реакции окисления – восстановления, перенос атомов H и O или электронов от одного к другому.
Трансферазы
Перенос определенных группы атомов от одного вещества к другому
Гидролазы( пищеварительные ферменты, входящие в состав лизосом и других органоидов)
Реакции гидролиза, при которых из субстрата образуются два продукта.
Лиазы (участвующих в регуляциях синтеза и распада промежуточных продуктов обмена )
Ферменты, катализируемые реакции разрыва связей, в субстрате без присоединения воды или окисления.
Изомеразы.
Ферменты, катализирующие превращения в пределах одной молекулы, они вызывают внутримолекулярные перестройки .
Лигазы (синтетазы)
Катализируемое соединение 2-х молекул с использованием энергии фосфатной связи, сопряжено с распадом АТФ.
- В пищевой промышленности ферменты используют при приготовлении безалкогольных напитков, сыров, консервов, колбас, копченостей. В животноводстве ферменты используют при приготовлении кормов. Ферменты используют при изготовлении фотоматериалов. Ферменты используют при обработке овса и конопли. Ферменты используют для смягчения кожи в кожевенной промышленности. Ферменты входят в состав стиральных порошков, зубных паст. В медицине ферменты имеют диагностическое значение – определение отдельных ферментов в клетке помогает распознаванию природы заболевания (например вирусный гепатит – по активности фермента в плазме крови) их используют для замещения недостающего фермента в организме.
- В пищевой промышленности ферменты используют при приготовлении безалкогольных напитков, сыров, консервов, колбас, копченостей.
- В животноводстве ферменты используют при приготовлении кормов.
- Ферменты используют при изготовлении фотоматериалов.
- Ферменты используют при обработке овса и конопли.
- Ферменты используют для смягчения кожи в кожевенной промышленности.
- Ферменты входят в состав стиральных порошков, зубных паст.
- В медицине ферменты имеют диагностическое значение – определение отдельных ферментов в клетке помогает распознаванию природы заболевания (например вирусный гепатит – по активности фермента в плазме крови) их используют для замещения недостающего фермента в организме.








































