
Явления
Различные явления в химии встречаются
Эти явления человеком различаются: Одни – физическими называются,
В них вещества ___ _, Их первоначальный состав ____________ _ . Другие – химическими называются, В них вещества __ ,
Продукты от реагентов ___ ____, Химическими реакциями эти явления называются.

Понятие о химической реакции. Реакции, идущие без изменения состава веществ.

К каким явлениям относятся данные превращения?
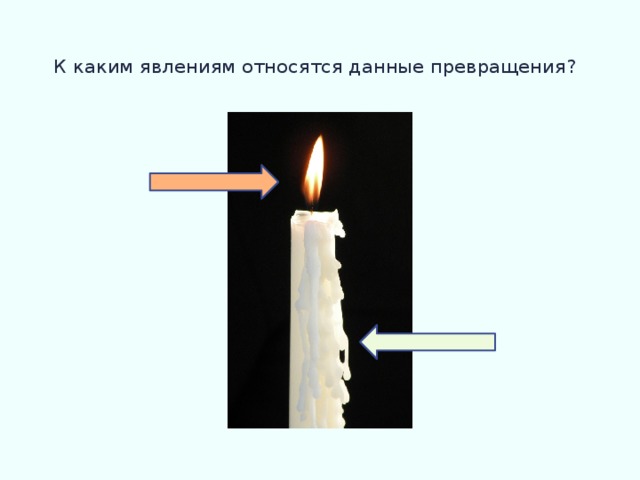
К каким явлениям относятся данные превращения?

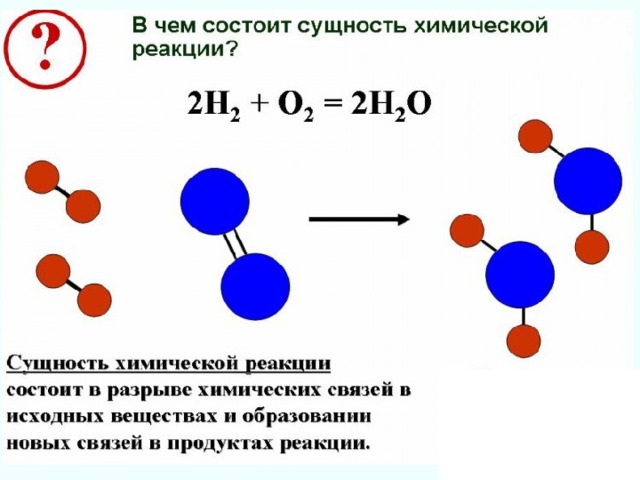
Химическая реакция
это процесс, в результате которого из одних веществ образуются другие вещества, отличающиеся от них по составу или строению, и по свойствам.

Назовите химические процессы:
1) плавление алюминия;
2) на медных предметах образуется зеленый налет;
3) испарение воды;
4) серебряные ложки со
временем чернеют;
5) ржавление гвоздя;
6) образование инея на деревьях;
7) яблоко чернеет на воздухе;
8) скисание молока

Ьдощрщшрщршщршрлштлтлтшщрщшрщтрлтдлтлдрщртлдтдбт длтдтдб

Историческая справка
В 1748 году сформулирован
закон сохранения массы веществ:
«Все перемены, в натуре случающиеся, такого суть состояния, что сколько чего у одного тела отнимается, столько присовокупится к другому»
М.В. Ломоносов
Масса веществ, вступающих в реакцию,
равна массе веществ, образующихся
в результате реакции.

Классификация химических реакций Реакции, идущие без изменения состава веществ
в результате которых из одних веществ образуются другие вещества, отличающиеся по строению и по свойствам, но одинаковые по составу.
В неорганической химии
В органической химии
аллотропные видоизменения одного химического элемента
изомеры
АЛЛОТРОПИЯ
ИЗОМЕРИЯ

Аллотропные видоизменения (модификации)
это простые вещества, образованные одним химическим элементом, а явление их существования называют аллотропией .
С (графит) С (алмаз)
S (ромбическая) S (пластическая)
Р (красный) Р (белый)
Sn (белое олово) Sn (серое олово)
3О 2 (кислород) 2О 3 (озон)

Аллотропные видоизменения УГЛЕРОДА
С (графит) С (алмаз)
Графит – устойчивая при нормальных условиях аллотропная модификация углерода, имеет серо-черный цвет и металлический блеск, кажется жирным на ощупь, очень мягок и оставляет черные следы на бумаге.
Алмаз - бесцветное, прозрачное, сильно преломляющее свет вещество. Алмаз тверже всех найденных в природе веществ, но при этом довольно хрупок. Он настолько тверд, что оставляет царапины на большинстве материалов.
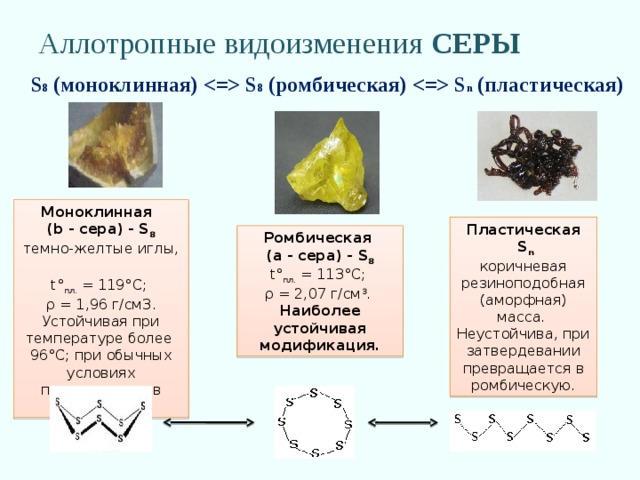
Аллотропные видоизменения СЕРЫ
S 8 (моноклинная) S 8 (ромбическая) S n (пластическая)
Моноклинная (b - сера) - S 8
темно-желтые иглы, t° пл. = 119°C; ρ = 1,96 г/см3. Устойчивая при температуре более 96°С; при обычных условиях превращается в ромбическую.
Пластическая S n
коричневая резиноподобная (аморфная) масса. Неустойчива, при затвердевании превращается в ромбическую.
Ромбическая (a - сера) - S 8
t° пл. = 113°C; ρ = 2,07 г/см 3 . Наиболее устойчивая модификация.
Аллотропные видоизменения ФОСФОРА
Р 4 (белый) Р (красный) Р (черный) Р (металлический)
Белый фосфор представляет собой белое вещество (может иметь желтоватый оттенок ). По внешнему виду он очень похож на очищенный воск или парафин , легко режется ножом и деформируется от небольших усилий.
Химически белый фосфор чрезвычайно активен, медленно окисляется кислородом воздуха уже при комнатной температуре и светится (бледно-зелёное свечение); ядовит.
При 8,3·10 10 Па чёрный фосфор переходит в новую, ещё более плотную и инертную металлическую фазу, а при дальнейшем повышении давления — ещё более уплотняется и приобретает кубическую кристаллическую решётку, при этом его плотность возрастает. Металлический фосфор очень хорошо проводит электрический ток.
Красный фосфор имеет формулу Р n и представляет собой полимер со сложной структурой.
Имеет оттенки от пурпурно-красного до фиолетового.
Химическая активность красного фосфора значительно ниже, чем у белого; ему присуща исключительно малая растворимость.
Ядовитость его в тысячи раз меньше, чем у белого.
Чёрный фосфор представляет собой чёрное вещество с металлическим блеском, жирное на ощупь и весьма похожее на графит, и с полностью отсутствующей растворимостью в воде или органических растворителях.
Проводит электрический ток и имеет свойства полупроводника.

Аллотропные видоизменения ОЛОВА
Sn (белое олово) Sn (серое олово)
Морозной зимой 1916 г. партия олова была отправлена по железной дороге с Дальнего Востока в европейскую часть России, но в назначенное место прибыли не серебристо-белые слитки, а мелкий серый порошок.
За четыре года до этого произошла катастрофа с британской экспедицией Роберта Фолкона Скотта.
Достигнув географической точки Южного полюса, Скотт обнаружил остатки чужого лагеря и палатку с флагом норвежской экспедиции под руководством Руала Амундсена, которая побывала там ровно за месяц до этого.
Разочарованный Скотт и его товарищи отправились в обратный путь, но не обнаружили топлива в одной канистре, потом в другой... Они не могли обогреться и приготовить пищу. Топливо вытекло из канистр сквозь швы, пропаянные оловом. Скотт и четверо его товарищей погибли в жестоких снегах Антарктиды.
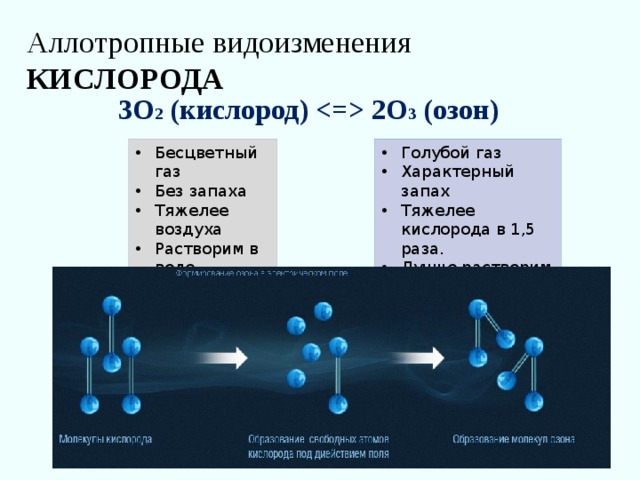
Аллотропные видоизменения КИСЛОРОДА
3О 2 (кислород) 2О 3 (озон)
- Бесцветный газ
- Без запаха
- Тяжелее воздуха
- Растворим в воде
- Голубой газ
- Характерный запах
- Тяжелее кислорода в 1,5 раза.
- Лучше растворим в воде, чем кислород.

Изомеры
- это вещества, имеющие одинаковый состав, т.е. одинаковую молекулярную формулу, но разное строение, а следовательно и разные свойства.
Явление существования изомеров называют изомерией , а реакции взаимопревращения изомеров – реакциями изомеризации .
СН 3 -СН 2 -СН 2 -СН 2 -СН 2 -СН 2 -СН 3 →

Изомеры
- это вещества, имеющие одинаковый состав, т.е. одинаковую молекулярную формулу, но разное строение, а следовательно и разные свойства.
Явление существования изомеров называют изомерией , а реакции взаимопревращения изомеров – реакциями изомеризации .
СН 3
I
СН 3 -СН 2 -СН 2 -СН 2 -СН 2 -СН 2 -СН 3 → СН 3 -С-СН-СН 3
I I
Н 3 С СН 3

Изомеры
- это вещества, имеющие одинаковый состав, т.е. одинаковую молекулярную формулу, но разное строение, а следовательно и разные свойства.
Явление существования изомеров называют изомерией , а реакции взаимопревращения изомеров – реакциями изомеризации .
СН 3
I
СН 3 -СН 2 -СН 2 -СН 2 -СН 2 -СН 2 -СН 3 → СН 3 -С-СН-СН 3
I I
Н 3 С СН 3
н -гептан
2,2,3 -триметилбутан
С 7 Н 16

Изомеры
- это вещества, имеющие одинаковый состав, т.е. одинаковую молекулярную формулу, но разное строение, а следовательно и разные свойства.
Явление существования изомеров называют изомерией , а реакции взаимопревращения изомеров – реакциями изомеризации .
СН 3
I
СН 3 -СН 2 -СН 2 -СН 2 -СН 2 -СН 2 -СН 3 → СН 3 -С-СН-СН 3
I I
Н 3 С СН 3
н -гептан
2,2,3 -триметилбутан
На реакциях изомеризации основано проведение риформинга нефти и бензина, для повышения октанового числа бензина

Выполните задание:
- Составьте структурные формулы возможных изомеров состава
С 5 Н 12
- и назовите их по номенклатуре ИЮПАК
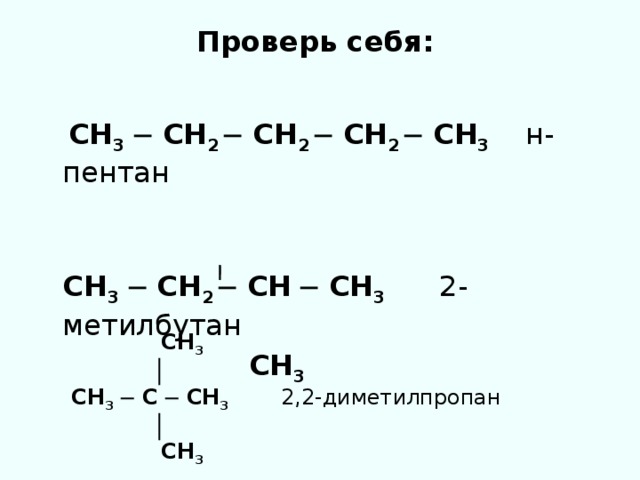
Проверь себя:
СН 3 ─ СН 2 ─ СН 2 ─ СН 2 ─ СН 3 н-пентан
СН 3 ─ СН 2 ─ СН ─ СН 3 2-метилбутан
СН 3
СН 3
│ СН 3 ─ С ─ СН 3 2,2-диметилпропан
│
СН 3

ВЫВОДЫ :
Одной из причин многообразия неорганических веществ является аллотропия, которая может быть обусловлена :
1) различным составом молекул простых веществ (аллотропия кислорода: кислород О 2 и озон О 3 );
2) различным кристаллическим строением аллотропных модификаций (аллотропные модификации углерода имеют атомную решетку, но у алмаза она объемная тетраэдрическая, а у графита – слоистая).
Причиной многообразия органических веществ является изомерия и существование изомеров.

Подведём итоги:
- Независимо от того, между какими веществами – органическими или неорганическими – происходит химическое превращение, для них характерны одни и те же закономерности.
- Мир химических реакций огромен, разнообразен и интересен. Знание классификации и типов химических реакций помогут объяснить вам многие химические процессы, протекающие в природе, в организме человека, а также многие другие химические явления, с которыми вы постоянно сталкиваетесь.

Подумай
Почему деление на металлы и неметаллы условно?
Плотность паров этиленового углеводорода по водороду равна 28. Определите его молекулярную формулу. Сколько изомеров имеет данный алкен?

ДОМАШНЕЕ ЗАДАНИЕ :
§ 13 с. 112-117, задания 6, 8 на с. 117










































