

СДЕЛАЙТЕ СВОИ УРОКИ ЕЩЁ ЭФФЕКТИВНЕЕ, А ЖИЗНЬ СВОБОДНЕЕ
Благодаря готовым учебным материалам для работы в классе и дистанционно
Скидки до 50 % на комплекты
только до
Готовые ключевые этапы урока всегда будут у вас под рукой
Организационный момент
Проверка знаний
Объяснение материала
Закрепление изученного
Итоги урока


Проектная работа
Коррозия металлов является серьезной проблемой в различных отраслях, так как она приводит к разрушению изделий, снижая их прочность и долговечность. В данном докладе мы рассмотрим природу коррозии, методы её возникновения и причины.
Просмотр содержимого документа
«Проектная работа»
МИНИСТЕРСТВО ОБРАЗОВАНИЯ И НАУКИ ХАБАРОВСКОГО КРАЯ
Краевое государственное бюджетное
профессиональное образовательное учреждение
«Комсомольский-на-Амуре судомеханический техникум
имени В.В. Орехова» (КГБ ПОУ КСМТ)
Направление: Технологии металлургического производства
Тема работы: Коррозия металлов
Методы борьбы с коррозией металла
Выполнили: Рыбалко Д.А, Решеткова Е.
студенты 1 курса СП 24с, УКП 24с
специальности: Сварочное производство, Управление качеством продукции, процессов и услуг (по отраслям)
Научный руководитель: Середа Т.Н.
Комсомольск-на-Амуре, 2024г.
Коррозия металлов является серьезной проблемой в различных отраслях, так как она приводит к разрушению изделий, снижая их прочность и долговечность. В данном докладе мы рассмотрим природу коррозии, методы её возникновения и причины. Особое внимание будет уделено способам защиты от коррозии, таким как покрытие, гальванизация, катодная защита и использование коррозионно-устойчивых сплавов. Эти методы помогают обеспечить долговечность металлоконструкций и продуктов, а также снижают экономические затраты на обслуживание и замену поврежденных изделий. Мы также обсудим примеры применения этих методов в реальной жизни.
Название: “ Коррозия металлов Методы борьбы с коррозией металла»
Тип: Доклад
Объект исследования: Металлические материалы
Предмет исследования: Процессы коррозии металла
Методы исследования: Химический анализ, электрохимические методы, микроскопия и др.
Научная новизна: Разработка новых методов защиты от коррозии, исследование механизмов разрушения металла под воздействием коррозии
Цель доклада: Изучение процессов коррозии металла и разработка эффективных методов защиты от нее
Проблема: Высокие затраты на ремонт и замену корродированных металлических конструкций
Целевая аудитория: Производственные предприятия, инженеры-конструкторы, научные исследователи
Задачи доклада:
1. Провести анализ механизмов коррозии металла
2. Изучить существующие методы защиты от коррозии
3. Разработать новые методы защиты и провести их тестирование
4. Подготовить рекомендации по применению разработанных методов защиты.
Содержание
ВВЕДЕНИЕ……………………………………………………………………………………..стр.2
ОСНОВНАЯ ЧАСТЬ……………………………………………………………………………стр.3
История…………………………………………………………………………………………..стр.4
Механизмы коррозии металла………………………………………………………………….стр.5
Электрохимические процессы……………………………………………………… ………....стр.7
Биологическая коррозия металлов…………………………………………………………… стр.8
Кавитационная коррозия металлов…………………………………………………………….стр.8
Виды электрохимических процессов…………………………………………………………. стр.9
Факторы, влияющие на коррозию…………………………………………………...................стр.11
Существующие методы защиты……………………………………………………..................стр.12
Покрытия…………………………………………………….................................................... стр.13
Ингибиторы коррозии…………………………………………………………………………...стр.14
Катодная защита……………………………………………………………………… ……….. .стр.15
Экономический ущерб от коррозии…………………………………………………………… стр.16
Разработка новых методов защиты……………………………………………………………..стр.17
Электрохимические методы………………………......................................................................стр.18
Наноматериалы…………………………………………………………………………………...стр.19
Инновационные подходы……………………………………………………………………. стр.20
Заключение……………………………………………………………………………………….стр.21
Список использованной литературы………………………………………………………........стр.22
1. История изучения коррозии металлов насчитывает несколько этапов:
Древний период. Древнегреческий историк Геродот (5 век до нашей эры) и древнеримский учёный Плиний Старший (1 век до нашей эры) упоминают о применении олова для защиты железа от ржавчины.
Начало научного изучения М. В. Ломоносовым. Он провёл эксперимент — точное взвешивание нагретого в запаянной реторте до высокой температуры металла. Учёный констатировал, что после обжига металла и его вскрытия в него входит воздух, вследствие чего металл делается тяжелее.
Развитие электрохимической теории благодаря работам русских академиков В. В. Петрова, Т. Гротгуса, Э. Х Ленца, В. А. Кистяковского, Н. А. Изгарышева. Они в значительной мере содействовали развитию электрохимической теории растворения металлов.
Сформулировка теории электрохимической коррозии советскими учёными. В начале тридцатых годов XX века советский учёный Александр Фрумкин, изучая амальгамы металлов, показал, что активный металл амальгамы растворяется в кислотах, хотя амальгама — это однородное вещество. В 1935 году Алексей Шултин объяснил коррозию как индивидуальных металлов, так и сплавов. Он рассмотрел механизм протекания процесса коррозии и факторы, влияющие на его скорость. В том же 1935 году Ярослав Дурдин высказал мысль о растворении металлов в кислотах без наличия инородных включений в них. Таким образом, советские учёные, в первую очередь Шултин и Дурдин, сформулировали теорию электрохимической коррозии металлических материалов.
Создание отечественной науки о коррозии Г. В. Акимовым. Учёный заложил основы структурной коррозии металлов, исследовал ряд теоретических и практических вопросов коррозии и создал школу коррозионистов в советские времена.
Как только металл вошел в жизнь людей сразу же появилась проблема с коррозией. Корро́зия (от лат. corrosio — разъедание) — самопроизвольное разрушение металлов и сплавов в результате химического, электрохимического или физико-химического взаимодействия с окружающей средой. В повседневной жизни чаще используют термин «ржавление».
Первые упоминания о коррозии относятся к IV — V веку до нашей эры. Известный философ древности Платон говорил о ржавчине, как о чем-то земном, что выделяется из металла.
Для защиты металла в ход шло масло и жир, затем металл стали покрывать легкоплавким оловом. Этот процесс назывался “лужение” и в V веке до н.э. его упоминал в своих трудах известный историк Геродот. Но и лужение не спасало от разрушения.
Прошло 2000 лет, а в понимании природы коррозии ничего не изменилось. Один из основателей минералогии Георг Агрикола (1494-1555 г.) в 1546 г. писал: ”… ржавчина является выделением металлического железа”. Для борьбы с этим явлением он предлагал использовать покрытия из гипса, битума, смолы.
2.Механизмы коррозии металла
Коррозионные разрушения металла – явление достаточно известное. Поверхностная ржавчина является только одним из признаков коррозии. Под действием неблагоприятных факторов окружающей среды структура металла постепенно разрушается вглубь. Как правило, коррозионные процессы запускаются при контакте металла с жидкими, газообразными веществами. Чаще всего это влага – конденсат, атмосферные осадки, сточные воды. Последующее разрушение происходит из-за окисления материала. Результатом коррозионного воздействия становится утрата конструкцией своих свойств, выход изделия из строя. Скорость процесса окисления во многом зависит от степени агрессивности окружающей среды.
Коррозия металлов — это самопроизвольный процесс разрушения металлов и их сплавов под воздействием факторов окружающей среды (кислорода, влаги, вредных примесей в воздухе).
Различают химическую и электрохимическую коррозию:
Химическая коррозия — взаимодействие металлов с сухими газами или жидкостями, не проводящими электрический ток (керосин, бензин и др.). Химической коррозии подвергаются металлы при термической обработке, детали двигателей внутреннего сгорания, арматура печей, бензобаки, нефтепроводы, нефтехимическое оборудование и др..
Электрохимическая коррозия — разрушение металла, который находится в контакте с другим металлом в присутствии электролита. К электрохимической коррозии относятся все случаи коррозии в водных растворах. Электрохимической коррозии подвергаются подводные части судов, паровые котлы, проложенные в земле трубопроводы.
Из-за коррозии поверхность металлических изделий покрывается налётом из продуктов окисления и теряет блеск. Изменяется электропроводность металла, уменьшается его
пластичность и прочность.
Контактная коррозия - Происходит при контакте двух различных металлов в электролитическом растворе. Различные металлы имеют разные электродные потенциалы, поэтому между ними возникает разность потенциалов, которая вызывает ускоренное разрушение одного из металлов.
Щелевая коррозия - Возникает в узких зазорах или щелях, где доступ кислорода ограничен. В таких местах концентрация ионов водорода увеличивается, что создает кислую среду и ускоряет коррозию.
2.2 Почему образуется коррозия?
Жизнь современного человека нельзя представить без металлов. Они окружают нас везде - это и бытовая техника в наших домах, и транспортные средства, на которых мы добираемся до дома или работы, и смартфоны, без которых многие из нас не представляют жизнь. Почти всё, что нас окружает состоит из металлов, но, к сожалению, как и всё в этом мире, они не вечны и под действием внешней среды разрушаются - корродируют.
Почему коррозия «выгодна» для металлов? Дело в том, что большинство из них существуют в природе в химически связанном состоянии, например, в виде оксидов (корунд) или сульфидов (пирит). В чистом виде почти все металлы неустойчивы и чтобы выделить их из соединений приходится затрачивать немалую энергию. Обратный же процесс, когда металлы переходят в связанное состояние, всегда термодинамически более выгоден. Поэтому он происходит самопроизвольно, а металлы при любой возможности стремятся вступить в реакцию со своим окружением и перейти в более устойчивую форму. Иллюстрация этого представлена на рисунке
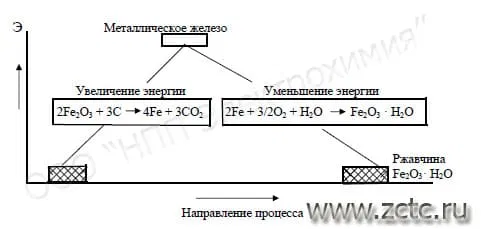
Железо, его сплавы подвержены разрушению – коррозии. Она возникает при электрохимическом, химическом взаимодействии отдельных компонентов материала с веществами из окружающей среды. Окислительно-восстановительные реакции способствуют преобразованию металлов в их оксиды.
Коррозия металлов возникает вследствие химических или электрохимических взаимодействий металлов со средой.
Некоторые причины, по которым это происходит:
Окисление. Передача электронов от металла к кислороду приводит к появлению оксидов металла.
Трение. При постоянном соприкосновении металл изнашивается, что создаёт условия для более интенсивного воздействия окислительных сред и ускоренного разрушения.
Влага. Повышенная влажность способствует активации процессов, особенно если вода содержит растворенные соли.
Химические вещества. Наличие агрессивных химических составов в окружающей среде, таких как кислоты, щелочи, соли и другие соединения, может ускорить изменения.
Электролитическая среда. Некоторые среды могут служить электролитами, что усиливает коррозию.
Разностные потенциалы. Если на металлической поверхности есть места с разными потенциалами, это может создать условия для образования анодов и катодов, что способствует коррозии.
Микробиологическая коррозия. Некоторые виды бактерий и микроорганизмов могут вызывать коррозию, питаясь металлами или производя агрессивные химические соединения.
Резкий перепад температуры. Это может повлечь за собой коррозионные пятна и нарушение покрытия, если изделие было обработано.
Некачественная механическая обработка. Формирование микротрещин и дефектов на поверхности может привести к концентрации жидкости, агрессивных составов и кислорода.
2.3 Электрохимические процессы
Электрохимические процессы — это процессы химического превращения вещества, происходящие на границе раздела фаз.
Электрохимическая коррозия – это процесс взаимодействия металла с коррозионной средой (электролитом), сопровождающийся окислением металла и восстановлением акцептора из коррозионной среды.
Электрохимическая коррозия подчиняется законам электрохимической кинетики. Она представляет собой переход металла из свободного состояния в связанное с потерей электронов. Скорость такой коррозии зависит от электродного потенциала самого металла.
Современная теория, объясняющая электрохимическую коррозию, была предложена советским учёным, доктором химических наук Яковом Михайловичем Колотыркиным.
В основе этой теории лежит предположение, что вся поверхность металла равнодоступна и для катодной для анодной составляющей процесса коррозии.
Электрохимическая коррозия включает в себя 4 основных стадии (рисунок 2):
1.Растворение металла Me (ионизация) и высвобождение электронов (е);
2.Перенос электронов по металлу (количество их в элементарной стадии - z);
3.Восстановление деполяризатора D (присоединение е);
4.Перенос ионов по раствору электролита.
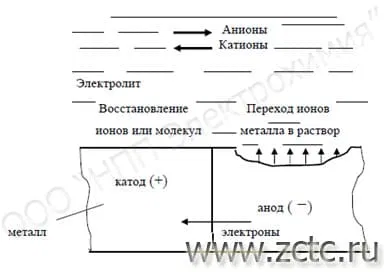
2.4 Биологическая коррозия металлов.
Биокоррозия – это разрушение металла, вызванное непосредственно или косвенно жизнедеятельностью бактерий, плесени и грибов.
Данному типу коррозии подвержены абсолютно все материалы и изделия известные человеку. Это обусловлено образованием окислительных ферментов, вызывающих разрушение различных субстратов с образованием органических кислот. Данные кислоты также оказывают разрушающее действие на материалы.
Например, вырабатываемые грибками органические кислоты вызывают питтинговую коррозию углеродистой стали в трюмах или алюминиевых топливных баков.
2.5 Кавитационная коррозия металлов.
Кавитационная коррозия – это разрушение, возникшее вследствие удара под воздействием текучей среды (потока жидкости или газа). Проявляется при схлопывании на поверхности металла пузырьков газа, сопровождающееся гидравлическим ударом.
2.6 Эрозия.
Эрозия – износ и выбивание частиц металла с поверхности под влиянием твёрдых частиц, находящихся в потоке жидкости. Эрозия металла ускоряется коррозионным действием среды. Иными словами, потеря материала происходит не только вследствие механического действия потока, но и в результате некоторого электрохимического процесса. Иллюстрация процесса эрозии приведена на рисунке 3.
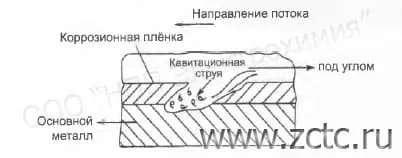 Рисунок 3 – Пример эрозионной коррозии.
Рисунок 3 – Пример эрозионной коррозии.
3.Виды электрохимических процессов
Процессы взаимного превращения химической и электрохимической энергий называют электрохимическими процессами.
Электрохимические процессы делят на две группы:
1. процессы превращения химической энергии в электрическую (в гальванических элементах);
2. процессы превращения электрической энергии в химическую (электролиз).
Законы Фарадея. В 1833г. Английский ученый Фарадей открыл законы, определяющие зависимость между количеством прошедшего электричества и количеством вещества, испытавшего химические превращения на электроде.
С учетом современной терминологии законы Фарадея можно записать в следующем виде:
1. Количество вещества, испытавшего электрохимические изменения на электроде, прямо пропорционально количеству прошедшего электричества.
2. Массы прореагировавших на электроде веществ при постоянном количестве электричества относятся друг к другу как молярные массы их эквивалентов.
При превращении одного моля эквивалентов веществ на электроде через него проходит 96484Кл (А∙с). Эта величина называется постоянной Фарадея. Постоянную Фарадея можно рассчитать исходя из того, что один моль эквивалентов веществ несет 6.022 ∙1023 элементарных зарядов (постоянная Авогадро), а элементарный заряд равен 1,602∙10-19 Кл. Отсюда
F =6.022 ∙1023 ∙1,602∙10-19 =96468 Кл/ (моль-экв.)
При расчетах используется объединенное уравнение двух законов Фарадея m j = Mi G /F,
где mj - масса прореагировавшего на электроде вещества; Mi - молярная масса эквивалентов, G – количество прошедшего электричества.
Таким образом, зная количество вещества, испытывающего превращения на электроде можно рассчитать количество электричества, которое должно пройти через электрохимическую ячейку. Например, если в результате реакции
Cu2+ + 2e = Cu
На электроде выделилось 63,54 г меди, то теоретическое количество электричества определяется из соотношения
96500 Кл (26,8 А∙ч) - 31,77 г Cu (масса моля эквивалентов)
Х « - 63,5 « Cu
Отсюда следует, что через электрод теоретически должно пройти количество электричества
Х = 96500∙63,54 / 31,37 = 194000 Кл.
Понятие об электродном потенциале. Рассмотрим процессы, протекающие при погружении металла в раствор собственных ионов. В узлах кристаллической решетки металла расположены ионы, находящиеся в равновесии со свободными электронами:
М+∙ е ↔ М+ + е
При погружении металла в раствор начинается сложное взаимодействие металла с компонентами раствора. Наиболее важной является реакция поверхностных ионов металла, находящихся в узлах решетки, с полярными молекулами воды, ориентированными у поверхности электрода. В результате взаимодействия происходит окисление металла и его гидратированные ионы переходят в раствор, оставляя в металле электроны, заряд которых не скомпенсирован положительно заряженными ионами в металле:
М + mН2О → М(Н2О)mn+ + ne
Металл становится заряженным отрицательно, а раствор - положительно. Положительно заряженные ионы из раствора притягиваются к отрицательно заряженной поверхности металла. На границе металл – раствор возникает двойной электрический слой. Между металлом и раствором возникает разность потенциалов, которая называется электродным потенциалом или потенциалом электрода. По мере перехода ионов в раствор растет отрицательный заряд поверхности металла и положительный заряд раствора, что препятствует окислению металла. Наряду с этой реакцией протекает обратная реакция – восстановление ионов металла до атомов:
М(Н2О)mn+ + ne → М + mН2О
С увеличением скачка потенциалов между электродом и раствором скорость прямой реакции падает, а обратной реакции растет. При некотором значении электродного потенциала скорость прямого процесса равна скорости обратного процесса, устанавливается равновесие:
М + mН2О ↔ М (Н2О)mn+ + ne
Для упрощения гидратационную воду обычно в уравнение реакции не включают и она записывается в виде:
М ↔ М n+ + ne
Равновесие имеет динамический характер, процессы при равновесии идут с одинаковой скоростью в прямом и обратном направлениях.
Электролиз. Электролизом называют процессы, происходящие на электродах под действием электрического тока, подаваемого от внешнего источника. При электролизе происходит превращение электрической энергии в химическую. Ячейка для электролиза, называемая электролизером, состоит из двух электродов и электролита. Электрод, на котором идет реакция восстановления (катод), у электролизера подключен к отрицательному полюсу внешнего источника тока. Электрод, на котором протекает реакция окисления (анод), подключен к положительному полюсу источника тока.
Электрохимическая система состоит из двух электродов – анода и катода,
соединенных друг с другом внутренней и внешней цепью.
Роль внутренней цепи выполняет электролит, внешней – металлический проводник,
соединяющий электроды. Различают два типа электрохимических систем – электролизеры
и гальванические элементы. Рассмотрим особенности гальванических элементов
(электролизеры рассмотрены в 8.4).
Гальваническим элементом называется прибор (устройство), в котором энергия
химической реакции превращается в электрическую энергию.
Основу гальванического элемента, как любой электрохимической системы, образуют
анод и катод. Характеристической особенностью электрода является не знак его заряда, а
окислительно-восстановительный процесс, который на нем протекает.
Анодом называют электрод, на котором, реализуется реакция окисления (в
гальваническом элементе анод имеет отрицательный, а при электролизе – положительный
заряд).
Катодом называют электрод, на котором, реализуется реакция восстановления (в
гальваническом элементе катод имеет положительный, а при электролизе –
отрицательный заряд).
Гальванический элемент позволяет при помощи вольтметра определить
электродвижущую силу (ЭДС), которая характеризует возможность осуществления
электрохимических реакций и является величиной, определяющей восстановительную
активность конкретного металла.
4.Факторы, влияющие на коррозию
1. Состав и структура металла
- Химический состав: Чистые металлы обычно менее подвержены коррозии, чем сплавы. Сплавление металлов с другими элементами может изменять их устойчивость к коррозии. Например, добавление хрома в сталь повышает ее стойкость к коррозии за счет формирования защитного слоя оксидов.
- Микроструктура: Неоднородности в микроструктуре металла могут создавать участки с различной активностью, что увеличивает вероятность возникновения локальной коррозии.
2. Температура
- При повышении температуры скорость химических реакций возрастает, включая процессы коррозии. Высокие температуры также могут способствовать разрушению защитных слоев на поверхности металла.
3. Влажность
- Вода является одним из ключевых факторов, способствующих коррозии. Высокая влажность увеличивает скорость электрохимической коррозии, особенно в сочетании с присутствием солей и других агрессивных веществ.
4. Доступ кислорода
- Окислительные процессы играют важную роль в коррозии. Недостаток кислорода в некоторых зонах может приводить к развитию щелевой коррозии, тогда как избыток кислорода ускоряет образование оксидов на поверхности металла.
5.Тип окружающей среды
- Атмосферная коррозия: Воздействие атмосферных условий, таких как дождь, снег, туман и пыль, влияет на скорость коррозии.
- Подземная коррозия: Почвенная среда содержит влагу, соли и микроорганизмы, которые могут способствовать коррозии подземных конструкций.
6. Биологические факторы
- Микроорганизмы, такие как бактерии и грибы, могут выделять вещества, способствующие коррозии. Особенно это касается анаэробных бактерий, вызывающих микробиологическую коррозию.
5.Существующие методы защиты
1. Покрытия и краски
- Органические покрытия: Лакокрасочные материалы образуют защитный слой на поверхности металла, предотвращающий контакт с агрессивной средой. Такие покрытия могут включать эмали, лаки, грунтовки и другие составы.
- Металлические покрытия: Нанесение тонкого слоя другого металла на поверхность основного материала. Например, цинкование (гальванизация), никелирование или хромирование. Цинковое покрытие защищает сталь даже при повреждении слоя благодаря эффекту протекторной защиты.
2. Протекторная защита
- Метод заключается в присоединении к защищаемому металлу более активного металла (протектора), который служит анодом и разрушается первым, защищая основной металл. Наиболее распространенным примером является использование цинка в качестве протектора для стали.
3. Использование стойких сплавов
- Некоторые сплавы обладают высокой устойчивостью к коррозии благодаря своему составу. Например, нержавеющая сталь содержит хром, который образует на поверхности тонкий слой оксида хрома, препятствующий дальнейшему окислению.
4. Обработка поверхности
- Специальные методы обработки поверхности, такие как фосфатирование, анодирование или пассивация, создают на поверхности металла защитные слои, повышающие его устойчивость к коррозии.
5. Контроль окружающей среды
Коррозия металла может привести к загрязнению окружающей среды, пустой трате ресурсов и повреждению экосистемы.
Коррозия — это предполагаемый процесс, который превращает очищенный металл обратно в более стабильную форму, такую как его оксид, гидроксид или сульфид. Этот процесс может иметь несколько негативных последствий для окружающей среды. Во-первых, это может привести к загрязнению. Когда металлы корродируют, они могут защищать окружающую среду от вредных веществ. Например, ржавое железо может содержать оксиды железа в почве, воде и воздухе, что может быть вредно для растений, животных и людей. Аналогичным образом, корродированный свинец или ртуть могут представлять собой вредные вещества, которые могут загрязнять водные источники и наносить вред водной флоре и фауне.
Во-вторых, коррозия может привести к пустой трате ресурсов. Металлы — это ценные ресурсы, которые часто добываются из земли путем добычи полезных ископаемых, в процессе, который может иметь значительные экологические последствия. Когда эти металлы корродируют, их больше нельзя использовать, и их необходимо заменять, что требует большей добычи и переработки. Это не только истощает ресурсы Земли, но и способствует загрязнению и разрушению окружающей среды обитания.
Наконец, коррозия может нанести вред экосистемам. Например, корродированные металлические конструкции могут разрушиться, нанося физический ущерб окружающей среде. Кроме того, вещества, используемые во время применения, могут изменить pH почвы и воды, что может повлиять на рост растений и выживание животных. Например, оксиды железа могут сделать почву более кислой, что может нанести вред видам растений.
5.1 Покрытия
1. Органические покрытия - Эти покрытия представляют собой лакокрасочные материалы, которые наносятся на поверхность металла для создания защитного барьера. Органические покрытия могут быть выполнены из различных материалов, включая:
- Эмали и краски: Создают плотный слой, который предотвращает проникновение влаги и агрессивных веществ к поверхности металла. Эмали могут содержать пигменты, придающие покрытию дополнительные защитные свойства.
- Лаки: Тонкий прозрачный слой, обеспечивающий защиту от атмосферной коррозии. Лаки часто используются для декоративных целей, но они также защищают металл от внешних воздействий.
- Грунтовки: Наносятся перед основным покрытием для улучшения адгезии и дополнительной защиты. Грунтовка может содержать ингибиторы коррозии, которые замедляют коррозионные процессы.
2. Металлические покрытия - Нанесение тонкого слоя другого металла на поверхность основного материала обеспечивает дополнительную защиту от коррозии. Металлические покрытия могут быть созданы следующими методами:
- Цинкование (гальванизация): Нанесение слоя цинка на сталь. Цинк защищает сталь двумя способами: физически, создавая барьер, и электрохимически, выступая в роли протектора. Даже при повреждении покрытия цинк продолжает защищать сталь, так как он более активный металл.
- Никелирование: Покрытие поверхности металла слоем никеля. Никель обладает хорошей устойчивостью к коррозии и широко применяется в декоративных целях
. - Хромирование: Нанесение слоя хрома на поверхность металла. Хром обеспечивает высокую устойчивость к коррозии и придает изделию блестящий внешний вид.
- Алюминирование: Алюминий образует на своей поверхности плотную оксидную пленку, которая защищает металл от дальнейшего окисления. Алюминиевые покрытия применяются в авиационной и космической технике.
Горячее алюминирование, проводимое в ваннах с расплавленным металлом (так же, как и горячее цинкование), применяют в основном для нанесения покрытий на полосы и листы. По одному из методов горячего А. стальную полосу вначале нагревают в печи с окислительной средой до т-ры 450° С, с тем чтобы сжечь остатки смазочных масел и создать на поверхности изделия тонкую пленку окислов железа. Затем полоса поступает в печь с восстановительной средой, где при т-ре 730—800° С эти окислы восстанавливаются. После охлаждения в спец. зоне печи полосу пропускают через ванну с алюминиевым расплавом, охлаждают на воздухе и сматывают в рулон.
Для нагрева ванн используют силитовые стержни, через к-рые пропускают электрический ток. Есть также ванны с индукционными (посредством токов низкой частоты) и магнито-стрикционными нагревателями. Скорость движения полосы до 1 м/сек. Толщина покрытия (0,02—0,07 мм) определяется его назначением и регулируется скоростью движения полосы и т-рой расплава. Рулоны окончательно обрабатывают обычно в правильных машинах, иногда — в клетях для холодной прокатки (дрессировки). Для того, чтобы на поверхности изделий и расплавленного металла не образовывались окисные пленки, снижающие адгезию алюминия и основы, в металл вводят флюсы, процесс ведут в защитной среде или на поверхность изделия предварительно наносят промежуточные покрытия
Покрытия из чистого алюминия достаточно стоики в воде и на воздухе, что обусловлено образованием на поверхности окисной пленки, защищающей металл от дальнейшего окисления. Алюминиевые покрытия устойчивее цинковых — примерно в шесть раз при одинаковой их массе и в 2,5 раза при одинаковой толщине. В атмосфере пром. предприятий стойкость горячеалюминиро-ванных изделий в 10 раз выше стойкости горячеоцинкованных, в горячей воде — в 15 раз. Алюминированные изделия сохраняют блеск до т-ры 470° С, отражая 85% тепла и света. Вакуумное алюминиевое покрытие в 15—20 раз повышает стойкость стали к газовой коррозии при т-ре 700—800° С.
Алюминирование дает возможность защищать от коррозии детали самолетов, ракет и автомобилей, сварные трубы, стенные и кровельные панели, обогревательные приборы, сельскохозяйственный инвентарь и инструменты, изделия бытового назначения. Алюминированную жесть используют взамен луженой в консервной промышленности. Экономическая эффективность А. основывается на его низкой себестоимости, на существенном повышении срока службы алюминированных изделий, прежде всего изделий из сталей и алюминиевых сплавов
5.2 Ингибиторная защита
Ингибиторная защита коррозии представляет собой эффективный метод снижения скорости коррозионных процессов посредством добавления специальных химических соединений, называемых ингибиторами коррозии, в окружающую среду или непосредственно на поверхность металла. Ингибиторы действуют, формируя защитную пленку на поверхности металла, которая предотвращает контакт металла с агрессивными компонентами среды, такими как вода, кислород, кислоты и щелочи.
Ингибиторы коррозии работают по нескольким механизмам:
1. Формирование защитной пленки: Ингибиторы образуют на поверхности металла тонкую пленку, которая изолирует металл от агрессивной среды. Эта пленка может быть органического или неорганического происхождения.
2. Замедление электрохимических реакций: Ингибиторы могут влиять на скорость анодных и катодных реакций, снижая общую скорость коррозии. Это достигается за счет изменения потенциала металла или уменьшения доступности активных центров на его поверхности.
3. Уменьшение активности агрессивных агентов: Некоторые ингибиторы связываются с агрессивными ионами, такими как хлориды, уменьшая их активность и способность инициировать коррозию.
Типы ингибиторной коррозии:
1. По химической природе:
- Неорганические ингибиторы: Включают соединения, такие как нитрит натрия , хроматы , молибдаты и фосфаты . Эти ингибиторы часто используются в системах водоподготовки и охлаждения.
- Органические ингибиторы: Включают аминовые соединения, имидазолины, тиазолины и другие азотсодержащие органические молекулы.
2. По механизму действия:
- Анодные ингибиторы: Увеличивают потенциал анода, что приводит к пассивации поверхности металла.
- Смешанные ингибиторы: Оказывают влияние как на анодные, так и на катодные процессы. Примером смешанного ингибитора является бензотриазол, используемый для защиты меди и её сплавов.
3. По области применения
- Ингибиторы для водных систем: Используются в системах водоснабжения, охлаждения и отопления. Примеры включают нитриты, хроматы и фосфаты.
5.3 Катодная защита
Катодная защита — это метод защиты металлов от коррозии, основанный на изменении электрохимического потенциала защищаемого металла таким образом, чтобы сделать его катодом в электрохимической паре. Это достигается либо подключением внешнего источника постоянного тока, либо использованием более активного металла в качестве анода (протектора). В результате этого процесса коррозия смещается на анод, который постепенно разрушается, оставляя защищаемое изделие практически нетронутым.
Принципы работы катодной защиты:
1. Создание внешнего источника тока: В этом случае к защищаемому объекту подключается отрицательный полюс источника постоянного тока, а положительный полюс соединяется с анодом, выполненным из материала, устойчивого к коррозии.
2. Использование протектора: Вместо подключения внешнего источника тока, к защищаемому металлу подсоединяется кусок более активного металла (протектора), который становится анодом. Протектор разрушается, отдавая электроны, тем самым защищая основной металл.
Достоинства катодной защиты:
- Высокая эффективность: Катодная защита способна полностью остановить коррозию на защищаемом объекте.
- Долговечность: Правильно спроектированная система катодной защиты может работать многие годы без замены компонентов.
- Широкий спектр применения: Подходит для защиты подземных и подводных объектов, таких как трубопроводы, резервуары и морские сооружения.
Недостатки катодной защиты:
- Стоимость установки и обслуживания: Требуется установка сложного оборудования и регулярный мониторинг системы.
- Риск перегрузки: Неправильная настройка системы может привести к избыточной защите, что может вызвать повреждение защищаемого металла.
- Необходимость в источнике энергии: Внешний источник тока требует постоянного энергоснабжения.
5.4 Экономический ущерб от коррозии
Экономические потери от коррозии металлов огромны. В США по последним данным NACE[10], ущерб от коррозии и затраты на борьбу с ней составили 3,1 % от ВВП (276 млрд долларов). В Германии этот ущерб составил 2,8 % от ВВП. По оценкам специалистов различных стран эти потери в промышленно развитых странах составляют от 2 до 4 % валового национального продукта. При этом потери металла, включающие массу вышедших из строя металлических конструкций, изделий, оборудования, составляют от 10 до 20 % годового производства стали[11].
 Обрушение Серебряного моста.
Обрушение Серебряного моста.
Ржавчина является одной из наиболее распространённых причин аварий мостов. Так как ржавчина имеет гораздо больший объём, чем исходная масса железа, её наращивание может привести к неравномерному прилеганию друг к другу конструкционных деталей. Это стало причиной разрушения моста через реку Мианус[англ.] в 1983 году, когда подшипники кронштейна моста проржавели внутри. Три водителя погибли при падении в реку. Исследования показали, что сток дороги был перекрыт и не был почищен, а сточные воды проникли в опоры моста[12]. Согласно исследованию Национального совета по безопасности на транспорте, разрушение моста было вызвано механической поломкой наружного кронштейна, удерживающего пролёт моста и его обоих штифтов. Ржавчина образовалась в подшипнике штифта. А так как её объём всегда гораздо больше, нежели исходная стальная деталь, это привело к неравномерному прилеганию друг к другу частей конструкции. В случае с мостом, ржавая масса отодвинула внутренний кронштейн от конца штифта, скрепляющего между собой наружный и внутренний кронштейны. (При этом возникло усилие, превышающее проектные пределы для зажимов, удерживающих штифты!) Из-за этого вся масса пролёта переместилась на внешний кронштейн. Эта дополнительная нагрузка на него вызвала усталостную трещину в штифте. Когда два тяжелых грузовика въехали в данную секцию моста, штифты окончательно вышли из строя, и пролёт моста упал в реку…
15 декабря 1967 года Серебряный мост, соединяющий Пойнт Плезант, штат Западная Виргиния, и Канауга, штат Огайо, неожиданно рухнул в реку Огайо. В момент обрушения 37 автомобилей двигались по мосту, и 31 из них упали вместе с мостом. Сорок шесть человек погибли, и девять серьёзно пострадали. Помимо человеческих жертв и травм, был разрушен основной транспортный путь между Западной Виргинией и Огайо. Причиной обрушения стала коррозия[13].
Мост Кинзу в Пенсильвании был разрушен в 2003 году от торнадо прежде всего потому, что центральные основные болты проржавели, существенно снизив его устойчивость.
6. Разработка новых методов защиты
Постоянное развитие технологий и поиск новых решений для защиты металлов от коррозии остаются актуальными задачами для ученых и инженеров. Новые методы защиты направлены на повышение эффективности, снижение затрат и минимизацию негативного влияния на окружающую среду. Рассмотрим некоторые перспективные направления разработки новых методов защиты от коррозии.
1. Умные покрытия и самообновляющиеся системы
- Самозалечивающиеся покрытия: Разработаны покрытия, способные самостоятельно восстанавливать поврежденные участки. Например, покрытия с микрокапсулами, содержащими активные компоненты, которые высвобождаются при нарушении целостности покрытия.
- Интерактивные покрытия: Покрытия, изменяющие свои свойства в ответ на изменение условий окружающей среды. Например, покрытия, меняющие проницаемость в зависимости от уровня влажности или концентрации агрессивных веществ.
3. Биоматериалы и биокоррозия
- Антибиотики и антимикробные препараты: Использование биологических агентов для подавления роста микроорганизмов, вызывающих микробиологическую коррозию.
- Биоразлагаемые ингибиторы: Разработка экологически безопасных ингибиторов коррозии на основе природных соединений, которые легко разлагаются после выполнения своих функций.
4. Электрохимические методы нового поколения
- Импульсная катодная защита: Использование импульсного тока для повышения эффективности катодной защиты и снижения потребления электроэнергии.
- Электропроводящие полимеры: Применение электропроводящих полимеров в качестве анодов или катодов для создания гибких и легких систем защиты.
5. Модификация поверхности лазером и плазмой
- Лазерная обработка: Лазерная модификация поверхности металлов для создания наноструктур, улучшающих адгезию покрытий и повышающих коррозионную стойкость.
Лазерная обработка металла от коррозии — это безопасный и экологичный метод, который позволяет удалить окислы без вреда для окружающей среды и без истончения формы изделий.
Принцип работы заключается в том, что загрязнённую поверхность обрабатывают лазерным лучом направленного действия. Короткие мощные импульсы или фотонный пучок вызывают распад частиц подверженного коррозии металла и органических веществ.
В зависимости от типа выбранного излучения воздействие светового потока может быть радикальным (абляция) и более мягким (десорбция):
Абляция — импульсное излучение, приводящее к распаду и испарению слоя ржавчины. С помощью сканирующего устройства оценивают металлическую поверхность и в соответствии с толщиной загрязнений выбирают мощность. Затем снимают слой коррозии или краски, при этом поверхность металла остаётся чистой.
Десорбционный принцип лазерной очистки металла состоит в мягкой обработке фотонным пучком. Удаление происходит не целым слоем, а отдельными чешуйками. Этот метод подходит для очищения изделий с рифлёной и сложной структурной поверхностью.
Преимущества лазерной очистки металла:
простой принцип работы;
отсутствие расходных материалов;
бесшумная работа установки;
высокая точность, равномерность удаления коррозионного слоя, работа без истончения основного материала;
качественная очистка через несколько минут работы;
бесконтактная технология, возможность обработки материалов разного типа, в том числе работа с хрупкими изделиями;
высокий ресурс работы — от 50 тысяч до 90 тысяч часов.
Недостатком можно назвать стоимость оборудования.
- Плазменная обработка: Использование плазмы для модификации поверхности металлов, что позволяет улучшить сцепление покрытий и повысить их защитные свойства.
6.1 Электрохимические методы
Электрохимические методы борьбы с коррозией основаны на управлении электрохимическими реакциями, происходящими на поверхности металла, с целью предотвращения или замедления процессов коррозии. Эти методы включают катодную и анодную защиту, а также использование гальванических пар. Рассмотрим подробнее каждый из них.
1. Анодная защита
Анодная защита — это метод, при котором защищаемый металл становится анодом в электрохимической ячейке. В отличие от катодной защиты, анодная защита направлена на создание пассивного состояния на поверхности металла, что снижает его склонность к коррозии.
Как работает анодная защита?
- Потенциал анода: Подавая небольшой постоянный ток на защищаемую конструкцию, можно поднять потенциал анода выше критического значения, при котором начинается пассивация. В результате на поверхности металла образуется тонкий слой оксида, который предотвращает дальнейшее окисление и коррозию.
Преимущества анодной защиты:
- Эффективность в агрессивных средах: Анодная защита особенно эффективна в условиях, где обычные методы защиты, такие как покрытия, неэффективны.
- Минимальные затраты на эксплуатацию: После настройки системы анодная защита требует минимального вмешательства и обслуживания.
Недостатки анодной защиты: - Ограниченность применения: Анодная защита подходит не для всех металлов и условий эксплуатации.
- Требует точного контроля: Неправильное управление системой может привести к ускорению коррозии вместо её замедления.
2. Гальваническая защита
Гальваническая защита основана на использовании гальванических пар, где более активный металл (анод) жертвенно разрушается, защищая менее активный металл (катод). Этот метод аналогичен использованию протектора в катодной защите, но отличается отсутствием внешнего источника тока.
Как работает гальваническая защита?
- Гальваническая пара: Более активный металл (например, цинк) контактирует с менее активным металлом (например, сталью).
6.2 Наноматериалы
Нано материалы играют ключевую роль в разработке современных методов защиты от коррозии. Благодаря своим уникальным свойствам, таким как высокая удельная поверхность, повышенная реактивность и возможность модифицирования на атомарном уровне, наноматериалы предлагают новые подходы к созданию эффективных защитных покрытий и ингибиторов коррозии. Рассмотрим основные виды наноматериалов, используемых для борьбы с коррозией, и их применение.
1. Наночастицы металлов и оксидов
Наночастицы металлов и их оксидов, такие как нано частицы цинка, алюминия, титана и кремния, используются для создания защитных покрытий. Эти наночастицы обладают высокой адгезией к подложке и формируют плотные и прочные покрытия, которые эффективно защищают металл от агрессивных сред.
Применение:
- Антикоррозионные покрытия: Наночастицы металлов и оксидов добавляются в краски и лаки для улучшения их защитных свойств. Например, наночастицы цинка могут использоваться в цинк-наполненных покрытиях для защиты стали.
- Само залечивающиеся покрытия: Нано частицы, заключенные в микрокапсулы, могут высвобождаться при повреждении покрытия и заполнять трещины, предотвращая дальнейшее распространение коррозии.
2. Углеродные наноматериалы
Углеродные наноматериалы, такие как углеродные нанотрубки (CNT) и графен, обладают высокой механической прочностью, химической стойкостью и электропроводностью. Они используются для усиления традиционных покрытий и создания новых композитных материалов.
Применение:
- Усиление покрытий: Добавление CNT и графена в полимерные покрытия улучшает их механические свойства и коррозионную стойкость.
- Электропроводящие покрытия: CNT и графен могут использоваться для создания электропроводящих покрытий, которые предотвращают накопление статического электричества и снижают риск коррозии.
3. Нано композиты Нано композиты — это материалы, состоящие из наноразмерных наполнителей, распределенных в матрице из полимеров, металлов или керамик. Они сочетают в себе лучшие свойства каждого компонента, обеспечивая повышенную прочность, жесткость и коррозионную стойкость.
Применение:
- Защитные покрытия: Нанокомпозиты на основе полимеров и наночастиц металлов или оксидов используются для создания высокопрочных и долговечных покрытий
6.3 Инновационные подходы
Борьба с коррозией остается одной из важнейших задач в различных отраслях промышленности, строительства и транспорта. Современные инновационные подходы к защите металлов от коррозии включают использование новых материалов, технологий и методов, направленных на повышение эффективности, снижение затрат и минимизацию негативного влияния на окружающую среду. Рассмотрим некоторые из последних достижений в этой области.
1. Умные покрытия и само обновляющиеся системы
- Самозалечивающиеся покрытия: Разработаны покрытия, способные самостоятельно восстанавливать поврежденные участки. Например, покрытия с микрокапсулами, содержащими активные компоненты, которые высвобождаются при нарушении целостности покрытия.
- Интерактивные покрытия: Покрытия, изменяющие свои свойства в ответ на изменение условий окружающей среды. Например, покрытия, меняющие проницаемость в зависимости от уровня влажности или концентрации агрессивных веществ.
2. Наноразмерные добавки и композиты
- Наночастицы: Добавление наночастиц металлов, оксидов или углеродных нанотрубок в покрытия или металлические матрицы улучшает их механические и антикоррозионные свойства.
- Графеновые покрытия: Графен обладает высокой прочностью и химической стойкостью, что делает его перспективным материалом для создания ультратонких и высокоэффективных защитных покрытий.
3. Биоматериалы и биокоррозия
- Антибиотики и антимикробные препараты: Использование биологических агентов для подавления роста микроорганизмов, вызывающих микробиологическую коррозию.
- Биоразлагаемые ингибиторы: Разработка экологически безопасных ингибиторов коррозии на основе природных соединений, которые легко разлагаются после выполнения своих функций.
4. Электрохимические методы нового поколения
- Импульсная катодная защита: Использование импульсного тока для повышения эффективности катодной защиты и снижения потребления электроэнергии.
- Электропроводящие полимеры: Применение электропроводящих полимеров в качестве анодов или катодов для создания гибких и легких систем защиты.
Импульсная катодная защита металла — это стратегия борьбы с коррозией, которая использует силу электричества для подавления электрохимических реакций, вызывающих коррозию металла.
Система импульсной катодной защиты состоит из:
Выпрямителя — электрического устройства, преобразующего переменный ток из электросети в постоянный ток.
Анода — инертного, проводящего материала (например, смешанный оксид металла или графит), зарытого в почву на некотором расстоянии от трубопровода.
Контрольного электрода — специализированного электрода, закопанного рядом с трубопроводом, который измеряет электрический потенциал между трубопроводом и окружающей почвой.
Принцип работы: выпрямитель направляет электрический ток от анода к металлу, превращая его в катод в электрохимической реакции. Этот импульсный ток создаёт на металле отрицательный электрический потенциал, который противодействует естественной разности потенциалов между металлической конструкцией и окружающей средой, вызывающей коррозию.
Преимущества импульсной катодной защиты:
обеспечивает активную, непрерывную защиту от коррозии, в отличие от пассивных методов;
систему можно контролировать и настраивать удалённо, что позволяет эффективно обслуживать и оптимизировать систему;
позволяет значительно продлить срок службы заглублённых трубопроводов.
Заключение
Коррозия металлов — одна из главных проблем, с которой сталкиваются различные отрасли промышленности, строительства и транспорта. Она приводит к значительным экономическим потерям, ухудшает безопасность и сокращает срок службы металлических конструкций. Однако благодаря современным научным достижениям и технологическим инновациям борьба с коррозией стала более эффективной и целенаправленной.
Разработаны разнообразные методы защиты металлов от коррозии, среди которых выделяются электрохимические методы, такие как катодная и анодная защита, а также использование гальванических пар. Эти методы доказали свою эффективность в различных условиях эксплуатации, позволяя значительно замедлить или вовсе остановить коррозионные процессы.
Кроме того, значительное внимание уделяется применению наноматериалов, которые демонстрируют выдающиеся антикоррозионные свойства. Наночастицы металлов, оксиды, углеродные нанотрубки и графеновые покрытия уже нашли широкое применение в создании защитных покрытий и ингибиторов коррозии. Эти материалы обладают высокой удельной поверхностью, повышенной реактивностью и возможностью модифицирования на атомарном уровне, что делает их незаменимыми в разработке новых антикоррозионных технологий.
Современные подходы к защите от коррозии также включают использование биоматериалов, интерактивных покрытий, самообновляющихся систем и компьютерного моделирования. Биоматериалы и антибиотики помогают бороться с микробиологической коррозией, а интерактивные покрытия адаптируются к изменениям окружающей среды, обеспечивая длительную защиту. Самообновляющиеся системы способны самовосстанавливаться при повреждениях, увеличивая срок службы конструкций. Компьютерное моделирование и искусственный интеллект позволяют точно прогнозировать поведение материалов и разрабатывать оптимизированные стратегии защиты.
Таким образом, современная наука и технология предлагают множество инструментов для эффективной борьбы с коррозией. Важно продолжать исследования и разработку новых методов, чтобы обеспечить ещё большую защиту металлов и минимизировать экономические потери, связанные с коррозией.
В заключение следует сказать, что, хотя коррозия и является лечебным процессом, она может иметь значительные экологические последствия. К ним относятся загрязнение, растраты ресурсов и ущерб экосистемам. Поэтому важно управлять коррозией и предотвращать ее, чтобы свести к минимуму ее воздействие на окружающую среду.
- Снижение влажности, уменьшение содержания агрессивных веществ в воздухе или воде, поддержание стабильной температуры и исключение механических воздействий помогают снизить риск коррозии.
Список использованной литературы
1 Улиг Г.Г. Коррозия и борьба с ней / Г.Г. Улиг, Р.У. Реви. - Л.: Химия, 1989. - 344 с.
2 Никифоров В.М. Технология металлов и конструкционные материалы / В. М. Никифоров. - М.: Высшая школа, 1980. - 450 с.
3 Герасимов Я. И. Курс физической химии / Я. И. Герасимов, В. П. Древинг, Е. Н. Еремин и др. - М.: Химия, 1973. - 624 с.
4 Исаев Н. И. Теория коррозийных процессов / Н. И. Исаев. - М.: Металлургия, 1997. - 368 с.
5 Cеменова И.В. Коррозия и защита от коррозии / И. В. Семеновой. - М.: ФИЗМАТЛИТ, 2002. - 232 с.
6 Вячеславов П. М. Металлические покрытия, нанесенные химическим способом / П. М. Вячеславов. - Л.: Машиностроение, 1985. - 103 с.
7 Строкан Б. В. Коррозионная стойкость оборудования химических производств: Способы защиты оборудования от коррозии / Б. В. Строкан. -Л.: Химия, 1987. - 280 с.
8 Иванов Е.С. Ингибиторы коррозии металлов в кислых средах Е.С. Ивано. - М.: Металлургия, 1986. - 175 с.
9 Френкель Г.Я. Протекторная защита от коррозии металлического оборудования и специальных стальных конструкций гидротехнических сооружений / Г.Я. Френкель. - М.: Гидропроект, 1993. - 186 с.
10 Шлугер М. А. Коррозия и защита металлов / М. А. Шлугер, Ф. Ф. Ажогин, Е. А. Ефимов. - М.: Металлургия, 1981. - 215 с.
11 Розенфельд И. Л. Защита металлов от коррозии лакокрасочными покрытиями / И. Л. Розенфельд, Ф. И. Рубинштейн, К. А. Жигалова. - М.: Химия, 1987. - 222 с.
12 Люблинский Е. Я. Электрохимическая защита от коррозии / Е. Я. Люблинский. - М.: Металлургия, 1987. - 96 с.












