Просмотр содержимого документа
«Проведение качественных реакций на определение групп катионов и анионов»

Проведение качественных реакция на обнаружение анионов и катионов в сложных растворах.
МБОУ Школа №48 г.о. Самара
Учитель химии и биологии
Терехова О. С.
2020 год

Введение. Аналитические реакции
- Химические превращения, протекающие с изменением состава и строения веществ и используемые в аналитической химии для целей качественного и количественного анализа, называются аналитическими реакциями .
- Химические реакции, при проведении которых наблюдается аналитический эффект (сигнал), называются аналитическими химическими реакциями .
- В качественном анализе практическое значение имеют только специфические реакции.
- Специфические реакции – реакции, которые при определенных условиях позволяют открыть одни ионы в присутствии других ионов по выпадению характерного осадка, изменению окраски или выделению газа и т.д.
- Реакции с внешним эффектом, характерные только для одного иона или соединения, называются специфическими .
- В школьном курсе специфические химические реакции называются качественными химическими реакциями

Аналитические реакции
Все реакции в аналитической химии делятся на две большие группы:
- Специфические (качественные) – эти реакции позволяют при определенных условиях обнаружить только 1 компонент смеси (катион или анион)
- Избирательные (селективные) – эти реакции позволяют за раз обнаружить несколько компонентов в смеси (катионов или анионов)
Однако данные две группы можно объединить в одну и получить групповой анализ всей смеси веществ.
Однако и групповой анализ смеси веществ позволяет определить только определенные группы катионов или анионов за раз.
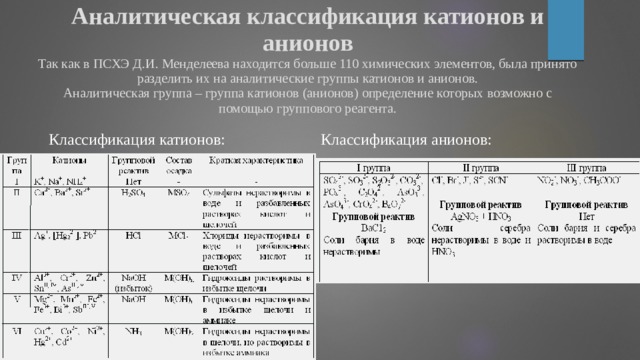
Аналитическая классификация катионов и анионов Так как в ПСХЭ Д.И. Менделеева находится больше 110 химических элементов, была принято разделить их на аналитические группы катионов и анионов. Аналитическая группа – группа катионов (анионов) определение которых возможно с помощью группового реагента.
Классификация катионов:
Классификация анионов:
![Анализ катионов с I-VI группы Прежде чем приступить к анализу предложенной смеси необходимо обратить внимание на окраску раствора. Если данный раствор не имеет цвета, то можно утверждать, что в нем нет «цветных» ионов: Cr 3+ , Fe 3+ , Cu 2+ , Co 2+ , Ni 2+ . Необходимо проверить реакцию раствора: при нейтральной реакции в растворе отсутствуют такие катионы как Sn(II), Sn(IV), Bi 3+ , Hg 2+ . В отдельные пробирки отливается небольшое количество раствора и добавляется HCl, H 2 SO 4 , SnCl 2 : А) Если при добавлении HCL не образуется осадка то отсутствуют катионы Ag + , [Hg 2 ] 2+ , Pb 2+ . Б) Если при добавлении H 2 SO 4 не образуется осадка то отсутствуют катионы Pb 2+ , Sr 2+ , Ba 2+ и возможно Ca 2+ B) Если при добавлении к отдельной порции раствора NaOH и SnCl 2 не появляется черного осадка, то, следовательно, в растворе отсутствуют катионы Bi 2+ , Hg 2+ , Hg 2 ] 2+ 4. После такого группового анализа, позволяющего отмести целые группы ионов, проводят специфические (качественные) реакции на определение конкретных ионов в данном растворе.](https://fsd.multiurok.ru/html/2021/01/13/s_5ffebd33834db/img4.jpg)
Анализ катионов с I-VI группы
- Прежде чем приступить к анализу предложенной смеси необходимо обратить внимание на окраску раствора. Если данный раствор не имеет цвета, то можно утверждать, что в нем нет «цветных» ионов: Cr 3+ , Fe 3+ , Cu 2+ , Co 2+ , Ni 2+ .
- Необходимо проверить реакцию раствора: при нейтральной реакции в растворе отсутствуют такие катионы как Sn(II), Sn(IV), Bi 3+ , Hg 2+ .
- В отдельные пробирки отливается небольшое количество раствора и добавляется HCl, H 2 SO 4 , SnCl 2 :
А) Если при добавлении HCL не образуется осадка то отсутствуют катионы Ag + , [Hg 2 ] 2+ , Pb 2+ .
Б) Если при добавлении H 2 SO 4 не образуется осадка то отсутствуют катионы Pb 2+ , Sr 2+ , Ba 2+ и возможно Ca 2+
B) Если при добавлении к отдельной порции раствора NaOH и SnCl 2 не появляется черного осадка, то, следовательно, в растворе отсутствуют катионы Bi 2+ , Hg 2+ , Hg 2 ] 2+
4. После такого группового анализа, позволяющего отмести целые группы ионов, проводят специфические (качественные) реакции на определение конкретных ионов в данном растворе.
 2 отмечается отсутствие анионов летучих кислот; при pHОбнаружение анионов I и II групп при помощи качественных реагентов AgNO3 и BaCl2 соответственно. Определение присутствия восстановителе при помощи KMnO4 и I2; присутствие окислителей при помощи KI Такими предварительными испытаниями мы отметаем большую часть анионов. " width="640"
2 отмечается отсутствие анионов летучих кислот; при pHОбнаружение анионов I и II групп при помощи качественных реагентов AgNO3 и BaCl2 соответственно. Определение присутствия восстановителе при помощи KMnO4 и I2; присутствие окислителей при помощи KI Такими предварительными испытаниями мы отметаем большую часть анионов. " width="640"
Анализ анионов I-III группы
- Чаще всего в аналитической практике обнаружение анионов проводят дробным методом, то есть в отдельных порциях раствора и в произвольной последовательности.
- Наиболее целесообразно начинать анализ с ряда предварительных испытаний как и в случае с катионным анализом
- Предварительные испытания:
- Определяем pH раствора: при pH2 отмечается отсутствие анионов летучих кислот; при pH
- Обнаружение анионов I и II групп при помощи качественных реагентов AgNO3 и BaCl2 соответственно.
- Определение присутствия восстановителе при помощи KMnO4 и I2; присутствие окислителей при помощи KI
Такими предварительными испытаниями мы отметаем большую часть анионов.











![Анализ катионов с I-VI группы Прежде чем приступить к анализу предложенной смеси необходимо обратить внимание на окраску раствора. Если данный раствор не имеет цвета, то можно утверждать, что в нем нет «цветных» ионов: Cr 3+ , Fe 3+ , Cu 2+ , Co 2+ , Ni 2+ . Необходимо проверить реакцию раствора: при нейтральной реакции в растворе отсутствуют такие катионы как Sn(II), Sn(IV), Bi 3+ , Hg 2+ . В отдельные пробирки отливается небольшое количество раствора и добавляется HCl, H 2 SO 4 , SnCl 2 : А) Если при добавлении HCL не образуется осадка то отсутствуют катионы Ag + , [Hg 2 ] 2+ , Pb 2+ . Б) Если при добавлении H 2 SO 4 не образуется осадка то отсутствуют катионы Pb 2+ , Sr 2+ , Ba 2+ и возможно Ca 2+ B) Если при добавлении к отдельной порции раствора NaOH и SnCl 2 не появляется черного осадка, то, следовательно, в растворе отсутствуют катионы Bi 2+ , Hg 2+ , Hg 2 ] 2+ 4. После такого группового анализа, позволяющего отмести целые группы ионов, проводят специфические (качественные) реакции на определение конкретных ионов в данном растворе.](https://fsd.multiurok.ru/html/2021/01/13/s_5ffebd33834db/img4.jpg)
 2 отмечается отсутствие анионов летучих кислот; при pHОбнаружение анионов I и II групп при помощи качественных реагентов AgNO3 и BaCl2 соответственно. Определение присутствия восстановителе при помощи KMnO4 и I2; присутствие окислителей при помощи KI Такими предварительными испытаниями мы отметаем большую часть анионов. " width="640"
2 отмечается отсутствие анионов летучих кислот; при pHОбнаружение анионов I и II групп при помощи качественных реагентов AgNO3 и BaCl2 соответственно. Определение присутствия восстановителе при помощи KMnO4 и I2; присутствие окислителей при помощи KI Такими предварительными испытаниями мы отметаем большую часть анионов. " width="640"










