Просмотр содержимого документа
«Проверочная работа по теме «Степень окисления. Окислительно – восстановительные реакции»»
Проверочная работа по теме «Степень окисления. Окислительно – восстановительные реакции»
Уровень А.
1.Наименьшую степень окисления сера имеет в соединении
1) 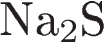 2)
2)  3)
3)  4)
4) 
2. Хлор проявляет положительную степень окисления в соединении с
1) серой 2) водородом 3) кислородом 4) железом
3. Одинаковую степень окисления сера имеет в каждом из двух соединений:
1) 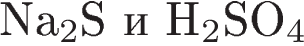 2)
2)  3)
3)  4)
4) 
4. Атом серы имеет минимальную возможную степень окисления в соединении:
1)  2)
2)  3)
3) 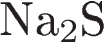 4)
4) 
5. Степень окисления азота в карбонате аммония равна
1) -3 2) -2 3) +2 4) +3
6. Степень окисления, равную +3, атом хлора проявляет в ионе
1)  2)
2)  3)
3)  4)
4) 
7. Какой элемент во всех соединениях проявляет степень окисления +2?
1) магний 2) марганец 3) железо 4) углерод
Уровень В.
В1. Установите соответствие между уравнением реакции и свойством азота, которое он проявляет в этой реакции.
| УРАВНЕНИЕ РЕАКЦИИ |
| СВОЙСТВО АЗОТА |
| А)  Б)  В)  Г) 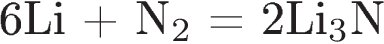 |
| 1) окислитель 2) восстановитель 3) и окислитель, и восстановитель 4) ни окислитель, ни восстановитель |
В2. Установите соответствие между схемой полуреакции восстановления и уравнением реакции.
| Схема полуреакции восстановления | Уравнение реакции |
| А)  | 1)  |
| Б)  | 2) |
| В) 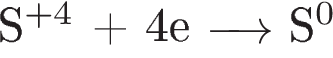 | 3) |
| Г) | 4) |
|
| 5) |
| 6) |
В3. Установите соответствие между схемой окислительно-восстановительной реакции и свойствами атома хлора, которое он проявляет в данной реакции.
| СХЕМА РЕАКЦИИ A) Б) B) Г) | СВОЙСТВО ХЛОРА 1) окислитель 2) восстановитель 3) и окислитель, и восстановитель 4) ни окислитель, ни восстановитель
|
|
|
В4. Установите соответствие между формулой вещества и окислительно-восстановительными свойствами атома азота в нём.
| ФОРМУЛА ВЕЩЕСТВА А) NH4Cl Б) HNO3 В) NH4NO3 Г) N2O3
| СВОЙСТВА АТОМА 1) только окислитель 2) только восстановитель 3) и окислитель, и восстановитель 4) ни окислитель, ни восстановитель
|
Уровень С.
С1.Охарактеризуйте химические реакции с точки зрения всех возможных классификаций.
1.
2.
3.
4.
С2. Закончить уравнение реакции, указать окислитель и восстановитель, процессы окисления и восстановления, уравнять методом электронного баланса:
















