Контроль знаний по теме «Подгруппа углерода». 9 класс.
Время выполнения 45 минут.
1 вариант - для сильных учащихся
2 вариант – для средних учащихся
3 вариант – для слабых учащихся
Ответы и оценивание работы.
| № варианта | 1 вариант | 2 вариант | 3 вариант |
| Ответ | Количество баллов | Ответ | Количество баллов | Ответ | Количество баллов |
| 1 | 2 | 1 | 2 | 1 | 3 | 1 |
| 2 | 4 | 1 | 4 | 1 | 4 | 1 |
| 3 | 4 | 1 | 2 | 1 | 3 | 1 |
| 4 | 1 | 1 | 2 | 1 | 1 | 1 |
| 5 | 2 | 1 | 3 | 1 | 4 | 1 |
| 6 | 1 | 1 | 3 | 1 | 2 | 1 |
| 7 | 3 | 1 | 1 | 1 | 2 | 1 |
| 8 | 1 | 1 | 1 | 1 | 3 | 1 |
| 9 | 1 | 1 | 4 | 1 | 1 | 1 |
| 10 | 4 | 1 | 3 | 1 | 4 | 1 |
| 11 | 3415 | 2 | 1 | 1 | 4 | 1 |
| 12 | 241 | 2 | 2221 | 2 | 2 | 1 |
| 13 | 312 | 2 | 23 | 2 | 3 | 1 |
| 14 |
| 3 | 14 | 2 | 234 | 2 |
| 15 | 22,67 л | 3 |
| 4 | 125 | 2 |
| Оценка | «5» - 22-19 б «4» - 18-14 б. «3» - 13-8 б. | «5» - 21- 18 б. «4» - 17-13 б. «3» - 12 – 7 б. | «5» - 17 -15 б. «4» - 14 – 11б. «3» - 10-6 б. |
1 вариант.
![]() 14. С0 - 4ē→С+4 5 восстановитель, окисляется
14. С0 - 4ē→С+4 5 восстановитель, окисляется
2N+5 +10ē→N20 2 окислитель, восстанавливается
5C +4 KNO3 →5CO2 + 2K2CO3 + N2
15. 2HCl + CaCO3 →CaCl2 + H2O + CO2
M (CaCO3) = 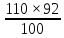 = 101,2 г
= 101,2 г
V (CO2) = 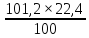 = 22,67 л
= 22,67 л
2 вариант.
15. 2Ca + O2 →2CaO Ca(OH)2 + CO2 изб.→Ca(HCO3)2
CaO+ H2O→ Ca(OH)2 Ca(HCO3)2 → CaCO3 + CO2 + H2O
1 вариант.
При выполнении заданий 1-10 отметьте одну цифру, которая соответствует номеру правильного ответа.
Элемент, электронная формула которого 1 s22s2 2p6 3s2 3p2 , образует водородное соединение
CH4 2) SiH4 3) H2O 4) H2S
У элементов подгруппы углерода с увеличением атомного номера уменьшается
1) атомный радиус 3) число валентных электронов
2) заряд ядра атома 4) электроотрицательность
Только ковалентные связи имеет каждое из двух веществ:
CaO и C3H6 2) NaNO3 и CO 3) N2 и K2S 4) CH4 и SiO2
Кристаллическую структуру, подобную структуре алмаза, имеет
Кремнезем 3) оксид натрия
Оксид углерода (II) 4) белый фосфор
Кремний не взаимодействует с каждым из веществ в ряду
O2, C, Ca 3) NaOH, Mg, F2
KCl, HNO3, H2SO4 4) Mg, P, O2
Оксид углерода (IV) взаимодействует с каждым из двух веществ
водой и оксидом кальция
кислородом и оксидом серы(IV)
сульфатом калия и гидроксидом натрия
фосфорной кислотой и водородом
Карбонат калия в растворе не взаимодействует с
азотной кислотой 3) сульфатом натрия
углекислым газом 4) карбонат кальция
Гидрокарбонат натрия реагирует с
соляной кислотой 3) хлоридом бария
сульфатом бария 4) сульфатом натрия
+HCl +Na2CO3


В схеме превращений CaCO3 X1 X2 + NaCl веществом «Х2» является
CaCO3 2) CaCl2 3) CaO 4) Ca(OH)2
Оксид углерода (II) проявляет восстановительные свойства при нагревании с
N2 2) CO2 3) Fe 4) Fe2O3
При выполнении заданий 11-13 к каждому элементу первого столбца подберите соответствующий элемент из второго столбца. Запишите в таблицу выбранные цифры под соответствующими буквами. Цифры в ответе могут повторяться.
Установите соответствие между реагирующими веществами и продуктами реакции
| Реагирующие вещества | Продукты реакции |
| А) KHCO3 + KOH→ | KNO3 + CO2 + H2O |
| Б) KHCO3 + HCl→ | KCl + Na2CO3 |
| В) K2CO3 + HNO3→ | K2CO3 + H2O |
| Г) K2CO3 + BaCl2→ | KCl+ H2O + CO2 |
|
| BaCO3 + KCl |
|
| KCl + H2CO3 |
Установите соответствие между двумя веществами и реактивом, с помощью которого можно различить эти вещества.
| Вещества | Реактив |
| А) K2CO3 (р-р) и Na2SiO3 (Р-Р) | CuCl2 (р-р) |
| Б) Na2CO3(тв.) и CaCO3 (тв.) | HNO3 (р-р) |
| В) K2SO4 (р-р) и KOH (р-р) | MgO |
|
| H2O |
Установите соответствие между названием вещества и реагентами, с которыми это вещество может взаимодействовать
| Название вещества | Реагенты |
| А) оксид углерода(II) | Ba(OH)2 (р-р), Mg |
| Б) оксид углерода(IV) | CO2 (р-р), HCl (р-р) |
| В) карбонат натрия | Fe2O3, O2 |
|
| H2O, SO2 |
Для заданий 14,15 дайте развернутый ответ.
Используя метод электронного баланса, расставьте коэффициенты в уравнении реакции, схема которой
C + KNO3 →CO2 + K2CO3 + N2
Определите окислитель и восстановитель.
Определите объем (н.у.) оксида углерода (IV), образующегося при растворении 110 г известняка, содержащего 92% карбоната кальция, в избытке соляной кислоты.
2 вариант.
При выполнении заданий 1-11 отметьте одну цифру, которая соответствует номеру правильного ответа.
Атом элемента, максимальная степень окисления которого +4, в основном состоянии имеет электронную конфигурацию внешнего энергетического уровня
3s23p4 2) 3s23p2 3) 2s22p3 4) 2s22p6
У кремния неметаллические свойства выражены сильнее, чем у
углерода 2) кислорода 3) фтора 4) германия
В молекуле СО2 химическая связь
ионная 3) ковалентная неполярная
ковалентная полярная 4) водородная
Кристаллическая решетка графита
ионная 3) молекулярная
атомная 4) металлическая
Углерод взаимодействует со всеми веществами ряда:
Al, O2, Na2O 3) Al, O2, CuO
H2, O2, BaO 4) Al, H2, Li2O
Оксид углерода (II) может взаимодействует с
1) оксидом алюминия 3) кислородом
2) соляной кислотой 4) серной кислотой
Карбонат кальция реагирует с
HCl 2) MgO 3) Pb 4) H2O
Карбонат кальция можно получить при взаимодействии
растворов карбоната натрия и бромида кальция
карбоната кальция и оксида кальция
оксида кальция и карбоната магния
фосфата кальция и карбоната натрия
Углерод выступает в качестве восстановителя в реакции с
водородом 3) алюминием
кальцием 4) оксидом меди(II)
К слабым электролитам относится
гидроксид натрия 3) угольная кислота
азотная кислота 4) хлорид бария
Сокращенное ионное уравнение Ca 2+ +CO32-→ CaCO3 соответствует взаимодействию
хлорида кальция и карбоната натрия
сульфида кальция и углекислого газа
гидроксида кальция и углекислого газа
фосфата кальция и карбоната калия
При выполнении задания 12 к каждому элементу первого столбца подберите соответствующий элемент из второго столбца. Запишите в таблицу выбранные цифры под соответствующими буквами. Цифры в ответе могут повторяться.
Установите соответствие между схемой реакции и степенью окисления восстановителя
| Схема реакции | Степень окисления восстановителя |
| А) С+О2 →СО2 | 1) – 4 |
| Б) СО2 + С→ СО | 2) 0 |
| В) СuO +С →Сu + СО | 3) +4 |
| Г) СН4 +Н2О →СО + Н2 | 4) +2 |
|
| 5)+1 |
|
| 6)-2 |
При выполнении заданий 13-14 из предложенного перечня ответов выберите два правильных и запишите в таблицу цифры.
Общими для углерода и кремния является:
наличие в их атомах трех электронных слоев
образованные ими высших оксидов с общей формулой ЭО2 и одинаковыми химическими свойствами
наличие на внешнем электронном слое их атомов четырех электронов
существование соответствующих им простых веществ в виде двухатомных молекул
образование ими соединений с амфотерными свойствами
В ряду химических элементов
углерод →азот → кислород:
не изменяется число электронных слоев в атоме
уменьшается число электронов во внешнем электронном слое
уменьшается степень окисления в высших оксидах
усиливаются неметаллические свойства
увеличивается радиус атома
Для задания 15 дайте развернутый ответ.
Напишите уравнения реакций, с помощью которых можно осуществить следующие превращения:
Са →СаО →Са(ОН)2 →Са(НСО3)2→ СаСО3
3 вариант.
При выполнении заданий 1-13 отметьте одну цифру, которая соответствует номеру правильного ответа
Число энергетических уровней и число внешних электронов атома кремния соответственно равны
4,6 2)2,5 3) 3,4 4) 3,7
В сероуглероде химическая связь
Ионная 3) ковалентная неполярная
Металлическая 4) ковалентная полярная
Кристаллическая решетка алмаза
Молекулярная 3) атомная
Ионная 4) металлическая
Степень окисления углерода в CO2 равна
+4 2) -4 3) +2 4) - 2
Вещество СО – это
Кислотный оксид 3) основный оксид
Амфотерный оксид 4) несолеобразующий оксид
Среди перечисленных веществ кислой солью является
гидрид магния 3) гидроксид кальция
гидрокарбонат натрия 4) гидроксокарбонат меди (II)
Кремний вступает в реакцию с
оксидом магния 3) водородом
кислородом 4) гидроксидом алюминия
Углекислый газ в промышленности получают
взаимодействием карбоната кальция с соляной кислотой
разложением гидрокарбоната кальция
термическим разложением карбоната кальция
сжиганием угля
Оксид кремния взаимодействует с веществами
Mg, NaOH 3) CO2, C
H2O, C 4) Na2CO3, Cu
В результате кипячения водного раствора гидрокарбоната кальция в осадок выпадает
оксида кальция 3) карбид кальция
гидроксид кальция 4) карбонат кальция
В цепочке превращений C→ X→ Y→ CaCO3 вещества X и Y соответственно
CO, CO2 3) Al4C3, CH4
CO2, CO 4) CO2, Ca(HCO3)2
Вещества, с помощью которых можно осуществить превращения
Si →SiO2 →Na2SiO3→ H2SiO3
H2O, Na2O, HCl 3) MgO, NaOH, CO2 + H2O
O2, Na2CO3, HCl 4) O2, Na2SO4, CO2 +H2O
Стекло окрашивает в зеленый цвет
Оксид кобальта 3) оксид хрома (III)
Оксид кальция 4) оксид меди (II)
При выполнении заданий 14-15 из предложенного перечня ответов выберите три правильных и запишите в таблицу цифры.
Углекислый газ может реагировать
Азотом
Магнием
Раствором гидроксида натрия
Оксидом кальция
Раствором сульфата натрия
Оксидом фосфора (V)
Раствор карбоната натрия взаимодействует с
HCl
CuSO4
K2SO4
KOH
CaCl2
Fe(OH)3







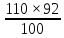 = 101,2 г
= 101,2 г 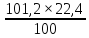 = 22,67 л
= 22,67 л



















