Н.А. Дашдемирова
Химия
Галогены – элементы VIIА группы
Рабочая тетрадь
9 класс
г.Зеленокумск, 2025 год.
Общая характеристика
на последней оболочке 7 электронов
двухатомные молекулы
максимальная степень окисления +7 (исключение F, максимальная 0 в F2)
минимальная степень окисления -1
промежуточная степень окисления: +1, +3, +5 (исключение F)
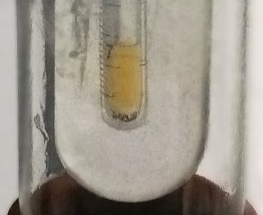
Физические свойства галогенов
Химические свойства галогенов

Галогены не реагирует с кислородом
I.Простые вещества 1.1. + неметаллы
F2 + H2 ⟶ 2HF
Cl2 + H2 ⟶ 2HCl
Вr2 + H2 ⟶_______
I2 + H2 _______
3F2+ S ⟶ SF6
Cl2 + S ⟶ _____ Вr2 + S ⟶_______
Cl2 + S ⟶ _____ Вr2 + S ⟶_______
Cl2 + P ⟶ _____ Вr2 + P ⟶_______
Cl2 + P ⟶ _____ Вr2 + P ⟶_______
3I2 + 2P ⟶2PI3
1.2. + металлы
3Cl2 + 2Fe ⟶ 2FeCl3 _____________________________
Cl2 + Cu ⟶ CuCl2 _____________________________
II.Сложные вещества
2.1. + вода
2F2 + H2O ⟶ OF2 + 2HF
Cl2 + H2O ⟶ HCl + HClO (бром аналогично)
______________________________
2.2. + щелочь (р. Диспропорционирование) :
Cl2 + NaOH ⟶ NaCl + NaClO + H2O (аналогично с Br2 и I2) (ОВР)
_____
3Cl2 + 6NaOH ⟶ 5NaCl + NaClO3 + 3H2O (при нагревании!). (ОВР)
2.3. Каждый вышестоящий галоген может вытеснить нижестоящий и серу.
Cl2 + 2KBr ⟶ Br2 + 2KCl.
Cl2 + 2KI ⟶ 2KCl + I2
Cl2 + KF ⟶ реакция не идет
Н2S + CI2 ⟶ 2HCI + S
K2S + Br2 ⟶_________________
Cl2 + HI ⟶ ______________
2.4. галогены не реагирует с оксидами и кислородсодержащими кислотами
Cl2 + SiO2 ⟶ реакция не протекает
Cl2 + H2SO4 ⟶ реакция не протекает
Исключение!!! CO + Cl2 ⟶ COCl2
2.5. + соль. Реакция не идет!
Cl2 + Na2SO4 ⟶ реакция не протекает;
Исключение!!! Cl2 + 2FeCl2 ⟶ 2FeCl3
Хлороводород. Соляная кислота.
НСI – это газ хорошо растворимый в воде. Водный раствор хлороводорода – это соляная кислота.
Получение хлороводорода
1. Концентрированная серной кислоты и хлорид натрия:
H2SO4(конц.) + NaCl(тверд.) → NaHSO4 + HCl↑
_________________________________________________
2. Галогеноводороды получают также прямым взаимодействием простых веществ:
Cl2 + H2 → 2HCl
Химические свойства соляной кислоты
1.1. + диссоциация
НСI ____________
1.2. + металл до водорода
Fe + 2HCl → FeCl2 + H2
Zn + HCl →______________
Al + HCl →____________
Cu + HCl →____________
1.3. + основный и амфотерный оксид
2HCl + CaO → CaCl2 + H2O (РИО)
6HCl + Al2O3 → 2AlCl3 + 3H2O (РИО)
НСI + CuO →_________________________ (РИО)
1.4. +основание
HCl + NaOH → NaCl + H2O (РИО)
2HCl + Cu(OH)2 → CuCl2 + 2H2O (РИО)
HCl + Zn(OH)2 → _______________________ (РИО)
1.5. + соль. Качественная реакция.
HCl + AgNO3 = AgCl↓ + HNO3 (РИО)
HBr + AgNO3 = AgBr↓ + HNO3 (РИО)
HI + AgNO3 = AgI↓ + HNO3 (РИО)

2HCl + CaCO3 → CaCl2 + 2H2O + CO2 (РИО)