Методическая разработка урока по физике, 11 класс.
Школа: МБОУ «СОШ имени А.М.Горького».
Учитель: Щепилина Татьяна Ивановна.

Тема урока: « СПЕКТРАЛЬНЫЙ АНАЛИЗ и его применение».
Цель урока:– обобщить знания учащихся по спектрам химических веществ и практическим применением спектрального анализа в астрофизике, медицине, металлургии и других отраслях.
Планируемые образовательные результаты
Предметные:
Сформированные понятия о видах спектров, применить при выполнении заданий из демонстрационного варианта ВПР- 2018 и КИМ ЭГЭ -2018, знать сущность, виды спектрального анализа и его практическое применении.
Метапредметные:
развивать представление о процессе научного познания, обеспечить развитие аналитических умений, применять знания в конкретных ситуациях.
Личностные:
воспитание и формирование коммуникативных качеств, прививать культуру умственного и практико-деятельностного труда, повышать практический познавательный интерес к предмету, профессиям.
Тип урока: обобщение и применение знаний (с использованием ИКТ).
Вид урока: урок -экскурсия с элементами практико- ориентированного и личностно-ориентированного обучения.
Оборудование:
Компьютеры, проектор, экран, презентации к уроку, видеоролики, Flash анимации, спектроскоп, спектрограф, оптико-эмульсионный спектрометр.
Демонстрации: наблюдение сплошного и линейчатых спектров при помощи спектроскопа, получение их фотографий.
План урока
I. Орг. момент.
II. Актуализация опорных знаний
III. Постановка учебной проблемы. Сообщение темы и цели урока.
IV. Повторение и обобщение материала
1. Спектроскоп, спектрограф и новейшие спектральные приборы (видеоролик)
2. Виды спектров
3. Спектральный анализ
- в медицине (сообщение будущего медика (презентация);
- в астрофизике (сообщение любителя астрономии);
- в металлургии (сообщение будущего химика-аналитика)
4. Применение спектрального анализа (презентация и экскурсия в лаборатории завода)
V. Закрепление и применение общеучебных навыков.
VI. Самостоятельная работа на индивидуальных компьютерах с последующей проверкой
VII. Домашнее задание.
VIII. Рефлексия, итоги урока. Оценки.
Ход урока
I. Организация класса. (1 мин)
Начнём урок со слов слайда 1(Презентация)

II. Актуализация опорных знаний (5 мин).
Вспомним предыдущие темы и ответим на вопросы.
Что такое свет? (поток электромагнитных волн с длиной волны 400 нм -800нм.)
Учитель: Когда начинает звучать струна? Начинает звучать после удара молоточка по струне.
Как в струне гитары нет звука, так и внутри атома нет света.


Как же излучается свет?
Электромагнитные волны излучаются при ускоренном движении частиц. Эти заряженные частицы входят в состав атомов, из которых состоит вещество. Для того, чтобы атом начал излучать, ему необходимо передать энергию. Излучая, атом теряет полученную энергию и для свечения вещества необходим приток энергии к атомам извне.
2. При каком условии электромагнитные волны излучаются? (Электромагнитные волны излучаются при ускоренном движении заряженных частиц)
3. Что необходимо сделать, чтобы атом излучал? (Для того чтобы атом начал излучал, ему необходимо передать определенную энергию)
4. Какие источники света вы знаете? (Естественные и искусственные, а они в свою очередь подразделяются на тепловые и люминесцирующие)
5. Кто открыл явление дисперсии и какой опыт со светом поставил этот учёный? (Ньютон. Направил на призму световой пучок малого поперечного сечения. Падая на стеклянную призму, он преломлялся и давал на стене изображение с радужным чередованием цветов. Радужную полоску он назвал спектром.)
6. Выполняя лабораторную работу по определению длины световой волны, вы использовали замечательное устройство. Как оно называется? (дифракционная решётка). Что вы получали с помощью дифракционной решётки (радужную полоску-спектр)
III. Постановка учебной проблемы. Сообщение темы и цели урока. (3 мин).
Тема урока: «Спектры, спектральный анализ и его применение»
Цель урока:– познакомиться со спектрами химических веществ и практическим применением спектрального анализа в астрофизике, металлургии, химии и других отраслях. (Слайд 3)
IV. Изучение нового материала. (18 мин)
1. Спектроскоп и спектрограф.
Для точного исследования спектров такие простые приспособления, как узкая щель, ограничивающая световой пучок, и призма, уже недостаточны. Необходимы приборы, дающие четкий спектр, т. е. приборы, хорошо разделяющие волны различной длины и не допускающие перекрытия отдельных участков спектра. Такие приборы называют спектральными аппаратами. Чаще всего основной частью спектрального аппарата является призма или дифракционная решетка. Рассмотрим схему устройства призменного спектрального аппарата. Исследуемое излучение поступает вначале в часть прибора, называемую коллиматором (Слайд 4,5).
Коллиматор представляет собой трубу, на одном конце которой имеется ширма с узкой щелью, а на другом - собирающая линза. Щель находится на фокусном расстоянии от линзы. Поэтому расходящийся световой пучок, попадающий на линзу из щели, выходит из нее параллельным пучком и падает на призму.
Так как разным частотам соответствуют различные показатели преломления, то из призмы выходят параллельные пучки, не совпадающие по направлению. Они падают на линзу. На фокусном расстоянии этой линзы располагается экран -матовое стекло или фотопластинка. Линза фокусирует параллельные пучки лучей на экране, и вместо одного изображения щели получается целый ряд изображений. Каждой частоте (узкому спектральному интервалу) соответствует свое изображение. Все эти изображения вместе и образуют спектр. Описанный прибор называется спектрографом. Если вместо второй линзы и экрана используется зрительная труба для визуального наблюдения спектров, то прибор называется спектроскопом. Призмы и другие детали спектральных аппаратов необязательно изготовляются из стекла. Вместо стекла применяются и такие прозрачные материалы, как кварц, каменная соль и др. Спектральный состав излучения веществ весьма разнообразен. Но, несмотря на это, все спектры, как показывает опыт, можно разделить на три типа.
2. Виды спектров испускания (Слайд 6). Непрерывный (сплошной) спектры.
Эксперимент №2 по наблюдению спектра при помощи спектроскопа 
Что представляют спектры, которые вы наблюдали? (Слушаем ответы учащихся). Каждый из спектров- это частокол цветных линий различной яркости, разделённых широкими тёмными полосами. Такие спектры называются линейчатыми. Наличие линейчатого спектра означает, что вещество излучает свет только вполне определенных длин волн (точнее, в определенных очень узких спектральных интервалах). Каждая из линий имеет конечную ширину.
Линейчатые спектры дают все вещества в газообразном атомарном (но не молекулярном) состоянии. В этом случае свет излучают атомы, которые практически не взаимодействуют друг с другом. Это самый фундаментальный, основной тип спектров. Изолированные атомы данного химического элемента излучают строго определенные длины волн. При увеличении плотности атомарного газа отдельные спектральные линии расширяются и, наконец при очень большой плотности газа, когда взаимодействие атомов становится существенным, эти линии перекрывают друг друга, образуя непрерывный спектр.
Линейчатые спектры представлены в учебнике рис.V,2,3,4 на цветной вклейке.
Полосатые спектры. (видеоролик к уроку)
Как вы думаете, чем отличаются спектры, которые излучаются атомами от молекулярных? (ответы учащихся)
Для наблюдения молекулярных спектров так же, как и для наблюдения линейчатых спектров, обычно используют свечение паров в пламени или свечение газового разряда. (Слайд 9)
С помощью очень хорошего спектрального аппарата можно обнаружить, что каждая полоса представляет собой совокупность большого числа очень тесно расположенных линий, разделённых тёмными промежутками. Это полосатый спектр. В отличие от линейчатых спектров полосатые спектры создаются не атомами, а молекулами, не связанными или слабо связанными друг с другом.

3. Спектры поглощения. (Слайд 10-11)
4. Спектральный анализ (видеоролик к уроку)
Линейчатые спектры играют особо важную роль, потому что их структура прямо связана со строением атома. Ведь эти спектры создаются атомами, не испытывающими внешних воздействий. Главное свойство линейчатых спектров состоит в том, что длины волн (или частоты) линейчатого спектра какого-либо вещества зависят только от свойств атомов этого вещества, но совершенно не зависят от способа возбуждения свечения атомов. Атомы любого химического элемента дают спектр, не похожий на спектры всех других элементов: они способны излучать строго-определенный набор длин волн.
На этом основан спектральный анализ - метод определения химического состава вещества по его спектру. Подобно отпечаткам пальцев у людей линейчатые спектры имеют неповторимую индивидуальность. Неповторимость узоров на коже пальца помогает часто найти преступника. Точно так же благодаря индивидуальности спектров каждого атома химического элемента, имеется возможность определить химический состав тела. С помощью спектрального анализа можно обнаружить данный элемент в составе сложного вещества. Это очень чувствительный метод. Количественное содержание элемента в исследуемом образце определяется путем сравнения интенсивности отдельных линий спектра этого элемента с интенсивностью линий другого химического элемента, количественное содержание которого в образце известно. Количественный анализ состава вещества по его спектру затруднен, так как яркость спектральных линий зависит не только от массы вещества, но и от способа возбуждения свечения. Так, при низких температурах многие спектральные линии вообще не появляются. Однако при соблюдении стандартных условий возбуждения свечения можно проводить и количественный спектральный анализ. В настоящее время определены спектры всех атомов и составлены таблицы спектров. С помощью спектрального анализа были открыты многие новые элементы: рубидий, цезий и др. Элементам часто давали названия в соответствии с цветом наиболее интенсивных линий спектра. Рубидий дает темно-красные, рубиновые линии. Слово цезий означает «небесно-голубой». Это цвет основных линий спектра цезия. (Слайд 12-13,)
5. Применение спектрального анализа.

Медицина (сообщение «будущего» медика с практическим обследованием желающих по спектрограммам).



Учащаяся рассказала о характеристике прибора и его применении в обследованиях на основе спектрального анализа.
Астрофизика (сообщение учащегося).
Астрофизика – раздел физики по определению химического состава звёзд, газовых облаков и т.д. и их физических характеристик: температуры, давления, скорости движения, магнитной индукции. С помощью спектрального анализа узнали химический состав Солнца и звезд, комет. Другие методы анализа здесь вообще невозможны. Оказалось, что звезды состоят из тех же самых химических элементов, которые имеются и на Земле. Любопытно, что гелий первоначально открыли на Солнце и лишь затем нашли в атмосфере Земли. Название этого элемента напоминает об истории его открытия: слово гелий означает в переводе «солнечный». Спектральный анализ можно производить не только по спектрам испускания, но и по спектрам поглощения. Именно линии поглощения в спектре Солнца и звезд позволяют исследовать химический состав этих небесных тел. Ярко светящаяся поверхность Солнца - фотосфера - дает непрерывный спектр. Солнечная атмосфера поглощает избирательно свет от фотосферы, что приводит к появлению линий поглощения на фоне непрерывного спектра фотосферы. Но и сама атмосфера Солнца излучает свет. Во время солнечных затмений, когда солнечный диск закрыт Луной, происходит обращение линий спектра. На месте линий поглощения в солнечном спектре вспыхивают линии излучения. Не так давно, астрономы при помощи спектральных анализов установили, что в центре некоторых галактик находятся чёрные дыры. Астрономы использовали телескоп Уильяма Гершеля и с его помощью нашли способ, который позволяет определить химический состав атмосферы планет вне солнечной системы, что, по мнению ученых, может помочь в поиске неземных цивилизаций.




Применение основных понятий и свойств звезд в заданиях по астрофизике ЕГЭ.


Спектральный анализ прогрессирует не только науку, но и производственную сферу человеческой деятельности.
Металлургия, машиностроение, атомная индустрия.
Благодаря сравнительной простоте и универсальности спектральный анализ является основным методом контроля состава вещества в металлургии, машиностроении, атомной индустрии. С помощью спектрального анализа определяют химический состав руд и минералов. Состав сложных, главным образом органических, смесей анализируется по их молекулярным спектрам. Криминалистика
Спектральный анализ широко применяют в криминалистике, для расследования улик, найденных на месте преступления. Также спектральный анализ в криминалистике хорошо помогает определять орудие убийства и вообще раскрывать некоторые частности преступления.
Выступление заведующего лабораторией спектрального анализа.

(Экскурсия в лабораторию).

V. Закрепление знаний (7 мин)
Вопросы по теме:
1. Какие виды спектров вы знаете?
2. Какой спектр называется спектром поглощения?
3. Что называют спектральным анализом?
4. Где применяется спектральный анализ?
5. Как называются приборы лаборатории для спектрального анализа и что вы наблюдали?
Задания на экране компьютеров. (слайд19-25 презентация)(выполнение заданий обучающего характера с последующей проверкой).

VI. Самостоятельная работа (контролирующего характера) (7 мин)
Выполняется тест по вариантам за компьютерами (приложение файл Excel «спектр тест 11 класс.xls» тест)
Ученики заносят свою фамилию. Нажимают «Пуск». Выполняют тест. Затем нажимают кнопку «Результат». Программа автоматически выполняет проверку, выставляет оценку и показывает правильный ответ. Ребята могут сравнить свой ответ с правильным.
| вариант 1 | | | | |
| А1. На рис. а, б, в приведены спектры излучения паров стронция, |
| неизвестною вещества и кальция. Можно утверждать, что в веществе (рис. б): |
| Ответы: | 1. | не содержится ни стронция, ни кальция; | 
| |
| | 2. | содержится кальций, но нет стронция; | |
| | 3. | содержатся и стронций, и кальций; | | |
| | 4. | содержится стронций, но нет кальция. | | |
| Вввод правильного ответа: | | | |
| A2. На рис. б приведен спектр поглощения неизвестного газа, а также спектры |
| поглощения атомов водорода (рис. а) и гелия (рис. в). Что можно сказать о | 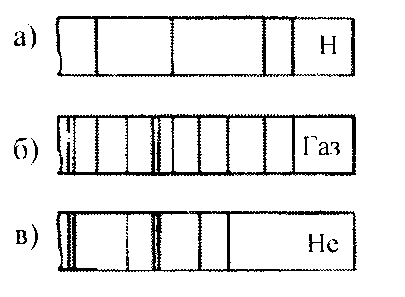
| |
| химическом составе газа? | | | |
| Ответы: | 1. | газ состоит только из атомов водорода; | |
| | 2. | газ состоит только из атомов гелия; | | |
| | 3. | газ состоит из атомов водорода и гелия; | |
| | 4. | газ состоит из атомов водорода, гелия и еще какого-то вещества. | | |
| Вввод правильного ответа: | | | |
| А3. Линейчатый спектр дают: | | |
| | | | | | | |
| Ответы: | 1. | жидкости в проходящем через них свете; | | |
| | 2. | нагретые твердые тела; | | |
| | 3. | атомы разреженного газа; | | |
| | 4. | нагретые до высокой температуры жидкости. | | |
| Вввод правильного ответа: | | | |
| А4. Какой спектр дает раскаленный добела металл? |
|
|
|
|
| |
| Ответы: | 1. | непрерывный; | | | |
| | 2. | линейчатый; | | | |
| | 3. | полосатый; | | | |
| | 4. | поглощения. | | | |
| Вввод правильного ответа: | | | |
| А5.Химики обнаружили, если в пламя газовой горелки (цвет пламени синий) бросить щепотку поваренной соли (NaCI), то цвет пламени на время приобретет яркую желтую окраску. Это послужило основой разработки метода |
| Ответы: | 1. | измерения температуры пламени; | | |
| | 2. | выделения натрия из поваренной соли; | |
| | 3. | спектрального анализа химического состава вещества |
| | 4. | нового горючего | | | |
| Вввод правильного ответа: | | | |
| А6.Известно, что криптон имеет в видимой части спектра излучения линии, соответствующие длинам волн 557 и 587 нм. В спектре излучения неизвестного газа обнаружены две линии, соответствующие 557 и 587 нм. Отсюда следует, что в неизвестном газе |
| Ответы: | 1. | криптон отсутствует; | | | |
| | 2. | присутствует только криптон; | | |
| | 3. | помимо криптона присутствует еще один элемент; |
| | 4. | помимо криптона присутствуют еще два или три элемента |
| Вввод правильного ответа: | |
| |
| А7. На рисунке приведены спектр поглощения неизвестного газа (в середине), спектры поглощения атомов водорода (вверху) и гелия (внизу). Что можно сказать о химическом составе газа? |
| Ответы: | 1. | Газ содержит атомы водорода и гелия; | |
| | 2. | Газ содержит атомы водорода, гелия и еще какого-то вещества; |
| | 3. | Газ содержит только атомы водорода; | |
| | 4. | Газ содержит только атомы гелия | 
| |
| Вввод правильного ответа: | |
| |
| |
|
|
|
|
| |
| |
|
|
|
|
| |
| |
|
|
|
|
| |
| |
|
|
|
|
| |
| | | | | | | |
VII. Итоги урока. Рефлексия. Оценки. (3 минуты)
VIII. Домашнее задание (1 минута)
1. § 81-83 изучить параграфы, уметь отвечать на вопросы в конце параграфов и выполнить тест с дополнительной информацией.
2. Подготовить сообщение: « История открытия спектрального анализа».






































