
Металлы I группы главной подгруппы – щелочные металлы.
Учитель химии Григорьева И.Н.

Электронное строение атомов
Li +3 )2)1
Na +11 )2)8)1
K +19 )2)8)8)1
Rb +37 )2)8)18)8)1
Cs + 55 )2)8)18)18)8)1
1. Радиус атома увеличивается
2. Энергия ионизации уменьшается
3. Химическая активность
( металлические свойства, восстановительные свойства) увеличиваются.
Me 0 – ē → Me +
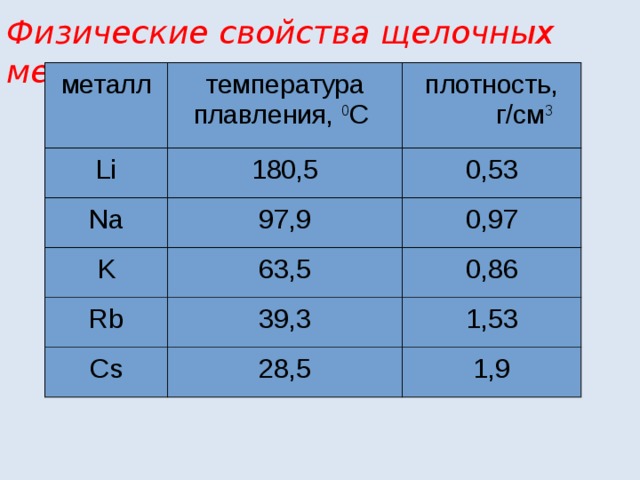
Физические свойства щелочных металлов
металл
температура плавления, 0 С
Li
плотность,
180,5
Na
г/см 3
0,53
97,9
K
Rb
0,97
63,5
0,86
39,3
Cs
1,53
28,5
1,9

ЛИТИЙ
КАЛИЙ
НАТРИЙ
Серебристо-белые металлы, мягкие, легкие, на воздухе окисляются, энергично взаимодействуют с водой.

Химические свойства щелочных металлов
- Взаимодействие с неметаллами
4 Li + O 2 = 2 Li 2 O оксид
2 Na + O 2 = Na 2 O 2 пероксид
K + O 2 = KO 2 надпероксид
2 Ме + Cl 2 = 2 MeCl хлорид
2 Me + S = Me 2 S сульфид
6 Me + N 2 = 2 Me 3 N нитрид
2 Me + H 2 = 2 MeH гидрид
2Me + 2HOH = 2MeOH + H 2 ↑

Соединения щелочных металлов
Оксиды - Ме 2 О – основные оксиды.
Химические свойства:
1. Ме 2 О + H 2 O = 2 MeOH
2. Ме 2 О + кислота = соль + H 2 O
3. Me 2 O + кислотный оксид = соль

Гидроксиды - МеОН – сильные основания, щелочи.
КОН - едкое кали
NaOH- едкий натр

Химические свойства щелочей:
- МеОН + кислота = соль + Н 2 О
2. МеОН + кислотный оксид = соль + Н 2 О
3. МеОН + соль = основание + соль
4. МеОН + амфотерный оксид = соль + Н 2 О (при t o )
5. МеОН + амфотерный гидроксид = соль + Н 2 О (при t o )
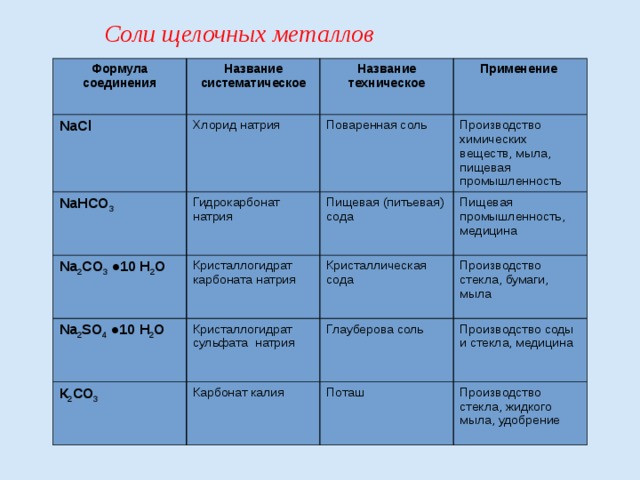
Соли щелочных металлов
Формула соединения
Название систематическое
NaCl
Название техническое
Хлорид натрия
NaHCO 3
Na 2 CO 3 ●10 H 2 O
Применение
Поваренная соль
Гидрокарбонат натрия
Na 2 SO 4 ●10 H 2 O
Кристаллогидрат карбоната натрия
Пищевая (питьевая) сода
Производство химических веществ, мыла, пищевая промышленность
Пищевая промышленность, медицина
Кристаллическая сода
Кристаллогидрат сульфата натрия
К 2 CO 3
Производство стекла, бумаги, мыла
Глауберова соль
Карбонат калия
Производство соды и стекла, медицина
Поташ
Производство стекла, жидкого мыла, удобрение

























