


Название кислороду Oxygenium
дал А . Лавуазье
C лат . о xygenium – “ рождающий кислоту ”
С греч . oxygenes – “ образующий кислоты ”

- Химический знак – О
- Относительная атомная масса : Ar = 16
- Изотопы кислорода – ( 99 ,75 %) , ,
- Строение атома : ( 8 p + + 8n 0 ) + 8
- Заряд ядра : ( +8)
- Электронная конфигурация атома : 1s 2 2s 2 2p 4
- Типичный неметалл . Сильный окислитель ( по электроотрицательности уступает лишь фтору )
- Валентные возможности : в соединениях обычно 2-х валентен , реже – 3-х , (4-х) валентен
- Возможные степени окисления : - 2 , - 1 , 0 , + 2 , (+4)
(наиболее характерные степени окисления : 0 , - 2 )

Английский ученый .
В 1774 году разложением
o ксида ртути ( II )
получил кислород
и
изучил его свойства
2 HgO = 2Hg + O 2 ↑
1733 - 1804

Шведский ученый .
В 1771 году провел опыты
по разложению
оксида ртути ( II ) ,
изучил свойства
образующегося газа .
Однако результаты
его исследований
были опубликованы
лишь в 177 7 году .
1742 - 1786

С целью проверки опытов
Шееле и Пристли
в 1774 году получил кислород ,
установил его природу и изучил
его способность соединяться
с фосфором и серой при горении
и металлами при обжиге .
Изучил состав атмосферного воздуха .
Создал кислородную теорию горения .
Совместно с Ж . Менье установил
сложный состав воды и получил
воду из кислорода и водорода .
2H 2 + O 2 = 2 H 2 O
Лавуазье показал , что процесс дыхания
подобен процессу горения .
1743 - 1794

1572 - 1633
Голландский алхимик и технолог .
Получил кислород примерно за 150 лет
до Пристли и Шееле при нагревании нитрата калия :
2К NO 3 = 2KNO 2 + O 2 ↑
Его открытие было засекречено , т . к . использование полученного газа предполагалось для дыхания людей на подводных лодках
Кислород занимает 1 место по распространенности элементов на Земле (по массе)
1 - кислород - 49
2 - алюминий - 7
3 - железо - 5
4 - кальций - 4
5 - натрий - 2
6 - калий - 2
7 - магний - 2
8 - водород - 1
9 - остальные - 2
10 - кремний - 26

- В земной коре – 49 %
- (атмосфера , литосфера , гидросфера)
- В воздухе – 20,9 % ( по объему )
- В воде
(в чистой воде – 88 , 8 % , в морской воде – 8 5,8 % )
- В песке , многих горных породах и минералах
- В составе органических соединений :
белков , жиров , углеводов и др .
- В организме человека – 62 %
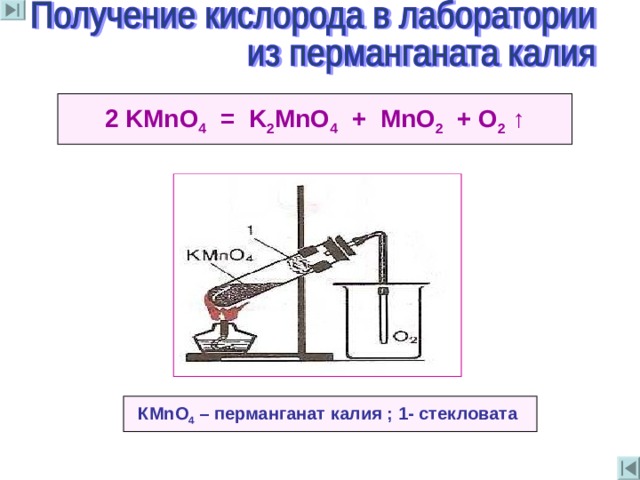
2 KMnO 4 = K 2 MnO 4 + MnO 2 + O 2 ↑
КМ nO 4 – перманганат калия ; 1- стекловата
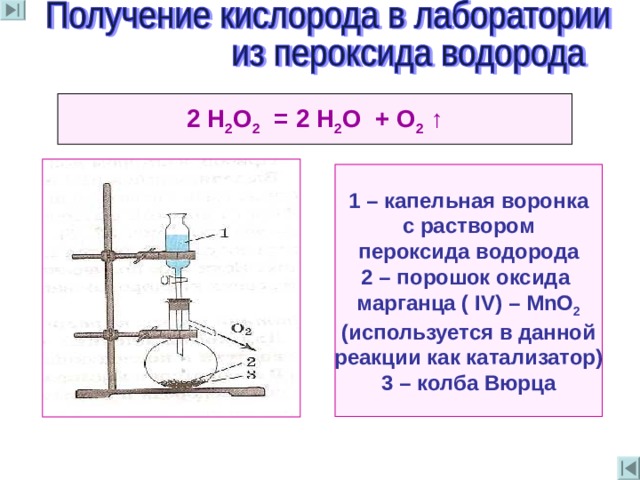
2 Н 2 O 2 = 2 Н 2 O + O 2 ↑
1 – капельная воронка
с раствором
пероксида водорода
2 – порошок оксида
марганца ( IV) – М nO 2
(используется в данной
реакции как катализатор)
3 – колба Вюрца
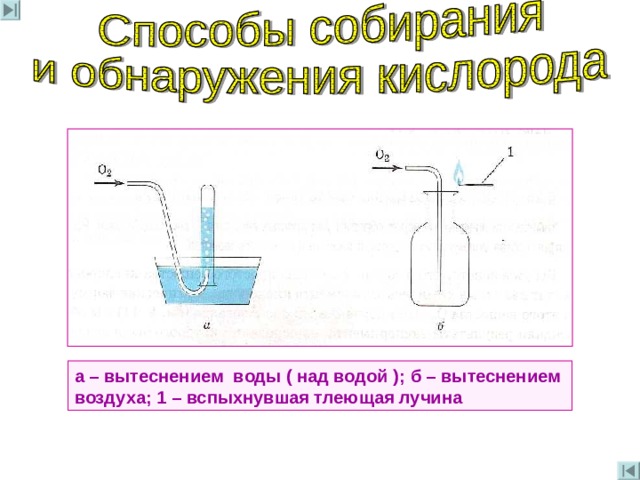
а – вытеснением воды ( над водой ) ; б – вытеснением воздуха ; 1 – вспыхнувшая тлеющая лучина

- Условия реакций – нагревание ( t )
2 КМ n О 4 = К 2 М n О 4 + М nO 2 + О 2 ↑
2КС l О 3 = 2КС l + О 2 ↑ 2Н gO = 2Hg + О 2 ↑
3 Р bO 2 = Р b 3 O 4 + О 2 ↑ 2К NO 3 = 2К NO 2 + О 2 ↑
- Условия реакции – присутствие катализатора ( K )
2Н 2 О 2 = 2Н 2 О + О 2 ↑ ( К – М n О 2 )
- Условия реакции – действие электрического тока ( )
(р . электролиза )
2Н 2 О = 2Н 2 ↑ + О 2 ↑

Кислород получают из воздуха
газовой ректификацией
- Воздух охлаждают примерно до – 200 0 С и под давлением сжижают
- Далее жидкий воздух подвергают перегонке
Жидкий азот испаряется при – 196 О С
( t кип . жидкого азота)
Жидкий кислород испаряется при – 183 О С
( t кип . жидкого кислорода)
- Газообразный кислород хранят в стальных баллонах , окрашенных в голубой цвет , под давлением 1 - 1 ,5 МПА

В 1774 г . А . Лавуазье доказал , что воздух – это смесь в основном двух газов - азота и кислорода
Кислород - 21 %
Азот - 78 %
Другие газы -1%
Примечание
К другим газам (1 %) относятся :
углекислый газ (0 ,03 %) ;
инертные газы
( в основном аргон - 0 ,93 % ) ;
водяные пары
Сжигание фосфора
под колоколом :
а – горение фосфора ;
б – уровень воды
поднялся на 1 / 5 объема

- Выдыхаемый человеком воздух
содержит ( в %, по объему)
1 – Кислород 16%
2 – Углекислый газ 4 %
3 – Остальное : азот ,
водяные пары и пр .

Отличается от лесного воздуха наличием выбросов : ( загрязняющих и ухудшающих воздух )
- от автотранспорта ( в Москве - 90% всех загрязнений)
- от котельных установок
- от промышленных предприятий
Автомашины выбрасывают в атмосферу :
углекислый газ СО 2 , сернистый газ SO 2 , оксиды азота NO и NO 2 , угарный газ СО , формальдегид НСОН , а также сажу
Металлургические предприятия выбрасывают в воздух :
сернистый газ , угарный газ , формальдегид , циановодород НС N
Алюминиевые заводы
фтороводород Н F
Целлюлозно – бумажныые комбинаты
сероводород , хлор , фенол C 6 H 5 OH и формальдегид
,

1 . Отношение к простым веществам
а) металлам
б) неметаллам
3 Fe + 2 О 2 ═ Fe 3 О 4 + Q
2Mg + O 2 ═ 2MgO + Q
С + О 2 ═ СО 2 + Q
S + О 2 ═ S О 2 + Q
4 Р + 5О 2 ═ 2Р 2 О 5 + Q
N 2 + О 2 2 NO Q
Реакции окисления , сопровождающиеся выделением теплоты и света ,
называют горением (вещества при этом воспламеняются)
t
t
( Fe О · Fe 2 О 3 )
t
t
t
Реакции окисления без горения
t
t
2Cu + O 2 ═ 2CuO + Q
Воспламенения меди не происходит
В реакциях окисления , как правило , образуются оксиды

2. Отношение к сложным веществам
- При полном сгорании углеводородов
образуются оксиды - углекислый газ и вода :
СН 4 + 2О 2 = СО 2 + 2Н 2 О + Q
метан
2С 2 Н 2 + 5О 2 = 4СО 2 + 2Н 2 О + Q
ацетилен
- При неполном сгорании углеводородов
(например , при недостатке кислорода О 2 ) образуются еще угарный газ СО и сажа С :
2 СН 4 + 3 О 2 = 2 СО + 4 Н 2 О + Q
СН 4 + О 2 = С + 2Н 2 О + Q
t
t
t
t

Условия для возникновения горения
Условия для прекращения горения
- Нагревание горючего вещества до температуры воспламенения
- Доступ кислорода
1 . Прекратить доступ к горючему веществу кислорода
2. Охладить вещество ниже температуры воспламенения

- Медленное окисление - химический процесс медленного взаимодействия вещества с кислородом без воспламенения вещества
- В ходе этого процесса теплота выделяется постепенно и вещество не нагревается до температуры воспламенения
Примеры :
- В процессах окисления (аэробного распада)
некоторых веществ пищи и продуктов обмена веществ в клетках и тканях живых организмов выделяется энергия , нужная организму
- В процессе гниения (окисления) навоза выделяется теплота и др .

- Реакции веществ с кислородом - реакции окисления .
Реакции окисления – составная часть окислительно –
– восстановительных реакций (ОВР)
- Преобладающая функция кислорода – окислительная .
При комнатной температуре О 2 – малоактивен , при высокой – сильный окислитель
- В реакциях окисления , как правило , получаются оксиды ( ЭО )
- Реакции окисления , сопровождающиеся воспламенением вещества , - реакции горения
- Реакции горения всегда – экзотермические реакции (+ Q )
- Медленное окисление - химический процесс медленного взаимодействия вещества с кислородом без воспламенения вещества

- Кислород входит в состав воды , которая составляет большую часть массы живых организмов и является внутренней средой жизнедеятельности клеток и тканей
- Кислород входит в состав биологически важных молекул , образующих живую материю
(белки , углеводы , жиры , гормоны , ферменты и др . )
- Кислород в виде простого вещества О 2 необходим как окислитель для протекания реакций , дающих клеткам необходимую для жизнедеятельности энергию

Кислород на Земле является
окислителем № 1,
т . к он обеспечивает протекание
таких важных процессов, как :
- дыхание всех живых организмов
- гниение органических масс
(помимо воздействия грибов и бактерий)

Кислород используют
В чистом виде :
- В металлургии – при получении чугуна , стали , цветных металлов ( для интенсификации окислительных процессов)
- Во многих химических производствах
- Как жидкий окислитель для ракет
- При резке и сварке металлов и сплавов
- В медицине - для приготовления лечебных водных и воздушных ванн , лечебных коктейлей
- В медицине - в кислородных подушках
В чистом виде и в составе смесей :
- На космических кораблях, подводных лодках в подводном плавании , на больших высотах
В составе воздуха :
- Для сжигания топлива (в двигателях автомобилей , тепловозов , теплоходов ; на тепловых электростанциях, на многих производствах и др . )

- Кислород расходуется в природе на процессы окисления
(дыхания , гниения , горения )
- Масса кислорода в воздухе пополняется в ходе процесса фотосинтеза
свет
6СО 2 + 6 Н 2 О = С 6 Н 12 О 6 + 6 О 2 ↑












































