Тема: Атомистическая теория. Масса и размер молекул. Тепловое движение частиц. Броуновское движение
Молекулярная физика – раздел физики, в котором изучаются физические свойства тел в различных агрегатных состояниях на основе рассмотрения их молекулярного строения, силы взаимодействия между частицами, образующими тела и характеры теплового движения этих частиц.
Молекулярная физика исходит из того, что любое тело – твердое, жидкое или газообразное – состоит из громадного числа молекул, которые находятся в беспорядочном движении, интенсивность которого зависит от температуры. При изучении молекулярной физики Вы познакомитесь со строением, структурой и свойствами некоторых материалов, с особенностями агрегатных изменений, рассмотрите зависимости количественных характеристик от физико-механических свойств веществ и их строения.
Молекулярная физика служит научной основой современного материаловедения, вакуумной технологии, порошковой металлургии, холодильной техники.
Представления о том, что все вещества состоят из мельчайших частиц - атомов, впервые появились в трудах древнегреческих ученых философов Левклиппа, Демокрита и Эпикура, живших V-III веках до нашей эры. Все явления природы они пытались объяснить движением этих невидимых частиц.
Учение о том, что все тела состоят из отдельных частиц – атомов, возникло в Древней Греции в IV в. до н.э. Основоположником атомистической теории был философ Демокрит.
Греческий философ Демокрит предположил, что все вещества состоят из невидимых человеческим глазом малых частиц - атомов. Он описал мир как систему атомов в пустоте, отвергая бесконечную делимость материи, постулируя не только бесконечность числа атомов во Вселенной, но и бесконечность их форм
Атомизм - учение о прерывистом, дискретном строение материи. До конца 19 века атомизм утверждал, что материя состоит из отдельных невидимых частиц - атомов.
Атомистическая теория (по-гречески atomos – неделимый) – вещество имеет дискретное строение, состоит из отдельных, разделенных пространственными промежутками частиц
Греческая форма атомизма плодотворно повлияла на развитие науки. Наиболее полно и в ясном изложении дошли до нас изустные и письменные работы древних греков.
Философы Левкипп и его ученик Демокрит (460-370 до н. э.) стали основателями атомистической теории. По учению Левкиппа материя состоит из отдельных частиц – атомов, находящихся в пустом пространстве, и слишком мелких, чтобы их можно было увидеть в отдельности. Атомы непрерывно движутся в пространстве и воздействуют друг на друга при помощи толчков и давления.
Более полно и стройно атомистическая теория была изложена великим древнегреческим философом-материалистом Демокритом.
Приведем некоторые принципиальные положения Демокрита, имеющие отношение к атомистической теории:
1. Ничто не возникает из ничего и ничего не переходит в ничто.
2. Материя состоит из бесконечного числа мельчайших, неделимых частиц – атомов.
3. Атомы вечны и неизменны, а все сложные тела, из них состоящие, изменчивы и преходящи.
4. Не существует ничего, кроме атомов и «чистого» пространства.
5. Атомы вечно движутся. Движение всегда присуще атомам и происходит в силу господства во Вселенной закона универсальной необходимости.
6. Атомы бесконечны по числу и бесконечно разнообразны по форме.
7. Во Вселенной существует бесконечное множество миров. Наш мир один из них.
8. Различие между вещами связано с различием их атомов по числу, величине, форме.
В 1913 г. Н. Бор (1885-1962) опубликовал серию статей «О строении атомов и молекул», открывших путь к атомной квантовой механике.
Многочисленные исследования, проведенные этими учеными позволили сформулировать основные положения молекулярно-кинетической теории – МКТ.
МКТ объясняет строение и свойства тел на основе закономерностей движения и взаимодействия молекул, из которых состоят тела.
В основе МКТ лежат три важных положения, подтвержденные экспериментально и теоретически.
Все тела состоят из мельчайших частиц – атомов, молекул, в состав которых входят еще более мелкие элементарные частицы (электроны, протоны, нейтроны). Строение любого вещества дискретно (прерывисто).
Атомы и молекулы вещества всегда находятся в непрерывном хаотическом движении.
Между частицами любого вещества существуют силы взаимодействия – притяжения и отталкивания. Природа этих сил электромагнитная.
Эти положения подтверждаются опытным путем.
Опытное обоснование 1 положения.
Все тела состоят из мельчайших частиц. Во-первых, об этом говорит возможность деления вещества (все тела можно разделить на части).
Наиболее ярким экспериментальным подтверждением представлений молекулярно-кинетической теории о беспорядочном движении атомов и молекул является броуновское движение.
Оно было открыто английским ботаником Р. Броуном (1827 г.). В 1827 году англ. ботаник Броун, изучая внутреннее строение растений с помощью микроскопа обнаружил, что частички твердого вещества в жидкой среде совершают непрерывное хаотическое движение.
Тепловое движение взвешенных в жидкости (или газе) частичек получило название броуновского движения.
Броуновские частицы движутся под влиянием беспорядочных ударов молекул. Из-за хаотического теплового движения молекул эти удары никогда не уравновешивают друг друга. В результате скорость броуновской частицы беспорядочно меняется по модулю и направлению, а ее траектория представляет собой сложную зигзагообразную кривую. Теория броуновского движения была создана А. Эйнштейном (1905 г.). Экспериментально теория Эйнштейна была подтверждена в опытах французского физика Ж. Перрена (1908–1911 гг.).
Причиной броуновского движения является непрерывное хаотическое движение молекул жидкости или газа, которые , беспорядочно ударяясь со всех сторон о частичку, приводят её в движение. Причина броуновского движения частицы в том, что удары молекул о неё не компенсируются. Значит броуновское движение является еще и опытным обоснованием 2 положения МКТ.
Непрерывное движение молекул любого вещества (твердого, жидкого, газообразного) подтверждается многочисленными опытами по диффузии.
Диффузией называют явление самопроизвольного проникновения одного вещества в другое.
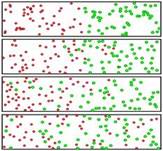
Рис. 1. Процесс диффузии в газах
Диффузия может происходить как в газах (мы можем наблюдать этот процесс, чувствуя распространение запахов), в жидкостях (смешивание окрашенной воды разных цветов) и даже в твёрдых телах (если на длительное время положить друг на друга очень гладкие листы стекла или металла, то невозможно будет отличить, где кончается один лист и начинается другой). Более того, существует также смешанная диффузия, то есть проникновение молекул газа в твёрдые и жидкие тела (иначе рыба в воде не могла бы дышать) .
Если пахучее вещество (духи) внести в помещение, то через некоторое время запах этого вещества распространится по всему помещению. Это свидетельствует о том, что молекулы одного вещества без воздействия внешних сил проникают в другое. Диффузия наблюдается и в жидкостях, и в твердых телах.
При изучении строения вещества было установлено, что между молекулами одновременно действуют силы притяжения и отталкивания, называемые молекулярными силами. Это силы электромагнитной природы.
Способность твердых тел сопротивляться растяжению, особые свойства поверхности жидкости приводят к выводу , что между молекулами действуют силы притяжения.
Малая сжимаемость весьма плотных газов и особенно жидкостей и твердых тел означает, что между молекулами существуют силы отталкивания.
Эти силы действуют одновременно. Если бы этого не было, то тела не были бы устойчивыми: либо разлетелись бы на частицы, либо слипались.
Межмолекулярное взаимодействие – это взаимодействие электрически нейтральных молекул и атомов.
Силы, действующие между двумя молекулами, зависят от расстояния между ними. Молекулы представляют собой сложные пространственные структуры, содержащие как положительные, так и отрицательные заряды. Если расстояние между молекулами достаточно велико, то преобладают силы межмолекулярного притяжения. На малых расстояниях преобладают силы отталкивания. Зависимости результирующей силы F и потенциальной энергии Ep взаимодействия между молекулами от расстояния между их центрами качественно изображены на рисунке. При некотором расстоянии r = r0 сила взаимодействия обращается в нуль. Это расстояние условно можно принять за диаметр молекулы. Потенциальная энергия взаимодействия при r = r0 минимальна. Чтобы удалить друг от друга две молекулы, находящиеся на расстоянии r0, нужно сообщить им дополнительную энергию E0. Величина E0 называется глубиной потенциальной ямы или энергией связи.
Между электронами одной молекулы и ядрами другой действуют силы притяжения, которые условно принято считать отрицательными (нижняя часть графика). Одновременно между электронами молекул и их ядрами действуют силы отталкивания, которые условно считают положительными (верхняя часть графика). На расстоянии равном размеру молекул результирующая сила равна нулю, т.е. силы притяжения уравновешивают силы отталкивания. Это наиболее устойчивое расположение молекул. При увеличении расстояния притяжение превосходит силу отталкивания, при уменьшении расстояния между молекулами – наоборот.
Атомы и молекулы взаимодействуют и значит обладают потенциальной энергией.
Атомы и молекулы находятся в постоянном движении, и значит, обладают кинетической энергией.
Масса и размеры молекул
Большинство веществ состоит из молекул, поэтому для объяснения свойств макроскопических объектов, объяснения и предсказания явлений важно знать основные характеристики молекул.
Молекулой называют наименьшую устойчивую частицу данного вещества, обладающую его основными химическими свойствами.
Молекула состоит из ещё более мелких частиц – атомов, которые в свою очередь , состоят из электронов и ядер.
Атомом называют наименьшую частицу данного химического элемента.
Размеры молекул очень малы.
Порядок величины диаметра молекулы 1*10-8 см = 1*10-10 м
Порядок величины объёма молекулы 1*10-20 м3
О том что размеры молекул малы можно судить и из опыта. В 1 л (м3 ) чистой воды разведем 1 м3 зеленых чернил, тете разбавим чернила в 1 000 000 раз. Увидим, что раствор имеет зеленую окраску и вместе с тем однороден. Это говорит о том, что даже при разбавлении в 1 000 000 раз в воде находится большое количество молекул красящего вещества. Этот опыт показывает, как малы размеры молекул.
В 1 см3 воды содержится 3,7*10-8 молекул.
Порядок величины массы молекул 1*10-23 г = 1*10-26кг
В молекулярной физике принято характеризовать массы атомов и молекул не их абсолютными значениями (в кг), а относительными безразмерными величинами относительной атомной массой и относительной молекулярной массой.
По международному соглашению в качестве единичной атомной массы m0 принимается 1/12 массы изотопа углерода 12С (m0С):
m0 =1/12 m0С=1,66 *10-27
Относительную молекулярную массу можно определить, если абсолютное значение массы молекулы (mмол в кг) разделить на единичную атомную массу.
M0 = mмол / 1/12 m0С
Относительная молекулярная (атомарная) масса вещества (из таблицы Менделеева)
714N Азот M0N = 14 M0N2 = 28
Относительное число атомов или молекул, содержащихся в веществе характеризуется физической величиной, называемой количеством вещества.
Количество вещества ע – это отношение числа молекул (атомов) N в донном макроскопическом теле к числу молекул в 0,012 кгуглерода NA
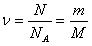
Количество вещества выражают в молях
Один моль – это количество вещества, в котором столько же молекул (атомов), сколько атомов содержится в 0,012 кг углерода.
Моль любого вещества содержит одинаковое число молекул. Это число называют постоянной Авогадро NA =6, 02 * 1023моль -1
Масса одного моля вещества называется молярной массой.
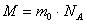
Число молекул в данной массе вещества: 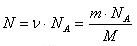
Масса вещества (любого количества вещества): 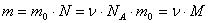
Определение молярной массы: