Tema:Demir.
Meýilnamasy:
1.Demiriň açylyşy.
2.Demiriň fiziki häsiýetleri.
3.Demiriň himiki häsiýetleri.
4.Demiriň izotoplary.
5.Demiriň alnyşy.
6.Demiriň ulanylyşy.
7.Demiriň elementiniň önümleri.
Demriň tebigy birleşmeleri. Demir Ýer gabygynda ýaýraýşy boýunça kislorod, kremniý we alýuminiý elementlerinden soň dördünji ýerde durýan elementdir (5,1%). Ýeriň merkezi demirden ybaratdyr. Kähalatlarda wulkanlaryň magmasynyň düzüminde demir erkin ýagdaýda hem duşýar. Meteoritleriň düzüminde hem demriň erkin halda duş gelýän halatlary bar. Demriň esasy minerallaryna magnetit-Fe3O4, gematit-Fe2O3, limonit--Fe2O3· nH2O, siderit-FeCO3 we beýlekiler degişlidirler.
Demriň alnyşy. Önümçilikde demir arassa görnüşde däl-de, eýsem, onuň splawlary bolan çoýun we polat görnüşinde öndürilýär(Seret: § 64. «Çoýnuň we poladyň öndürilişi»). Arassa demri almak üçin onuň duzlarynyň suw erginini elektroliz etmek ýa-da onuň oksidlerini wodorod bilen gaýtarmak usullaryndan peýdalanylýar:

Demriň fiziki häsiýetleri. Erkin halyndaky elementler kümüşsöw ak reňkli çalymtyl öwüşginli metaldyr. Arassa metal plastikdir, ýöne olaryň düzüminde garyndy bar bolsa, ol gaty we port bolýar. Howada durnuklydyr. Demir paramagnit häsiýetlidir. Ýöne, ol 769°C temperatura (Kýuriniň nokady) çenli gyzdyrylanda ol paramagnit häsiýetlerini ýitirýär we diamagnit häsiýetli ýagdaýa geçýär (paramagnit häsiýetli – magnite çekilmek, diamagnit häsiýetli – magnite çekilmezlik). Demriň şeýle öwrülişigi kristallik gözenekleriň öňküligine galmagy bilen geçýän faza öwrülişiginiň aýratyn bir görnüşidir. Şonda ýylylyk effektine gözegçilik edilmeýär. Demir we kobalt elementlerine polimorfizm häsiýeti mahsusdyr. Demriň dört hili C K0,10,016 0,160,16 0,4(ya da 40%)2- a-Fe, β-Fe, γ-Fe wle δ-Fe ýaly polimorf görnüşleri bar. Demir kyn suwuk hala geçýän metaldyr (1536°C).
Demriň himiki häsiýetleri. Demir howada 400–700°C-ä çenli durnukly, gaty maddadyr. Gury howada onuň üst ýüzünde mundan beýläk okislenmekden gorap saklaýan ýukajyk oksid gatlagy emele gelýär.
Demir sada we çylşyrymly maddalaryň birnäçesi bilen reagirleşýär.
Demir wodorod bilen kesgitli düzümli birleşmeler emele getirmeýär, ýöne wodorody köp mukdarda özüne siňdirýär. Demir kislorod bilen reagirleşýär:
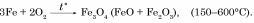
Çygly howada demir korroziýa sezewar bolýar (Seret: § 53. «Metallaryň korroziýasy we oňa garşy göreş çäreleri»).
Demir çygly howada otag temperaturasynda ýa-da gyzdyrylanda galogenler, kükürt we fosfor bilen reagirleşýär:

Adatdaky temperaturada demir suw bilen reagirleşmeýär. 800°C temperaturada demir suw bilen reagirleşýär. Şonda wodorod bölünip çykýar:
3Fe(gaty külke) + 4H2O(bug) → Fe3O4 + 4H2↑.
Demir metallaryň elektrohimiki güýjenme hatarynda sink bilen galaýynyň aralygynda ýerleşýär we howasyz şertlerde okislendiriji däl kislotalaryň gowşadylan erginleri bilen täsirleşende wodorody gysyp çykarýar:
Fe + 2HCl(gowş. ergin) → FeCl2 + H2↑;
Fe + H2SO4 (gowş. ergin) → FeSO4 + H2↑.
Demir kükürt kislotasynyň konsentrirlenen erginlerinde gyzdyrylanda hem demir (III) sulfaty emele gelýär. Demriň duzlary suw erginlerinde gidrolizleşendirler:
2Fe + 6H2SO4 → Fe2(SO4)3 + 3SO2↑ + 6H2O.
Okislendiriji kislotalaryň konsentrirlenen ergininde demir maşgalasynyň elementleri passiwleşýärler. Demir azot kislotasynyň gowşadylan ergini bilen reagirleşýär. Şonda demir (III) nitraty emele gelýär:
Fe + 4HNO3 (gowş. ergin) → Fe(NO3)3 + NO↑ + 2H2O.
Demriň möhüm birleşmeleri we olaryň häsiýetleri. Demriň FeO we Fe2O3 düzümli oksidleri, ol oksidlere gabat gelýän demir (II) gidroksidi Fe(OH)2 we demir (III) metagidroksidi FeO(OH) düzümli gidroksidleri hem-de duzlary ýaly möhüm birleşmeleri bardyr. Demriň oksidleriniň we gidroksidleriniň amfoter häsiýetleri bolup, olaryň şol häsiýetleri kislotalar we aşgarlar bilen reaksiýalarynda ýüze çykýar. Co, Ni elementlerinden tapawutlanyp, demriň +6 okislenme derejeli ýagdaýynda hem birleşmeleri bardyr.
Demir ionlarynyň hil reaksiýalary. Demriň birleşmeleriniň emele gelmek reaksiýalarynyň köpüsi Fe2+ we Fe3+ – ionlary açmak üçin hil derňewinde peýdalanylýar. Ol kompleks duzlaryň birleşmeleri demriň hil we mukdar derňewinde giňden peýdalanylýar. Erginde Fe3+ ionlarynyň bardygyny bilmek üçin onuň üstüne tiosianat NCS – ionlaryny saklaýan ergin goşulsa, reaksiýa netijesinde gyzyl gan reňkli demir (III) tiosianat birleşmesi emele gelýär (42-nji surat):

[Fe(H2O)5Cl]Cl2 + KNCS(ergin) E [Fe(H2O)5(NCS)]Cl2 + KCl.
sary reňkli birleşme ýiti gyzyl reňkli birleşme
Şonda tiosianat birleşmesiniň düzüminde çalşylan tiosianat ionlarynyň sany erginiň konsentrasiýasyna baglylykda birden bäşe çenli bolup bilýär. Çalşylan tiosianat ionlarynyň sanynyň artmagy bilen erginiň gyzyl reňki ýitileşýär. 4-nji we 5-nji ionlar suwuň molekulalary bilen çalşylanda ion birleşmesiniň zarýady üýtgeýär.
Demriň we onuň birleşmeleriniň magnit häsiýetleri (ferromagnetizm) maglumatlary ýatda saklamak üçin elektron tehnikasynda giňden peýdalanylýar. Şonuň ýaly-da, bedende demir ionlarynyň elektronlary geçirmekde uly ähmiýeti bardyr. Ol gandaky gemoglobiniň düzümine girip (43-nji surat), dem alşa gatnaşýar.