Просмотр содержимого документа
«Tema: Kaliy elementi.»
Tema: Kaliý.
Meýilnamasy:
1.Kaliýniň açylyşy.
2.Kaliýniň fiziki häsiýetleri.
3.Kaliýniň himiki häsiýetleri.
4.Kaliýniň izotoplary.
5.Kaliýniň alnyşy.
6.Kaliýniň ulanylyşy.
7.Kaliý elementiniň önümleri.
Kaliý tebigatda. K duzlar görnüşinde tebigatda giňden ýaýrandyrlar. Olardan KCl – silwin, KCl– silwinit, KCl •6H2O – karnallit ýaly minerallary mysal hökmünde görkezmek bolar. Bulardan başga-da, tebigatda Ýerüsti ösümlikleriň külünde K2CO3 bardyr.
Türkmenistanda kaliý elementleriniň duzlary birnäçe ýerlerde (Babahojada, Jebelde, Köýtendagda), glauber duzy (Garabogaz köl aýlagynda), silwinit (Garlykda, Köýtendagda, Garabilde) duş gelýär.
Kaliý elementiniň alnyşy. Kaliý elementi 1807-nji ýylda iňlis alymy G.Dewi tarapyndan açyldy.

Kaliý elementiniň fiziki häsiýetleri. Kaliý kümüşsöw ak reňkli ýumşak metaldyr. Ol suwuk hala geçmek temperaturasy litiý elementiniňkiden pesdir, ýagny aňsat suwuk hala geçýär. Ol howada durnuksyzdyr.

Kaliý elementiniň himiki häsiýetleri. Bu element himiki taýdan işjeň metaldyr. Ol himiki reaksiýalarda diňe gaýtaryjy häsiýetleri ýüze çykarýar. Birleşmelerinde bu element diňe bir walentlidir we okislenme derejesi diňe +1 bolup bilýär. Kaliý birnäçe sada we çylşyrymly maddalar bilen reagirleşýär Kaliý elementi kislorod bilen otag temperaturasynda reagirleşýär. Litiý elementinden tapawutlylykda, reaksiýa netijesinde kaliý nadperoksidi emele gelýär:
K + O2 (howa) → KO2 (ýanýar, garyndy K2O2).
Kaliý galogenler bilen reagirleşýär we netijede, bu elementiň galogenidleri emele gelýär:
2K + Cl2 → 2KCl.
Kaliý otag temperaturasynda suw bilen reagirleşýär. Şonda wodorod bölünip çykýar:
2K + 2H2O → 2KOH + H2.
Otag temperaturasynda kaliý duz kislotasynyň gowşadylan ergini bilen reagirleşýär. Şonda wodorod bölünip çykýar. Natriý elementinden tapawutlylykda, kaliý okislendiriji kislotalaryň gowşadylan ergini bilen reagirleşýär:
2K + 2HCl → 2KCl + H2.

Kaliý hloridi KCl tehniki ekinler üçin dökün hökmünde ulanylýar. Häzirki wagtda Garlyk(Magdanly) kaliý kärhanasynda bu duz öndürilýär.
Kaliý dökünleri ýetmezçilik edende ösümlikler kesellere çydamsyz hem-de hasyly durumsyz bolýar. Kaliý hloridini diňe tehniki ekinler(gowaça) üçin peýdalanyp bolýar. Ähli ekinler üçin ýaramly kaliý bu kaliý bolan döküni sulfatydyr Geljekde. Garlykda kaliý sulfatynyň önümçiligi
hem işe giriziler Kaliý sulfatyny aşakdaky usullar bilen öndürmek bolýar
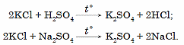
KNO3 mineral dökün hökmünde ulanylýar.