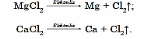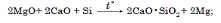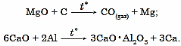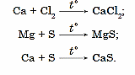Просмотр содержимого документа
«Tema: Kalsiý elementi.»
Tema:Kalsiý.
Meýilnamasy:
1.Kalsiýniň açylyşy.
2.Kalsiýniň fiziki häsiýetleri.
3.Kalsiýniň himiki häsiýetleri.
4.Kalsiýniň izotoplary.
5.Kalsiýniň alnyşy.
6.Kalsiýniň ulanylyşy.
7.Kalsiý elementiniň önümleri.
Kalsiý elementi tebigatda. Bu elementiň atomynda iki sany walent elektronlary bolup, olar s- orbitalda ýerleşendirler. Kalsiý elementiň emele getirýän birleşmeleriniň ösümlikleriň we haýwanlaryň ýaşaýşy üçin ähmiýeti örän uludyr(hlorofil).
Bu elementiň senagat ähmiýetli minerallarynyň birnäçesi(magnezit, dolomit, hek daşy, gips we beýlekiler) Türkmenistanda hem duş gelýärler.
Kalsiý elementiň suwda ereýän duzlary tebigy suwuň düzüminde duş gelýär we suwuň talhlygyny emele getirýär.
Kalsiý elementiň alnyşy. Kalsiý elementi 1808-nji ýylda iňlis alymy G. Dewi tarapyndan açyldy. Bu elementi almagyň iki dürli usullaryndan peýdalanylýar.
1. Kalsiý hloridleriniň rasplawyny elektroliz etmek usuly bilen alynýar:
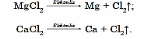
2. Kalsiý elementleri ýokary temperaturada(1200–2000 °C) olaryň birleşmelerinden gaýtaryjylary täsir etdirmek bilen hem alynýar:
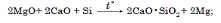
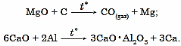
Şonda emele gelen gaz halyndaky metallar sowadylyp, kondensirlenýär. Reaksiýa inert gurşawda geçirilýär.
Kalsiý elementiň fiziki häsiýetleri. Kalsiý kümüşsöw ak reňkli, ýalpyldawuk metaldyr. Kalsiý howada durnuklydyr. Sebäbi bu metalyň üstünde ýukajyk we dykyz oksid gatlagy emele gelýär. Şol gatlak magniý metalyny mundan beýläk okislenmekden gorap saklaýar.
Kalsiý elementiniň himiki häsiýetleri. Kalsiý himiki taýdan işjeň metaldyr. Ol birleşmelerinde walentliligi hemişe II we okislenme derejesi+2-ä deň. Bu elementiň
Kalsiý we aşgar- ýer metallary kislorod bilen reagirleşýärler. Olar gyzdyrylanda howada ýanýarlar. Olar howada ýananda, adatça, nitritleriniň we oksidleriniň garyndysy emele gelýär:
2Mg + O2 → 2MgO (600–650°С);
2Ca + O2 → 2CaO (300°С).
Kalsiý we aşgar-ýer metallary gyzdyrylanda (150–400°С), galogenler we kükürt bilen hem reagirleşýärler. Şonda olaryň degişli elementler bilen birleşmeleri emele gelýär:
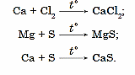
Kalsiý we aşgar- ýer metallary metallaryň elektrohimiki güýjenme hatarynda wodoroddan öňde ýerleşendirler. Şonuň üçin olar kislotalaryň gowşadylan erginlerinden wodorody gysyp çykarýarlar. Şonuň ýaly- da, magniý gyzdyrylanda we beýleki elementler otag temperaturasynda suwuň düzüminden hem wodorody gysyp çykarýarlar:
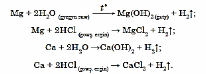
Kalsiý elementiniň RMgX we R2Mg düzümli magniorganiki birleşmeleri emele getirmek häsiýeti bar. Şol birleşmelerden Grinýaryň reaktiwiniň ähmiýeti uludyr. Grinýaryň reaktiwi birnäçe organiki maddalaryň sintezinde ulanylýar. Grinýaryň reaktiwi magniý bilen alkilgalogenidleriň dietilefirdäki ergininiň özara reaksiýasy netijesinde alynýar:
RX + Mg → RMgX;
C3H7Cl (suwuk) + Mg(gaty) → C3H7MgCl(gaty),
bu ýerde: R – uglewodorod radikaly; X – galogen atomy.
Kalsiý elementiniň CaO, Ca(OH)2, CaCO3 ýaly birleşmeleriniňgurluşyk materiallaryny we CaCl2, CaSO4 ýaly birleşmeleriniň bolsa, derman maddalary taýýarlamakda ähmiýeti uludyr. Senagatda hek daşyny gyzdyryp dargatmak usuly bilen alynýan kalsiý oksidinden hek suwy (Ca(OH)2), silikat kerpiji ýaly dürli hili gurluşyk materiallary öndürilýär