Tema: Wodorod.
Meýilnama:
1. Wodoroduň açylyşy.
2.Wodorodyň fiziki hasiýeti.
3.Wodorodyň himiki hasiýeti.
4.Wodorodyň izotoplary.
5.Wodorodyň alnyşy.
6.Wodorodyň ulanylyşy.
7.Wodorod elementiniň önümleri.
Wodorodyň omynyň himiki belgisi H, molekulýar formulasy H2, otnositel atom massasy 1, otnositel molekulýar massasy 2. Wodorod hemişelik 1 walentlilige eýedir. Erkin görnüşdäki wodorody ilkinji bolup, iňlis alymy G. Kawendiş 1766-njy ýylda aldy we oňa «Ýanyjy howa» diýip at berdi. Şol wagtda gaz halyndaky maddalara howa hökmünde garalýardy. Fransuz alymy A. Lawuazýe 1787-nji ýylda howanyň düzümini öwrendi we wodorody himiki element hökmünde kesgitledi. Ol bu elemente Hydrogenium diýip at berdi. «Hydrogenium» sözi türkmençä geçirilende, «Suw emele getiriji» diýmekligi aňladýar. Bu elementiň rusça ady wodorod bolup, ol hem şonuň ýaly manyny aňladýar. Ýer gabygynda wodorodyň massa paýy 1%-e deňdir. Beýleki himiki elementler bilen deňeşdirilende, Ýer gabygyndaky mukdary boýunça wodorod dokuzynjy orny eýeleýär. Emma älemde wodorod köp ýaýran elementdir. Ol Günüň, ýyldyzlaryň we olaryň arasyndaky giňişlikleriň esasy düzüm bölegidir. Günüň we ýyldyzlaryň üstünde temperatura örän ýokarydyr. Günüň üs tünde gyzgynlygyň derejesi 6000 °C-ä ýetýär. Şeýle ýokary temperaturalarda we kosmiki şöhleleriň täsirinde wodorod atomar görnüşde bolýar. Wodorodyň emele getirýän käbir möhüm birleşmeleri tebigatda giňden ýaýrandyr. Olara suwy, tebigy gazy, nebiti we ş.m. mysal getirmek bolar. Bu birleşmeler amaly taýdan möhüm ähmiýete eýedirler. Sada madda görnüşinde wodorod örän ujypsyz mukdarda atmosferanyň düzüminde (göwrümi boýunça 0,00005 %) duş gelýär. Ýöne, ýerden ýokaryk galdygyňça wodorodyň mukdary köpel ýär. Mysal üçin, 100 km belentlikde wodorodyň tutýan göwrümi 95 %-e ýetýär. Munuň sebäbi, esasan, ho- wa bilen deňeşdirilende, wodorodyň massasynyň örän ýeňildigi bilen baglanyşyklydyr. Fiziki häsiýeti. Wodorod reňksiz, yssyz we tagamsyz gazdyr. Wodorod howadan 14,5 esse ýeňildir. Wodorodyň eremek temperaturasy – 219,1°C-ä, gaýnamak temperaturasy – 252,6 °C-ä deňdir. Wodorod suwda örän ýaramaz ereýär. Suwuň 100 göwrüminde wodorodyň 2 göwrümi (20 °C-de) ereýär. Gaz halyndaky maddalaryň arasynda wodorod iň ýeňilidir. Şonuň üçin wodoroddan doldurylan ýukajyk bardalar (şarlar, sabyn köpürjikleri we ş.m.) ýeňillik bilen ýokaryk galýarlar. Wodorodyň möhüm aýratynlygy onuň metallarda gowy ereýänligidir. Mysal üçin, palladiniň bir göwrüminde wodorodyň 850 göwrümi ereýär. Wodorodyň metallarda eremegi çylşyrymly fiziki-himiki hadysadyr. Beýleki gazlaryň arasynda wodorod iň ýokary ýylylyk geçirijilige eýedir. Howa bilen deňeşdirilende, wodorodyň ýylylyk geçirijiligi 7 esse ýokarydyr. Munuň sebäbini şeýle düşündirmek bolar. Gaz halyndaky maddalaryň molekulalarynyň kinetik energiýasy temperatura baglydyr. Şol bir temperaturada molekulanyň massasy näçe kiçi bolsa, onuň hereket ediş tizligi şonça ýokarydyr. Islendik gazyň molekulasyndan ýeňil bolany üçin, wodorodyň molekulalarynyň hereket ediş tizligi ýokarydyr. Netijede, beýleki gazlaryň molekulalary bilen deňeşdirilende, wodorodyň molekulalary ýylylygy bir jisimden başga jisime çalt geçirýärler. Wodorodyň bu häsiýeti önümçilikde uly ähmiýete eýedir. Himiki häsiýeti. Adaty şertlerde wodorod diňe örän işjeň metallar we ftor bilen özara täsirleşýär. Beýleki metallar we metal däller bilen reaksiýa kesgitli şertlerde (temperatura, ýagtylyk we ş.m.) gatnaşýar. 1. Wodorodyň metallar bilen özara täsiri .Wodorod metallar bilen özara täsirleşip, MHn düzümli birleşmeleri emele getirýär. Reaksiýanyň deňlemeleri:
Ca + H2 → CaH2;
2Na + H2 → 2NaH;
2Li + H2 → 2LiH.
Wodorodyň metallar bilen birleşmeleri gidridler diýip atlandyrylýar. Meselem, CaH2 –kalsiniň gidridi, NaH – natriniň gidridi we ş.m. 2. Wodorodyň metal däller bilen özara täsiri Bu reaksiýalaryň netijesinde metal dälleriň wodorodly birleşmeleri emele gelýärler. Olar amaly taýdan möhüm ähmiýete eýedirler. Wodorodyň ftor we hlor bilen özara täsiri. Adaty şertlerde wodorod metal dällerden diňe ftor bilen reaksiýa gatnaşýar. Bu reaksiýa islendik temperaturada partlamak bilen geçýär. Reaksiýanyň deňlemesi:
H2 + F2 → 2HF (ftorlywodorod).
Otag temperaturasynda, ýagtylygyň ýok ýerinde wodorodyň hlor bilen reaksiýasy geçmeýär. Ýagtylygyň täsirinde bu reaksiýa örän çalt, partlama bilen bolup geçýär. Reaksiýanyň deňlemesi:
H2 + Cl2 → 2HCl (hlorlywodorod).
Hlorlywodorod suwda gowy ereýär. Hlorlywodorodyň suwdaky erginine duz kislotasy diýilýär. Wodorodyň kislorod bilen özara täsiri. Wodorod gyzdyrylanda, kislorod bilen ýeňil täsirleşip, suwy emele getirýär. Reaksiýanyň deňlemesi:
2H2 + O2 → 2H2O.
Bu reaksiýanyň netijesinde köp mukdarda ýylylyk bölünip çykýar. Reaksiýa ýokary tizlik bilen geçýär. Temperatura barha ýokarlanyp, 2025 °C-ä ýetýär. Tehnikada bu reaksiýa ýokary temperaturalary almak üçin ulanylýar. Wodorod arassa bolan ýagdaýynda kislorodda part laman ýanýar. Wodorodyň kislorod ýa-da howa bilen garyndysy gyzdyrylanda partlaýar. Wodorodyň iki göwrüminden we kislorodyň bir göwrüminden ybarat bolan garyndy has partlawukdyr. Şonuň üçin şeýle garyndy «Partlawuk gaz» diýip atlandyrylýar. Diýmek, wodorod bilen işe başlamazdan öňürti onuň arassalygyny barlamak zerurdyr. Wodorodyň arassalygyny barlamagyň usuly bilen «Wodorodyň alnyşy» atly temada tanşarys. Wodorodyň azot bilen özara täsiri. Wodorod bilen azotyň birleşmegi netijesinde ammiak NH3 emele gelýär. Bu reaksiýa ýörite şertlerde, ýagny ýokary temperaturada we basyşda geçýär. Ammiak himiýa senagaty we oba hojalygy üçin möhüm ähmiýetli maddadyr. Reaksiýanyň deňlemesi:
N2 + 3H2 ↔ 2NH3.
Wodorodyň kükürt bilen özara täsiri.Gyzdyrylyp eredilen kükürdiň üstünden wodorodyň akymy goýberilse, döwlen palak ýumurtganyň ysy geler. Munuň özi wodorodyň kükürt bilen birleşmesiniň, ýagny kükürtwodorodyň emele gelendigini aňladýar. Reaksiýanyň deňlemesi:
H2 + S → H2S (kükürtwodorod).
Kükürtwodorod gaz halyndaky maddadyr. Onuň suwdaky erginine kükürtwodorod kislotasy diýilýär. 3. Wodorodyň käbir metallaryň oksidleri bilen özara täsiri Käbir metallaryň oksidleri (CuO, Ag2O we ş.m.) bilen wodorodyň özara täsirleşmesiniň netijesinde metal bölünip çykýar. Reaksiýanyň deňlemesi: 
CuO + H2 =t Cu + H2O,
Ag2O + H2 =t 2Ag + H2O.
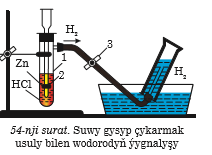
Reaksiýany şeýle geçirmek bolar. Içinde degişli metalyň oksidini saklaýan probirkany ýapgyt ýagdaýda ştatiwe berkitmeli. Metal bilen kislotany özara täsirleşdirip, wodorody almak üçin niýetlenen gapdaly turbajykly ikinji probirkany başga ştatiwe berkitmeli. Ikinji probirkada emele gelen wodorodyň barmagy üçin turbajygyň ujuny birinji probirkadaky metalyň oksidine golaý eltmeli (52-nji surat). Metalyň oksidini gyzdyryp, üstünden wodorodyň akymyny goýbermeli. Reaksiýanyň netijesinde iki sany madda, ýagny metal we suw emele geler. Senagatda käbir metallary almak üçin wodorodyň bu häsiýeti uly ähmiýete eýedir. Wodorodyň alnyşy. Wodorod tehnikada we himiýanyň tejribehanalarynda köp mukdarda ulanylýar. Şonuň üçin wodorody almagyň birnäçe usullary işlenilip düzülendir. Tejribehanada we senagatda wodorodyň alnyşynyň esasy usull aryna serediň. Metallaryň köpüsi kislotalar bilen reaksiýa gatnaş ýarlar. Reaksiýanyň netijesinde metallar kislotalaryň düzüminden wodorody gysyp çykarýarlar. Tejribehanada bu usul bilen wodorody almak üçin, adatça, sink bilen duz ýa-da kükürt kislotanyň özara täsiri ulanylýar. Reaksiýalaryň deňlemeleri:
2HCl + Zn → ZnCl2 + H2 ↑,
H2SO4 + Zn → ZnSO4 + H2 ↑.
Himiki taýdan işjeň metallara (Na, K, Ca we ş.m.) degişlidir. Bu reaksiýalarda metalyň kiçi bölejigini ulanmaly we seresap- lylygy pugta berjaý etmeli. Çünki reaksiýa örän güýçli geçýär, partlamanyň bolmagy mümkindir. Reaksiýada suwuň moleku- lasynyň düzümindäki wodorodyň bir atomyny metal gysyp çykarýar. Emele gelen OH-gidroksil topar diýip atlandyrylýar. Gidroksil toparlar metallar bilen birleşip, himiki birleşmeleriň aýratyn toparyny – esaslary emele getirý getirýärler. Esaslaryň özbaşdak agzalary gidroksidler diýip atlandyrylýar. Reaksiýalaryň deňlemeleri:
2Na + 2HOH → 2NaOH + H2 ↑,
Ca + 2HOH → Ca(OH)2 + H2 ↑.
Wodorody almak we ýygnamak üçin Kippiň abzaly we beýleki ýörite abzallar ulanylýar. Senagatda wodorody almak üçin onuň tebigy bir leşmeleri (tebigy gaz, ugurdaş gazlar, nebit gaýtadan işlenende emele gelýän gazlar, suw we ş.m.) ulanylýar. 1. Metandan wodorodyň alnyşy.Ýokary temperaturada metan bilen suw buglarynyň arasyndaky reaksiýanyň netijesinde wodorod alynýar:
CH4 + 2H2O = CO2 ↑+ 4H2↑.
2. Uglerod bilen suwuň özara täsirleşmesinden wodorodyň alnyşy.Bu usulda ilki bilen suw gazy alynýar. Onuň üçin güýçli gyzdyrylan koksuň üstünden 1000 °C-de suw bug lary goýberilýär:
C + H2O =t CO ↑ + H2 ↑.
Soňra emele gelen gazyň suw bugy bilen garyndysy 400- -450 °C-ä çenli gyzdyrylan katalizatoryň Fe2O3 üstünden goýberilýär. Netijede, CO bilen suw buglaryň arasynda özara täsirleşme geçýär:
CO + H2O + H2 =t CO2 + 2H2 ↑.
Uglerod bilen suwuň arasyndaky reaksiýany umu my görnüşde ýazmak hem bolar:
C + 2H2O =t CO2 + 2H2.
Bu ýagdaýda wodorod arassa görnüşde däl-de, eýsem, CO2 (kömürturşy gazy) bilen garyndy görnüşinde alynýar. Wodorody arassalamak üçin garyndy suwuň köp mukdarynyň içinden geçirilýär. Suwda ereýändigi sebäpli CO2 garyndynyň düzüminden aýrylýar. 3. Gidridlerden wodorodyň alnyşy .Geljekde wodorody awtomobilleriň ýangyjy hökmünde ulanmak göz öňünde tutulýar. Munuň üçin alynýan wodorodyň arassa bolmagy zerurdyr. Gidridleri dargatmak arassa wodorody almagyň usullarynyň biridir. Reaksiýanyň deňlemesi: TiH2 =t Ti + H2 ↑.
Gidridleriň suw bilen özara täsiri netijesinde hem wodorod alynýar. Meselem:
NaH + HOH → NaOH + H2↑.
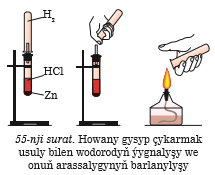
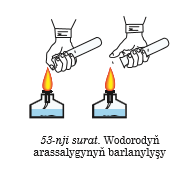
Wodorodyň alnyşynda onuň arassalygy örän wajypdyr. Dürli usullar arkaly alnan wodorod howa bilen haplanyp bilner.Bellenilip geçilişi ýaly, wodorod howa bilen partlawuk garyn- dyny emele getirýär. Şonuň üçin wodorod bilen işe başlamazdan öň onuň arassalygyny barlamak hökmandyr. Arassalygyny barlamak üçin probirkany wodoroddan dolduryp, ýakyp görmeli. Arassa wodorod kadaly ýanýar, arassa bolmadyk wodorod ýakylanda partlaýar.
Wodorodyň ulanylyşy.Wodorod tehnikada we önümçiligiň dürli pudaklarynda giň- den ulanylýar. Wodorodyň ulanylyşy onuň häsiýetlerine esaslanandyr. Wodorod ýananda köp mukdarda ýylylyk bölünip çykýar. Metallary kesmekde we kebşirlemekde onuň bu häsiýeti ulanyl- ýar. Suwuklandyrylan wodorod raketa ýangyjy hökmünde ulanylýar. Wodorod ýokary ýylylyk geçirijilige eýedir. Şonuň üçin wodorod kuwwatly maşynlarda artykmaç ýylylygy geçirmek üçin ulanylýar. Wodorodyň gaýnama temperaturasy örän pesdir. Munuň özi suwuk wodorody aşa pes temperaturany almak üçin ulanmaga mümkinçilik berýär. Geljekde wodorody awtomobil ýangyjy hökmünde ulanmak göz öňünde tutulýar. Onuň üçin wodorodyň alnyşynyň ykdysady taýdan amatly usuly ýola goýulmalydyr. Wodorod ýananda ýangyjyň beýleki görnüşlerinden tapawutlylykda atmosferany hapalamaýan madda, ýagny suw buglary emele gelýär. Şonuň üçin ýangyjyň beýleki görnüşleri bilen deňeşdirilende, wodorod ekologik taýdan arassadyr. Himiýa senagatynda käbir möhüm maddalary almak üçin wodorod giňden ulanylýar. Olara hlorlywodorod, ammiak, käbir reňkleýji maddalar we ş.m. degişlidir. Ammiak dökün önümçiligi üçin zerur maddadyr. Wodorod käbir metallary oksidleriniň düzüminden gaýtaryjy häsiýete eýedir. Wodorodyň bu häsiýeti metal lurgiýa senagatynda köpsanly reňkli metallary almak üçin uly ähmiýete eýedir. Azyk senagatynda wodorod suwuk ösümlik ýaglardan gaty ýaglary almak üçin ulanylýar. Muňa margariniň önümçiligini mysal getirmek bolar.