Вариант 1.
1. Что в периодической системе определяет порядковый номер элемента?(вес задания 1 балл)
А) Заряд ядра атома. Б) Число электронов в наружном слое атома.
В) Число электронных слоёв в атоме. Г) Число нейтронов в атоме.
2. Запишите определение понятия «атом». (вес задания 2балал)
3. Выберите ряд элементов, расположенных в порядке усиления металлических свойств:
А). Sr-Rb-K. Б). Na-K-Ca. В). Na-K-Cs. Г). Al-Mg-Be. (вес задания 2балла)
4. Установите соответствие. (вес задания 3балла)
А)1s22s22p1 1). Бор.
Б)1s22s1 2). Бром.
В)1s22s22p63s23p3 3). Фосфор.
Г)1s22s22p63s23p63d104s24p5 4). Литий.
5. Элемент Э с электронной формулой 1s22s22p63s23p63d104s24p1 образует высший оксид, соответствующий формуле: (вес задания 2балла)
А) Э2О. Б) Э2О3. В) ЭО2. Г) ЭО3.
6. Составьте электронную формулу элемента с порядковым номером 30 в Периодической системе. Сделайте вывод о принадлежности этого элемента к металлам или неметаллам. Запишите формулы его высшего оксида (вес задания 4балла)
7. По какой формуле определяется максимальное число электронов на энергетическом уровне?
а)N = A – Z; б) N = 2n2; в) N = 2n2 + 2; г) N = 2n2 – 2; д) N = 2n. (вес задания 1 балл)
8. У магния металлические свойства выражены: ( вес задания 1 балл)
1) слабее, чем у бериллия; 2) сильнее, чем у кальция;
3) сильнее, чем у алюминия; 4) сильнее, чем у натрия
9. Химические элементы расположены в порядке возрастания их атомного радиуса в ряду: ( вес задания 1 балл)
1) Be, B, C, N; 2) Rb, K, Na, Li; 3) O, S, Se, Te; 4) Mg, Al, Si, Р
10. Укажите форму р- электронных орбиталей: ( вес задания 1 балл)
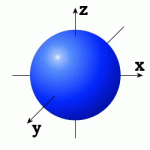


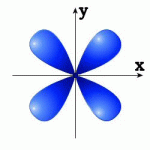
а) б) в) г)
Критерии оценивания
Оценка «5» - 16-18 баллов
Оценка «4» - 11-15 баллов
Оценка «3» - 7-10 баллов
Оценка «2» - менее 6 баллов
Вариант 2.
1. Что в периодической системе определяет номер группы (для элементов главных подгрупп)? ( вес задания 1 балл)
А) Заряд ядра атома. Б) Число электронов в наружном слое атома.
В) Число электронных слоёв в атоме. Г) Число нейтронов в атоме.
2. Запишите определение понятия «молекула». (вес задания 2балла)
3. Выберите ряд элементов, расположенных в порядке усиления металлических свойств:
А). K-Cs-Ba. Б). Al-Mg-Be. В). Be-Li-Al. Г).Ge-Sn-Pb. (вес задания 2балла)
4. Установите соответствие. (вес задания 3балла)
А) 1s22s22p3 1). Азот.
Б) 1s22s22p63s23p4 2). Кальций.
В) 1s22s22p63s23p2 3). Кремний.
Г) 1s22s22p63s23p64s2 4). Сера.
5. Элемент Э с электронной формулой 1s22s22p63s23p63d104s24p1 образует высший оксид, соответствующий формуле: (вес задания 2балла)
А) ЭО. Б) Э2О3. В) Э2О5. Г) ЭО3.
6. Составьте электронную формулу элемента с порядковым номером 32 в Периодической системе. Сделайте вывод о принадлежности этого элемента к металлам или неметаллам. Запишите формулы его высшего оксида . (вес задания 4балла)
7. Укажите форму s- электронных орбиталей: ( вес задания 1 балл)




а) б) в) г)
8. Число энергетических слоев и число электронов во внешнем энергетическом слое атомов мышьяка равны соответственно: ( вес задания 1 балл)
1) 4, 6; 2) 2, 5; 3) 3, 7; 4) 4, 5
9. Химические элементы расположены в порядке возрастания их атомного радиуса в ряду: ( вес задания 1 балл)
1) Be, B, C, N; 2) Rb, K, Na, Li; 3) O, S, Se, Te; 4) Mg, Al, Si, Р
10. Распределению электронов по энергетическим уровням в атоме элемента соответствует ряд чисел: 2, 8, 18, 6. В периодической системе в какой группе расположен этот элемент? ( вес задания 1 балл)
1) V A; 2) VI A; 3) V Б; 4) VI Б
Критерии оценивания
Оценка «5» - 16-18 баллов
Оценка «4» - 11-15 баллов
Оценка «3» - 7-10 баллов
Оценка «2» - менее 6 баллов
Вариант 3.
1. Что в периодической системе определяет номер периода? ( вес задания 1 балл)
А). Заряд ядра атома. Б). Число электронов в наружном слое атома.
В). Число электронных слоёв в атоме. Г). Число нейтронов в атоме.
2. Запишите формулировку периодического закона Д.И.Менделеева. (вес задания 2балла)
3. Выберите ряд элементов, расположенных в порядке усиления металлических свойств: (вес задания 2балла)
А). Mg-Ca-Zn. Б). Al-Mg-Ca. В). Sr-Rb-K. Г).Ge-Si-Sb.
4. Установите соответствие: (вес задания 3балла)
А) 1s22s2 1). Бериллий.
Б) 1s22s22p3 2). Натрий.
В) 1s22s22p63s1 3). Хлор.
Г) 1s22s22p63s23p5 4). Азот.
5. Элемент Э с электронной формулой 1s22s22p63s23p63d104s24p1 образует высший оксид, соответствующий формуле: (вес задания 2балла)
А) Э2О. Б) Э2О3. В) ЭО2. Г) ЭО3.
6. Составьте электронную формулу элемента с порядковым номером 38 в Периодической системе. Сделайте вывод о принадлежности этого элемента к металлам или неметаллам. Запишите формулы его высшего оксида . (вес задания 4балла)
7. Какая электронная формула соответствует атому элемента №33? ( вес задания 1 балл)
а) 1s22s22p63s23p64s23d94p4; б) 1s22s22p63s23p64s13d104p4;
в) 1s22s22p6323P64S24p3; г) 1s22s22p63s23p44s23d104p3; д) 1s22s22p63s23p63d84p5.
8. Чему равен заряд ядра атома (+Z), модель которого изображена на рисунке? ( вес задания 1 балл)
 + 13
+ 13
+ 15
+ 16
+ 18
9. Химические элементы расположены в порядке возрастания их атомного радиуса в ряду:
1) Be, B, C, N; 2) Rb, K, Na, Li; 3) O, S, Se, Te; 4) Mg, Al, Si, Р ( вес задания 1 балл)
10. Укажите форму s- электронных орбиталей: ( вес задания 1 балл)




а) б) в) г)
Критерии оценивания
Оценка «5» - 16-18 баллов
Оценка «4» - 11-15 баллов
Оценка «3» - 7-10 баллов
Оценка «2» - менее 6 баллов
Вариант 4.
1. Продолжите: Общее число электронов в атоме элемента определяют, используя Периодическую систему по номеру…( вес задания 1 балл)
А). Группы. Б). Периода. В). Ряда. Г). Порядковому.
2. Запишите современную формулировку периодического закона Д.И.Менделеева. (вес задания 2балла)
3. Выберите ряд элементов, расположенных в порядке усиления металлических свойств:
А). K-Rb-Sr. Б). Al-Mg-Be. В). Be-Li-Cs. Г).Ge-Sn-Sb. (вес задания 2балла)
4. Установите соответствие. (вес задания 3балла)
А).1s22s22p63s23p1 1). Алюминий.
Б).1s22s22p63s2 2). Калий.
В).1s22s22p63s23p63d104s24p4 3). Селен.
Г).1s22s22p63s23p64s1 4). Магний.
5. Элемент Э с электронной формулой 1s22s22p63s23p3 образует высший оксид, соответствующий формуле: (вес задания 2балла)
А). Э2О. Б). Э2О3. В). ЭО2. Г). Э2О5.
6. Составьте электронную формулу элемента с порядковым номером 34 в Периодической системе. Сделайте вывод о принадлежности этого элемента к металлам или неметаллам. Запишите формулы его высшего оксида(вес задания 4балла)
7. Укажите форму р- электронных орбиталей: ( вес задания 1 балл)




а) б) в) г)
8. Химический элемент расположен в IV периоде, I А группе. Распределению электронов в атоме этого элемента соответствует ряд чисел: ( вес задания 1 балл)
1) 2, 8, 8, 2; 2) 2, 8, 18, 1; 3) 2, 8, 8, 1; 4) 2, 8, 18, 2.
9. Химические элементы расположены в порядке возрастания их атомного радиуса в ряду: ( вес задания 1 балл)
1) Be, B, C, N; 2) Rb, K, Na, Li; 3) O, S, Se, Te; 4) Mg, Al, Si, Р.
10. Распределению электронов по энергетическим уровням в атоме элемента соответствует ряд чисел: 2, 8, 18, 6. В периодической системе в какой группе расположен этот элемент? ( вес задания 1 балл)
1) V A; 2) VI A; 3) V Б; 4) VI Б
Критерии оценивания
Оценка «5» - 16-18 баллов
Оценка «4» - 11-15 баллов
Оценка «3» - 7-10 баллов
Оценка «2» - менее 6 баллов











 + 13
+ 13

















