
ТУЗДАРДЫН ГИДРОЛИЗИ
Аткарган: Сүймөнкул Исматиллаев

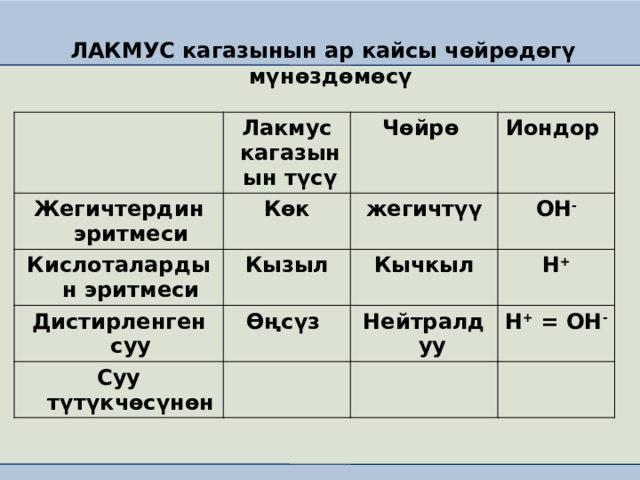
ЛАКМУС кагазынын ар кайсы чөйрөдөгү мүнөздөмөсү
Жегичтердин эритмеси
Лакмус кагазынын түсү
Көк
Кислоталардын эритмеси
Чөйрө
Иондор
жегичтүү
Кызыл
Дистирленген суу
ОН -
Өңсүз
Кычкыл
Суу түтүкчөсүнөн
Н +
Нейтралдуу
Н + = ОН -

Химиялык чөйрө
Суу өтө күчсүз электролит болуп саналат.
Электролиттик диссоциациянын натыйжасында суутектин катиону жана гидроксид-иондору (анионы):
Н 2 О Н+ + ОН¯

Суутектин катиону.
- 1 ē
+
Кычкылдануу
Суутектин катиону
Суутектин атому
1s² 1s°
Суутектин катиону эн жөнөкөй ядрого ээ ( p+ ; электрондук катмар бош ). Эркин протондо кыймыл жана кирүү жөндөмдүүлүгү өтө чоң.

Суутектик көрсөткүч
Суутектин катиондорунун Н + жана аниондордун ОН¯ концентрациясы таза сууда аябай аз: 1х10 7 моль/л (25°С).
Сууда Н+ и ОН¯ иондорунун саны бирдей;
Кислоталардын суудагы эритмелеринде Н+ көбүрөөк;
Жегичтердин суудагы эритме-леринде болсо – ОН¯ иондору көбүрөөк (кислоталардын жана негиздердин диссоциация-сынын эсебинен).
Эритменин чөйрөсүн суутектик көрсөткүч д.а..

Эритмесиндеги чөйрөлөрдүн түрлөрү
Суутектик көрсөткүч рН – эритмедеги суутектин иондорунун камтылышын мүнөздөөчү чоңдук.
Нейтралдуу
Кычкыл
Жегичтүү
Суутектин иондорунун саны гидроксид-иондордун санына тең болгон чөйрө
Суутектин иондорунун саны гидроксид-иондордун санынан көп болгон чөйрө
Суутектин иондорунун саны гидроксид-иондордун санынан аз болгон чөйрө

«ГИДРОЛИЗ» - грек сөзүнөн «гидро» - суу «лизис» - ажыроо
ГИДРОЛИЗ –
бул кээ бир туздар менен суунун арасындагы күчсүз электролиттин пайда болуусуна алып келген алмашуу реакциясы

Гидролиз
Бир эритмедеги кычкыл же жегичтүү чөйрөну пайда кылуучу, бирок чөкмөнүн же газдын бөлүүнүсү менен коштолбогон - туздар менен суунун өз ара аракеттенишүүсү кайталануучу гидролиз деп аталат (С.Аррениус, 1890 г.).
Бир эритмеде туз биринчи катиондорго жана аниондорго диссоциацияланат (кайталанбоочу реакция):
KNO 2 = K + + NO 2 ¯
ZnBr 2 = Zn 2+ + 2Br¯
Эгер пайда болгон иондордун арасында күчүз кислотанын аниондору бар болсо, анда гидролиз анион боюнча жүрөт
Эгер пайда болгон иондордун арасында күчүз жегичтердин катиондору бар болсо, анда гидролиз катион боюнча жүрөт

Анион боюнча гидролиз
Эгер пайда болгон иондордун арасында күчүз кислотанын аниондору бар болсо, анда гидролиз анион боюнча жүрөт . Бул анион жегичтуу чөйрөнү пайда кылуу менен суу менен аракеттенишип баштайт (кайталануучу реакция):
NO 2¯ + H 2 O HNO 2 + OH¯

Гидролизге күчсүз кислоталардын аниондору дуушар болот.
Мындай анион өзүнө эритмедеги суутектин катионун тартат, ал эми гидроксид – ион эркин (бош) калат:
NO 2 ¯ + H 2 O (H+; OH¯) HNO 2 + OH¯
Гидролизге дуушар болуучу аниондордун тизмеги:
CO 3 ²¯ SiO 4 ²¯ SO 3 ²¯ S²¯ ClO¯
CH3COO¯ NO 2 ¯ SeO 3 ²¯ Se²¯ BrO¯
CN¯ PO 4 ³¯ TeO 3 ²¯ Te²¯ F¯
Эске тут! Туздардын анион боюнча гидролизденүү даражасы гидролиздин продуктусунун диссоциациясынын даражасынан көз каранды:
Кислота канчалык күчсүз болсо, гидролизденүү даражасы ошончо чоң

Катион боюнча гидролиз
Күчсүз негиздердин катиондорун камтыган эригичтүү туздардын кайталануучу диссоциациясы:
NH 4 NO 3 = NH 4 + + NO 3 ¯
NH 4+ ионунун тескери гидролизи жүрөт
NH 4+ + H 2 O NH 3 х H 2 O + H +
Эритменин чөйрөсү күчсүз кычкыл .
Гидролизге дуушар болуучу аниондордун тизмеги:
Al 3+ Co 2+ Fe²+ Mn²+ Pb²+
Be²+ Cr³+ Fe³+ NH 4 + Zn²+
Cd²+ Cu²+ Hg²+ Ni²+

Жыйынтык (анион боюнча гидролиз):
күчтүү негиздин катиону жана күчсүз кислотанын анионунан пайда болгон туздар, гидролизге анион боюнча дууша болот жана жегичтүү чөйрөнү пайда кылат.
Жыйынтык (катион боюнча гидролиз):
күчсүз негиздин катиону жана күчтүү кислотанын анионунан пайда болгон туздар, гидролизге анион боюнча дууша болот жана жегичтүү чөйрөнү пайда кылат.
 кошуу Для подавления гидролизди азайтуу үчүн туздун эритмесин муздатуу же чөйрөнүн иондорун кошуу керек: F¯+ H 2 O +Q HF + OH¯( ) жегичти кошуу](https://static.multiurok.ru/multiurok/html/2020/04/14/s_5e95e6f991c24/img13.jpg)
Катион жана анион боюнча гидролиздин реакциялары кайталануучу жана тең салмактуулук абалын Ле – Шательенин принциби боюнча жылдырса болот:
- Гидролиздин даражасын көтөрүү үчүн туздун эритмесин суюлтурса же ысытса болот :
NH 4 + +H 2 O +Q NH 3 х H 2 O + H + [-Q]( )
кошуу
- Для подавления гидролизди азайтуу үчүн туздун эритмесин муздатуу же чөйрөнүн иондорун кошуу керек:
F¯+ H 2 O +Q HF + OH¯( )
жегичти кошуу

Алюминийдин хлоридинин гидролизинин механизми
H 2 O H + + OH -
AlCl 3 Al 3+ + 3Cl -
Al 3+ +3Cl - +HOH Al OH 2- + H + + 3Cl -
![Аммонийдин хлоридинин гидролизинин механизми AlCl 3 Al(OH) 3 HCl күчсүз негиз күчтүү кислота [OH] - + (кайсы бири күчтүү болсо ошол көп болот!) Кычкыл чөйрө](https://static.multiurok.ru/multiurok/html/2020/04/14/s_5e95e6f991c24/img15.jpg)
Аммонийдин хлоридинин гидролизинин механизми
AlCl 3
Al(OH) 3 HCl
күчсүз негиз күчтүү кислота
[OH] - +
(кайсы бири күчтүү болсо ошол көп болот!)
Кычкыл чөйрө

Туздардын гидролизинин реакциясынын теңдемесин жазуунун алгоритми
- Туздун курамын аныктоо, б.а. кандай негиз же кислота менен пайда болгонун аныктоо.
- Күчсүз электролиттин ионун алабыз жана суунун бир молекуласынын курамдык бөлүктөрү менен болгон аракеттенишүүсүн жазабыз; жыйынтыгында гидролиздин кыскача иондук теңдемесин алабыз.
- Кыскача иондук теңдеменин негизинде молекулярдык теңдемени алабыз.
Баштапкы заттар – туз жана суу . Гидролиздин продуктуларын жазуу үчүн пайда болгон иондорду, туздардын гидролиздин реакциясына катышпаган иондор менен байланыштырабыз .

Натрийдин карбонатынын гидролизинин схемасы
H 2 O H + + OH -
Na 2 CO 3 2Na + + CO 3 2-
2Na + +CO 3 2- +HOH HCO 3 - +2Na + + OH -
 [H] + (күчтүү ион көбүрөөк болот!) Жегичтүү чөйрө " width="640"
[H] + (күчтүү ион көбүрөөк болот!) Жегичтүү чөйрө " width="640"
Натрийдин карбонатынын гидролизинин схемасы
Na 2 CO 3
Na OH H 2 CO 3
күчтүү негиз күчсүз кислота
[OH] - [H] +
(күчтүү ион көбүрөөк болот!)
Жегичтүү чөйрө

Натрийдин хлоридинин гидролизинин схемасы
H 2 O H + + OH -
NaСl Na + + Cl -
Na + +Cl - +HOH Cl - + Na + + HOH
Берилген туз гидролизге кабылбайт.
![Натрийдин хлоридинин гидролизинин схемасы NaCl Na OH H Cl күчтүү кислота [OH] - = [H] + Нейтралдуу чөйрө](https://static.multiurok.ru/multiurok/html/2020/04/14/s_5e95e6f991c24/img20.jpg)
Натрийдин хлоридинин гидролизинин схемасы
NaCl
Na OH H Cl
күчтүү кислота
[OH] - = [H] +
Нейтралдуу чөйрө

Сабактын аягы
Баарынарга рахмат!




















 кошуу Для подавления гидролизди азайтуу үчүн туздун эритмесин муздатуу же чөйрөнүн иондорун кошуу керек: F¯+ H 2 O +Q HF + OH¯( ) жегичти кошуу](https://static.multiurok.ru/multiurok/html/2020/04/14/s_5e95e6f991c24/img13.jpg)

![Аммонийдин хлоридинин гидролизинин механизми AlCl 3 Al(OH) 3 HCl күчсүз негиз күчтүү кислота [OH] - + (кайсы бири күчтүү болсо ошол көп болот!) Кычкыл чөйрө](https://static.multiurok.ru/multiurok/html/2020/04/14/s_5e95e6f991c24/img15.jpg)


 [H] + (күчтүү ион көбүрөөк болот!) Жегичтүү чөйрө " width="640"
[H] + (күчтүү ион көбүрөөк болот!) Жегичтүү чөйрө " width="640"

![Натрийдин хлоридинин гидролизинин схемасы NaCl Na OH H Cl күчтүү кислота [OH] - = [H] + Нейтралдуу чөйрө](https://static.multiurok.ru/multiurok/html/2020/04/14/s_5e95e6f991c24/img20.jpg)











