Раздел 3. основы физиологии клетки
При изучении этого раздела Вы узнаете:
сущность понятий обмен веществ, ассимиляция, диссимиляция;
основные этапы обмена веществ;
сущность реакций энергетического обмена;
этапы и механизм процессов фотосинтеза;
сущность процессов биосинтеза белка;
механизм процессов транскрипции и трансляции;
этапы жизненного цикла клетки;
сущность процессов роста и размножения клеток;
сущность процессов митоза и его стадий.
ИНФОРМАЦИОННЫЙ БЛОК 3.1. Клеточный метаболизм.
Метаболизм, или обмен веществ - характерный признак всех живых существ. Без обмена веществ жизнь невозможна. В организме, его органах, тканях, клетках непрерывно образуются, разрушаются и обновляются их структурные компоненты. Для образования новых клеток, для работы всех органов и систем органов, а также для совершения физической работы организму нужна энергия. Эта энергия образуется в процессе обмена веществ. Источником энергии служат питательные вещества, поступающие с пищей, а у фототрофных организмов источником энергии является свет - энергия Солнца.
Непрерывность обмена веществ и энергии возможна потому, что организм существует как открытая система. Это значит, что с пищей, водой, при газообмене из внешней среды в организм поступают различные соединения. По химическому составу они отличаются от внутренней среды данного организма. В организме эти соединения подвергаются изменениям и превращениям, и, в конце концов, становятся тождественными химическим веществам организма и входят в его морфологические структуры. Через определенный период усвоенные вещества подвергаются разрушению, выделяя скрытую в них энергию, а конечные продукты расщепления выводятся во внешнюю среду. При этом разрушенную молекулу сразу же замещает новая, не нарушая структурной целостности организма. Следовательно, организм - не статичная, а открытая поточная система.
Поток вещества и энергии, наблюдаемый в организме, обусловливает самообновление и самовоспроизведение, которые осуществляются на всех уровнях организации - от молекулярного до организменного.
Обмен веществ складывается из двух неразрывных и взаимосвязанных процессов - ассимиляции (или анаболизма) и диссимиляции (или катаболизма).
Ассимиляция или анаболизм - это реакции биологического синтеза сложных молекул органических соединений, специфичных для данного организма, из более простых компонентов, поступающих в клетки. Например, из аминокислот в анаболических процессах синтезируются пептиды или белки. Анаболизм является основой для построения новых клеточных структур, для формирования новых тканей в процессе роста и поскольку за счет данных реакций идет образование тканевых и клеточных структур – эти реакции называются также пластическим обменом.
Энергия для анаболических реакций образуется в реакциях диссимиляции или катаболизма, при которых происходит расщепление молекул сложных органических соединений с выделением энергии. К реакциям катаболизма относят расщепление белков до аминокислот, жиров до жирных кислот и глицерина, сахаров до глюкозы, а также и реакции расщепления мономеров до неорганических соединений (углекислого газа, мочевины, воды и др.) Большинство перечисленных реакций идет с выделением энергии, заключенной в химических связях, поэтому эти реакции составляют часть энергетического обмена. Конечные продукты катаболизма не могут быть окислены в организме и удаляются из него.
Соотношение процессов катаболизма и анаболизма определяет три различных состояния: динамическое равновесие, рост и частичное разрушение структур организма. При динамическом равновесии анаболизм и катаболизм уравновешены. Это норма для взрослого зрелого и здорового организма. Преобладание анаболизма ведет к росту, это состояние является нормой для детей. Преобладание катаболизма приводит к уменьшению массы, истощению организма. Это лежит в основе старения или характерно для болезни.
Обмен веществ состоит из трех этапов: подготовительного, клеточного и этапа выделения.
Клеточный этап начинается с поступления в клетку из тканевой жидкости мономеров: аминокислот, глюкозы, жирных кислот и глицерина и др. Эти вещества в клетку поступают путем активного транспорта - с помощью ферментов клеточной мембраны (см. раздел 2). В клетке из аминокислот образуется необходимый клетке белок. Этот процесс происходит на рибосомах (как свободных, так и связанных с ЭПС). Синтезированные белки клетки являются или структурными - из них строятся клеточные органеллы, или ферментами, которые обеспечивают все процессы жизнедеятельности, а также выполняют другие функции. Часть аминокислот подвергается расщеплению, конечными продуктами которого являются CO2, H2O NH3. Из мономеров на каналах гладкой ЭПС синтезируются собственные жиры (фосфолипиды, стероиды и др.) и углеводы. В ядре идут постоянно процессы репликации и транскрипции - синтеза ДНК и РНК.
Для всех процессов жизнедеятельности необходима энергия, которая образуется в процессе реакций катаболизма.
Процессы ассимиляции и диссимиляции связаны не только структурно, т.е. осуществляются в клеточных органеллах, но и биохимически: продукты реакций ассимиляции могут быть использованы клеткой для энергетического обмена. Например, если в клетку не поступают углеводы и жиры для энергетического обмена, клетка расщепляет структурные белки.
3.2. Ферментативный характер реакций обмена
Большую роль в протекании реакций внутриклеточного обмена играют многочисленные клеточные ферменты. Ферменты - это высокоэффективные биологические катализаторы, белковые молекулы, синтезируемые живыми клетками. В каждой клетки имеются сотни и тысячи различных ферментов. С их помощью осуществляются разнообразные химические реакции, лежащие в основе процессов жизнедеятельности.
Ферменты обычно состоят из нескольких полипептидных цепей и обладают четвертичной структурой. Кроме того, ферменты могут иметь в своем составе и небелковые компоненты. Белковая часть называется апоферментом, а небелковая - кофактором (если это простое неорганическое вещество) или коферментом (если это сложное органическое соединение). Предшественниками многих коферментов являются витамины. Апофермент и кофермент составляют единый каталитически активный комплекс - голофермент.
Биологические катализаторы имеют несколько общих свойств:
по структуре они - глобулярные белки;
увеличивают скорость реакции, но сами в этой реакции не расходуются;
присутствие фермента никак не влияет на конечный продукт реакции;
очень малая концентрация фермента оказывает специфическое действие в отношении большого количества субстрата за малый промежуток времени;
ферменты обладают специфичностью.
Виды специфичности: абсолютная - один фермент катализирует превращения только одного субстрата; относительная - один фермент катализирует превращения нескольких, сходных по химическому строению, веществ; специфичность пути превращения - фермент катализирует только определенный путь превращения своего субстрата, то есть определенную химическую реакции; и стереоспецифичность - фермент обеспечивает превращения одного из стереоизомеров (например, или цис-, или транс-изомера).
Активность ферментов и скорость ферментативной реакции зависит от многих факторов.
Во-первых, от концентрации фермента - при возрастании концентрации фермента скорость реакции возрастает прямо пропорционально увеличению концентрации фермента. Во вторых, от концентрации субстрата - при ее увеличении сначала скорость возрастает прямо пропорционально увеличению концентрации, а затем этот процесс замедляется, и при достижении определенной концентрации субстрата скорость реакции больше не возрастает и остается постоянной.
Активность фермента зависит также от температуры - при повышении температуры на каждые 10° скорость возрастает примерно в 2 раза, но до определенного предела. Температура, обеспечивающая наибольшую скорость реакции и активность фермента, называется оптимальной. При дальнейшем повышении температуры до 39-50°С практически все ферменты денатурируют и теряют свойства. Ферментативная активность зависит и от реакции среды (pH). То значение pH, при котором скорость химической реакции максимальна, считается оптимальным для данного фермента. Например, для ферментов крови оптимальное значение pH=7,36.
В контакт с субстратом вступает лишь небольшая часть молекулы фермента, называемая активным центром. Форма активного центра фермента динамически соответствует субстрату, что можно сравнить с перчаткой, меняющей свою форму при надевании на руку. Активный центр состоит из двух участков - контактного и каталитического. Первый отвечает за связывание фермента с молекулой субстрата, а второй за протекание собственно катализа.
Известны различные соединения, которые могут тормозить химические реакции. Такие соединения называются ингибиторами. Ингибирование может быть обратимым и необратимым. В первом случае ингибитор непрочно связан с ферментом и может отделяться. Во втором случае ингибитор прочно связывается с ферментом, активность которого полностью утрачивается.
3.3. Фотосинтез
Жизнедеятельность всех организмов должна обеспечиваться энергией. Энергия эта поступает из окружающей среды. Первичным источником энергии для всего живого служит солнечный свет. Эта энергия улавливается растениями в процессе фотосинтеза и превращается в химическую энергию, которая сохраняется в запасных веществах, образующихся при фотосинтезе.
Впервые решить проблему питания растений попытался Я. Б. ван Гельмот более 300 лет назад. Он выращивал дерево в горшке, и только поливая его, добился значительного увеличения массы, однако масса почвы уменьшилась лишь на несколько грамм. Д. Пристли 17 августа 1771 года провел целую серию опытов по «улучшению» воздуха растениями. Детально изучил процессы фотосинтеза К. А.Тимирязев. В своей работе «Солнце, жизнь и хлорофилл» он не только описал механизм реакций фотосинтеза, но и показал значение зеленых растений для жизни на Земле.
Фотосинтез осуществляется различными группами автотрофных организмов - высшими зелеными растениями, многоклеточными зелеными, бурыми и красными водорослями, некоторыми одноклеточными эукариотами (например, эвгленой зеленой, хламидомонадой и другими) и бактериями. Фотосинтез - это единственный процесс в природе, который идет с запасанием химической энергии и обеспечивает доступным источником ее все существующие в природе организмы. Биологическая роль фотосинтеза огромна. В течение года в результате фотосинтеза на Земле усваивается около 200 млрд. тонн углекислого газа, образуется около 100 млрд. тонн органического вещества и выделяется около 145 млрд. тонн молекулярного кислорода. Фотосинтез, осуществляемый первыми фотосинтезирующими организмами (сине-зелеными водорослями), вызвал появление свободного кислорода в атмосфере и создал озоновый экран, обеспечив, таким образом, условия для биологической эволюции.
У всех фотосинтезирующих организмов, за исключением бактерий, процесс фотосинтеза представляет собой образование органических веществ из углекислого газа и воды с использованием энергии солнечного света, сопровождающийся выделением кислорода.
С
hν
уммарное уравнение фотосинтеза для высших растений и водорослей можно записать в следующем виде:
nH2O + nCO2 → (CH2O)n + nO2,
где hν - квант света, и если n = 6, то это соответствует образованию в качестве продукта фотосинтеза молекулы моносахарида глюкозы - C6H12O6.
Фотосинтезирующие бактерии также синтезируют на свету органические вещества из углекислого газа, однако, вместо воды они используют другие доноры водорода - неорганические (например, сероводород) или органические (например, молочная кислота) соединения.
Для фотосинтезирующих бактерий, донором водорода у которых служит сероводород (например, зеленые серные бактерии), общее уравнение фотосинтеза выглядит следующим образом:
hν
2nH2S + nСO2 → (CH2O)n + nH2O + 2nS,
где (CH2O) - фрагмент молекулы углевода.
Во всех случаях при фотосинтезе преобразование световой энергии в химическую включает окислительно-восстановительный перенос электронов и сопряженное с ним образование АТФ.
Фотосинтетические процессы у высших растений и некоторых водорослей осуществляется в особых клеточных органеллах - хлоропластах, строение которых рассматривалось в разделе 2.
Фотосинтезирующие бактерии содержат другие специализированные образования - хроматофоры, в мембранах которых также локализованы пигменты и специфические ферменты для реакций фотосинтеза.
Фотосинтез включает в себя три основных принципиально различных типа химических реакций: фотофизические, фотохимические и ферментативные. Первые два типа реакций входят в так называемую световую фазу фотосинтеза, для осуществления которой необходим свет, а последние реакции составляют темновую фазу фотосинтеза, свет для которой не нужен.
Реакции световой фазы фотосинтеза протекают на внутренних мембранах хлоропластов. Фотосинтетические пигменты, главный из которых хлорофилл, особым образом сгруппированы на этих мембранах, и формируют так называемые фотосистемы. Расположение молекул пигментов в фотосистеме напоминает пирамиду.
Ф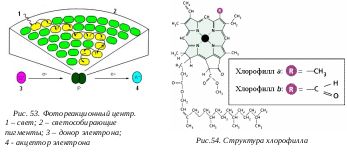 отон света может улавливать любая из молекул. При этом один из подвижных электронов этой молекулы хлорофилла переходит в возбужденное состояние, а затем отделяется и переходит к другой молекуле фотосистемы. Заканчиваются процессы перемещения электрона тем, что он оказывается у молекулы, расположенной на вершине пирамиды - в хлорофилле-ловушке.
отон света может улавливать любая из молекул. При этом один из подвижных электронов этой молекулы хлорофилла переходит в возбужденное состояние, а затем отделяется и переходит к другой молекуле фотосистемы. Заканчиваются процессы перемещения электрона тем, что он оказывается у молекулы, расположенной на вершине пирамиды - в хлорофилле-ловушке.
Если экстрагировать хлорофилл из растения и осветить его раствор, то раствор начнет флуоресцировать - поглощенная энергия будет высвечиваться при возвращении электронов в «основное состояние». В хлоропластах этого не происходит. Молекулы хлорофилла организованы в них таким образом, что возбужденные электроны не возвращаются сразу же в «основное состояние», а передаются другим молекулам - электрон отделяется от фотосистемы и движется по электронно-транспортной цепи. В ходе этого движения синтезируются АТФ и НАДФH.
Световая фаза идет при участии двух фотосистем.
В фотосистеме I при поглощении света хлорофиллом энергия электронов возрастает до уровня, на котором они могут восстанавливать неидентифицированный акцептор электронов X. От него электроны через ферредоксин (Fd) передаются НАДФ и восстанавливают его. Этот восстановленный НАДФ сам может затем поставлять электроны, необходимые для восстановления атмосферного СО2 до глюкозы. Таким путем световая энергия превращается в химическую. Источником протонов для синтеза НАДФH является вода.
В фотосистеме I имеет место также циклический поток электронов: электроны, захваченные акцептором X, возвращаются через цитохром h хлорофиллу. При таком потоке электронов синтезируется только АТФ.
В фотосистеме II электроны хлорофилла при поглощении света переходят на энергетический уровень, на котором они могут присоединяться к акцептору электронов Q-C550. Эти электроны передаются затем в серии окислительно-восстановительных реакций, включающих пластохинон, цитохром и пластоцианин, хлорофиллу фотосистемы I. В фотосистеме II богатые энергией электроны возбужденного хлорофилла передаются системе переноса электронов и замещаются бедными энергией электронами, поступающими от воды.
Параллельно процессу переноса электронов по электронно-транспортной цепи происходит процесс фотолиза воды:
hν
2 H2O…→ 2 [O] + 4 H+ + 4ē
О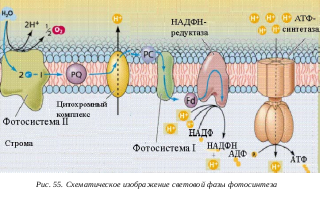 бразовавшиеся электроны замещают электроны, отданные молекулами хлорофилла, а атомы кислорода объединяются в молекулы и как побочный продукт удаляются в атмосферу.
бразовавшиеся электроны замещают электроны, отданные молекулами хлорофилла, а атомы кислорода объединяются в молекулы и как побочный продукт удаляются в атмосферу.
Хлорофилл, следовательно, играет роль промежуточного соединения на пути электронов от низкого энергетического уровня в молекуле воды к высокому энергетическому уровню в конечном акцепторе электронов. Именно в молекуле хлорофилла световая энергия используется для того, чтобы «перекачивать» электроны на этот высокий энергетический уровень.
Богатые энергией электроны из фотосистемы II, пройдя через ряд соединений, составляющих так называемую цепь переноса электронов, в конце концов, замещают электроны, утраченные хлорофиллом фотосистемы I. В цепи переноса электронов происходит ряд окислительно-восстановительных реакций, и в каждой из этих реакций электроны переходят на несколько более низкий энергетический уровень. Часть энергии, отдаваемой на отдельных этапах переноса электронов, используется для синтеза АТФ из АДФ и неорганического фосфата. Поэтому можно сказать, что синтез АТФ сопряжен с переносом электронов.
Еще одно место синтеза АТФ связано с фотосистемой I. Это циклическое фотофосфорилирование зависит от электронов, восстанавливающих акцептор X, а затем возвращаемых через ряд переносчиков хлорофиллу, от которого они первоначально и поступили.
Таким образом, в процессе фотосинтеза участвуют две фотосистемы, связанные между собой через систему переноса электронов и два богатых энергией соединения: АТФ и восстановленный НАДФ.
Эти соединения поставляют энергию для последующих реакций, не требующих участия света и приводящих, в конечном счете, к восстановлению СО2 до сахаров. Восстановление СО2 начинается с фиксации молекул СО2 молекулами «акцептора», после чего атомы углерода вступают в цикл реакций, в результате которого акцепторные молекулы регенерируют и на каждые шесть фиксированных молекул СО2 образуется одна молекула глюкозы. Именно в этих темновых реакциях фотосинтеза химическая энергия, которую генерируют световые реакции, стабилизируется в молекуле глюкозы. В конце концов, из молекул глюкозы образуется крахмал - соединение, в виде которого запасаются и атомы углерода, и энергия.
В ходе реакций темновой фазы происходят процессы фиксации углекислого газа при участии молекул НАДФH, на протекание которых затрачивается энергия АТФ. Эти реакции проходят во внутренней среде - строме хлоропластов. Наиболее распространенным способом фиксации углерода является цикл химических реакций, названный по имени его открывателя циклом Кальвина. Он включает в себя двеннадцать химических реакций. На каждый оборот цикла фиксируется одна молекула углекислого газа.
Суммарная реакция цикла Кальвина:
18АТФ + 12НАДФH + 6CO2 →C6H12O6 + 18H3PO4 + 18АДФ + 6H2O + 12НАДФ
Таким образом, суммарная реакция фотосинтеза имеет следующий вид:
6СО2 + 12Н2О + hν → С6 Н12О6 + 6О2 ↑ + 6Н2О
Невозможно переоценить значение фотосинтеза для всей жизни на Земле и для человечества в частности. Фотосинтез, в процессе которого улавливается и трансформируется энергия, не только поставляет «горючее», необходимое для существования всего живого; ему мы обязаны и теми энергетическими резервами, которыми располагает в настоящее время человечество с его все более усиливающейся индустриализацией, поскольку большая часть этих резервов представлена запасами ископаемого горючего. За счет фотосинтеза Земля получает ежегодно около 840 триллионов киловатт-часов, что более чем в 10 раз превышает мировое потребление энергии. Фотосинтез же поставляет и необходимый всем высшим формам жизни атмосферный кислород, который представляет собой его побочный продукт, высвобождающийся при окислении воды.
3.4. Энергетический обмен в клетке, его значение и этапы
Животные организмы, не способные к фотосинтезу, зависят от этих запасных веществ, синтезируемых растениями. Запасенная энергия переводится в форму, в которой она может использоваться растительными и животными клетками для выполнения какой-нибудь работы, например для синтеза других молекул, необходимых клетке, или же для механической, электрической и осмотической работы.
Эффективное высвобождение запасенной энергии происходит в процессе аэробного дыхания, во время которого молекулы, содержащие запасенную энергию, расщепляются в определенной последовательности реакций.
Все химические соединения характеризуются определенной энергией; часть энергии представляет собой так называемую свободную энергию, которая может быть использована для выполнения работы. Количество свободной энергии, которое может быть извлечено из данной молекулы, зависит от ее природы и от расположения атомов, входящих в ее состав. При химических реакциях, когда одни химические связи разрываются и вместо них возникают другие, происходит перераспределение энергии в молекуле. При некоторых реакциях свободная энергия высвобождается и может расходоваться на выполнение какой-нибудь работы. Существуют и реакции, идущие с потреблением свободной энергии.
Источником энергии в клетке чаще всего служат окислительно-восстановительные реакции, при которых происходит перенос электронов от одного соединения (которое, следовательно, окисляется) к другому (восстанавливающемуся). Способность отдавать электроны (т. е. действовать как восстановитель) определяет величину химического потенциала данного соединения. Когда соединение с более высоким химическим потенциалом восстанавливает соединение с более низким потенциалом, свободная энергия высвобождается. Разность между начальной и конечной энергиями электрона (или электронов) характеризует количество свободной энергии, «высвободившейся» в данной реакции. В клетке, разумеется, энергия в действительности не высвобождается; просто часть ее запасается в форме, которая затем может быть использована.
В переносе энергии от энерговыделеяющих химических реакций к процессам, идущим с потреблением энергии (которые собственно и составляют работу клетки), принимает участие аденозинтрифосфат, выполняющий важную роль носителя энергии. АТФ образуется в клетке путем присоединения еще одной фосфатной группы к аденозиндифосфату (АДФ). Поскольку э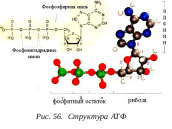 нергетический уровень АТФ выше, чем у АДФ, на присоединение этой фосфатной группы должна затрачиваться энергия. Именно та энергия, которая поставляется реакциями окисления-восстановления, затрачивается на образование АТФ и, следовательно, запасается в его молекуле. Это достигается благодаря сопряжению реакции фосфорилирования, т. е. переноса фосфатной группы, с реакциями окисления-восстановления (с переносом электронов).
нергетический уровень АТФ выше, чем у АДФ, на присоединение этой фосфатной группы должна затрачиваться энергия. Именно та энергия, которая поставляется реакциями окисления-восстановления, затрачивается на образование АТФ и, следовательно, запасается в его молекуле. Это достигается благодаря сопряжению реакции фосфорилирования, т. е. переноса фосфатной группы, с реакциями окисления-восстановления (с переносом электронов).
Энергия, запасенная в молекуле АТФ, высвобождается, когда она требуется для выполнения какой-нибудь работы, в результате гидролиза АТФ до АДФ и неорганического фосфата. Для того чтобы эта свободная энергия не рассеивалась полностью в виде тепла, превращение АТФ в АДФ, совершающееся в клетке ферментативным путем, происходит таким образом, что часть энергии используется для выполнения работы. АТФ действует как своего рода энергетический «челнок». Реакции окисления-восстановления и сопряженное с ними фосфорилирование протекают при дыхании (когда запасенная в клетке энергия используется на образование АТФ) и при фотосинтезе (когда энергия, уловленная хлоропластами, поступает - через АТФ - в конечные продукты фотосинтеза, т.е. в запасные вещества растений).
Основным энергетическим веществом клетки является глюкоза. Процесс ее расщепления в клетке до воды и углекислого газа в присутствии свободного кислорода состоит из трех этапов:
Гликолиз и окислительное декарбоксилирование пировиноградной кислоты с образованием ацетил-КоА.
Окисление ацетил-КоА в цикле трикарбоновых кислот (цикле Кребса).
Окислительное фосфорилирование в электронно-транспортной цепи.
На первом этапе происходит образование двух молекул ацетилкоэнзима А (ацетил-КоА) из молекулы глюкозы. Это происходит в две стадии. На первой - молекула глюкозы расщепляется до двух молекул пировиноградной кислоты (ПВК). Эта стадия известна под названием гликолиза (гр glycos - сладкий lysis - расщепление). Он протекает в цитоплазме и не требует присутствия кислорода. Гликолиз состоит из одиннадцати последовательных реакций и осуществляется при помощи десяти ферментов.
Суммарное уравнение гликолиза:
C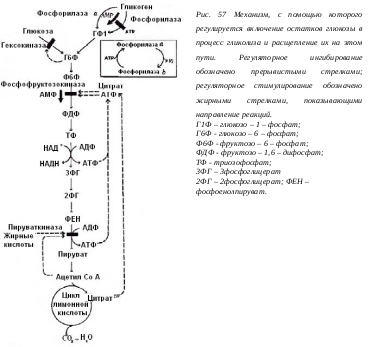 6H12O6 + 2H3PO4 + 2АДФ + 2НАД+ → 2CH3COCOOH + 2АТФ + 2НАДH
6H12O6 + 2H3PO4 + 2АДФ + 2НАД+ → 2CH3COCOOH + 2АТФ + 2НАДH
Дальнейшая судьба ПВК зависит от наличия в среде кислорода. В бескислородных условиях образовавшуюся пировиноградную кислоту анаэробные организмы перерабатывают либо в молочную кислоту (молочнокислое брожение), либо в этиловый спирт (спиртовое брожение).
У аэробных организмов ПВК переносится из цитоплазмы в митохондрии и там начинается вторая стадия первого этапа - окислительное декарбоксилирование ПВК. В этих реакциях участвуют три фермента и пять коферментов.
Уравнение реакции окислительного декарбоксилирования пировиноградной кислоты с образованием ацетил-КоА:
CH3COCOOH + КоА + НАД+ → CH3CO-КоА + CO2 + НАДH
Ацетил-КоА поступает в цикл трикарбоновых кислот, где происходит полное окисление промежуточных продуктов. Именно в матриксе митохондрии располагаются ферменты цикла Кребса. В целом цикл Кребса состоит более чем из десяти реакций.
Суммарное уравнение реакций цикла трикарбоновых кислот:
CH3CO-КоА + АДФ + Ф + 3 НАД+ + ФАД+ → КоА + АТФ + 3НАДH + ФАДH2 + 2CO2
В
осстановленные НАД и ФАД участвуют в третьем этапе клеточного дыхания - окислительном фосфорилировании.
В
ходе третьего этапа происходит окисление атомов водорода молекулярным кислородом с образованием воды и запасанием выделившейся энергии в виде АТФ. Процесс окислительного фосфорилирования осуществляется в несколько стадий путем последовательной передачи электронов по цепи молекул переносчиков или электронно-транспортной цепи. Эти молекулы локализуются на внутренней мембране митохондрий.
В результате работы электронно-транспортной цепи атомы водорода с НАДH и ФАДH2 разделяются на протоны и электроны. Электроны в конечном итоге переносятся на атомы кислорода, а протоны - в межмембранное пространство митохондрий. Затем протоны через пронизывающий всю мембрану комплекс фермента АТФ-синтетазы возвращаются в матрикс митохондрий. При этом образуется АТФ из АДФ и фосфорной кислоты. Механизм образования АТФ объясняется наиболее распространенной хемоосмотической теорией Митчелла, согласно которой АТФ образуется за счет кинетической энергии протона, проходящего через АТФ-синтетазу.
Суммарное уравнение всех реакций расщепления глюкозы будет выглядеть следующим образом:
C6H12O6 + 6O2 + 4 АДФ + 4 Ф + 10 НАД+ + 2 ФАД+→
→ 6 CO2 + 6 H2O + 4 АТФ + 10 НАДH + 2 ФАДH
Одна молекула НАДH2 способна образовать три молекулы АТФ, а одна молекула ФАДH2 - две молекулы АТФ. Следовательно, суммарное уравнение расщепления глюкозы можно записать следующим образом:
C6H12O6 + 6 O2 + 38 H3PO4 + 38 АДФ → 6 CO2 + 44 H2O + 38 АТФ
АТФ транспортируется ко всем участкам клетки, где необходима энергия. Эта энергия, заключенная в макроэргических связях в молекуле АТФ, выделяется при расщеплении АТФ до АДФ. АДФ снова поступает в митохондрии, где в ходе восстановительных реакций превращается в АТФ, связав энергию, освобожденную при окислении веществ.
Углекислый газ удаляется у растений через устьица, а у животных - через органы дыхания.
Кроме глюкозы окислению могут быть подвергнуты моносахариды, все 20 аминокислот, а также жирные кислоты и спирты липидов. Кроме указанного, существует еще несколько путей окисления органических веществ, например, пентозофосфатный цикл, в котором образуется НАДФH2, широко используемый в процессах биосинтеза.
3.5. Пластический обмен
Пластическим обменом называют все реакции биосинтеза, идущие в клетках организма. Это синтез белков, жиров, углеводов, нуклеиновых кислот. За счет процессов ассимиляции происходит образование клеточных структур, рост клеток, а, следовательно, всего организма. Синтетические процессы происходят на мембранах эндоплазматической сети и комплекса Гольджи. На гранулярной ЭПС идет синтез белка и фосфолипидов мембран, агранулярной ЭПС - синтез углеводов и липидов. Синтез нуклеиновых кислот идет в ядре и носит матричный характер. Процессы репликации (удвоения ДНК) катализируются ДНК-полимеразой, иРНК транскрибируется на ДНК, синтез рРНК идет в ядрышке.
3.5.1. Синтез белка
В настоящее время известно, что сходство и различие организмов определяется главным образом набором белков. Чем ближе организмы по происхождению друг к другу, тем большее сходство белков они обнаруживают. Молекула ДНК контролирует деятельность клетки и обеспечивает передачу наследственной информации в поколениях. Синтез белка происходит в рибосомах, расположенных в цитоплазме, а молекула ДНК находится главным образом в ядре клетки, таким образом, молекулы ДНК непосредственного участия в синтезе белка не принимают. В ДНК содержится и хранится информация о структуре белков, причем порядок расположения нуклеотидов в ДНК определяет порядок аминокислот в молекуле белка, то есть его первичную структуру. Информация, которую содержит молекула ДНК, называется генетической. Исследования показали, что четыре вида нуклеотидов и порядок их сочетания в молекуле ДНК представляют собой код, который определяет биосинтез специфических белков.
Код - это система символов, знаков, необходимая для перевода одной формы информации в другую. Каждую аминокислоту в молекуле белка определяет последовательность трех нуклеотидов ДНК, получивших название триплета или кодона. Участок ДНК, ответственный за синтез молекулы одного белка, называется геном. В состав гена входит столько триплетов, сколько аминокислот содержится в данном белке.
Код нуклеиновых кислот имеет свои особенности. Во-первых, триплетность - одну аминокислоту кодируют три нуклеотида. Это необходимо для обеспечения возможности определить все аминокислоты (четыре нуклеотида могут образовывать 64 разные тройки). Некоторые аминокислоты кодируются несколькими триплетами. Существуют бессмысленные кодоны (У-А-А; У-А-Г; У-Г-А), определяющие конец полипептидной цепи (стоп-кодоны).
Второй особенностью генетического кода является однозначность - код не перекрывается и один триплет кодирует только одну аминокислоту. Вырожденность генетического кода определяет способность кодировать одну и ту же аминокислоту (кроме метионина и триптофана) одновременно несколькими триплетами (от 2 до 6), что повышает устойчивость к случайным ошибкам (точечным мутациям).
Универсальность генетического кода - это способность триплетов кодировать одни и те же аминокислоты у самых разных организмов от вирусов до человека. Это является еще одним доказательством единства происхождения всего живого.
3.5.1.1 Этапы биосинтеза белка.
Биосинтез белка состоит из двух процессов: транскрипции и трансляции.
Транскрипция - синтез иРНК на ДНК, идет по принципу комплиментарности с помощью фермента РНК-полимеразы. Обычно копируется один или несколько рядом стоящих генов (ферментов, катализирующих один каскад реакций) - этот участок называется опероном. Опероны выявлены только у бактерий. В начале оперона имеется «посадочная площадка» для фермента РНК- полимеразы - эта площадка называется промотор. В транскрипции различают четыре стадии: связывание, инициация синтеза, элонгация синтеза и терминация.
Информация снимается с одной цепи.
Образовавшаяся цепочка иРНК подвергается процессу сплайсинга: отдельные некодирующие участки интроны вырезаются, а оставшиеся (кодирующие) - экзоны остаются и сшиваются. Зрелая иРНК поступает через ядерные поры в цитоплазму.
Т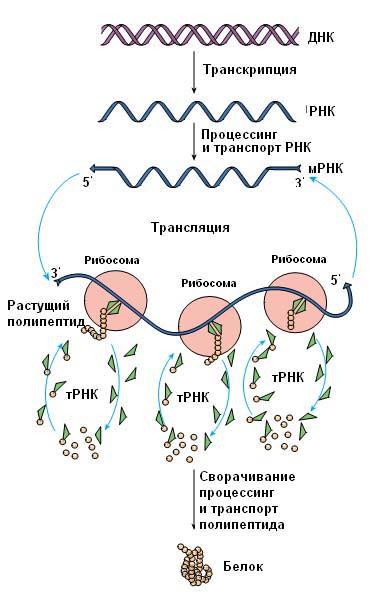 рансляция - перевод информации с кода триплетов иРНК в последовательность аминокислот полипептидной цепи. Трансляция идет на рибосомах с помощью транспортной РНК (тРНК), которая содержит 60-100 нуклеотидов. Несколько комплиментарных участков цепи тРНК слипаются за счет водородных связей и образуют крестообразную структуру. К одному концу тРНК прикрепляется аминокислота, противоположный конец - антикодон определяет аминокислоту, с которой соединяется акцепторный участок.
рансляция - перевод информации с кода триплетов иРНК в последовательность аминокислот полипептидной цепи. Трансляция идет на рибосомах с помощью транспортной РНК (тРНК), которая содержит 60-100 нуклеотидов. Несколько комплиментарных участков цепи тРНК слипаются за счет водородных связей и образуют крестообразную структуру. К одному концу тРНК прикрепляется аминокислота, противоположный конец - антикодон определяет аминокислоту, с которой соединяется акцепторный участок.
Т
Рис. 60. Общая схема биосинтеза белка
рансляция начинается с того, что иРНК связывается с рибосомной частицей. При этом рибосомная частица специфически взаимодействует с началом кодирующей нуклеотидной последовательности иРНК. Этап связывания иРНК с рибосомной частицей и образование первой пептидной связи называется
инициацией трансляции. В инициации трансляции участвуют не целая рибосома, а ее малая субъединица. При завершении этапа инициации трансляции, к ней присоединяется большая субчастица, образуя полную рибосомную частицу. Вслед за инициацией рибосома последовательно «читает» цепочку иРНК по триплетам нуклеотидов по направлению от 5' к З'-концу, наращивая полипептидную цепочку аминокислотными остатками. Этот этап собственно трансляции называется
элонгацией. В результате элементарного элонгационного цикла рибосомы прочитывается один триплет иРНК и образуется одна пептидная связь (добавляется одна аминокислота к растущему полипептиду).
В
ходе элонгации рибосома сидит на участке кодирующей последовательности и-РНК и удерживает молекулу пептидил-тРНК. Пептидил-тРНК - это растущая полипептидная цепь, ковалентно присоединенная к тРНК, которая и принесла последний аминокислотный остаток растущему пептиду. Когда пептидил-тРНК занимает Р-участок рибосомы (часть рибосомы, связывающая пептидил-тРНК), рибосома может связывать молекулу аминоацил-тРНК, соответствующую кодону, установленному на данный момент в А-участке (участок рибосомы связывающий аминоацил-тРНК). В результате, удерживаемая рибосомой пептидил-тРНК и вновь связанная аминоацил-тРНК оказываются в рибосоме бок о бок. Рибосома катализирует реакцию между этими двумя субстратами рибосомы - пептидил-тРНК и аминоацил-тРНК. Пептидильный остаток переносится от «своей» тРНК на аминогруппу аминоацил-тРНК, тем самым, удлиняясь на одну аминокислоту на С-конце. Теперь в Р-участке осталась деацилированная тРНК (без аминокислоты), а в А-участке помещается остаток тРНК удлиненной пептидил-тРНК. Следующий за этим акт транслокации состоит в том, что деацилированная тРНК (без аминокислоты) выталкивается из Р-участка, а пептидил-тРНК (ее остаток тРНК) перемещается вместе со связанным с ней кодоном иРНК из А-участка в Р-участок. В итоге А-участок освобождается, и в нем устанавливается следующий кодон иРНК. Цикл завершился.
Повторение таких циклов по числу кодонов мРНК создает полный процесс элонгации.
Достигнув специального нуклеотидного триплета (стоп-кодона, или кодона терминации), рибосома освобождает синтезированную полипептидную цепочку белка, происходит терминация трансляции.
Рибосомные частицы, закончившие трансляцию и отделившиеся от иРНК, снова готовы инициировать трансляцию.
П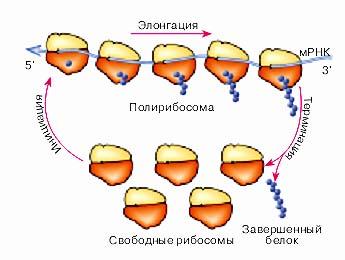 Рис. 62 Схема цикла трансляции осле инициации, двигаясь по цепи иРНК, рибосома все больше отодвигается от 5'-конца, и в результате ранее занимаемый ею отрезок иРНК становится свободным и способным связывать другую рибосому. Эта вторая рибосома тоже начинает трансляцию и двигается вслед за первой рибосомой, отодвигается от 5'-концевого отрезка и дает возможность третьей рибосоме сесть на иРНК и начать трансляцию и т.д. Таким путем, двигаясь вдоль иРНК друг за другом, несколько рибосом одновременно считывают одну и ту же запись и, следовательно, синтезируют идентичные полипептидные цепи. Такая структура, в которой одна иРНК связана со многими рибосомами, ее одновременно транслирующими, называется полирибосомой
Рис. 62 Схема цикла трансляции осле инициации, двигаясь по цепи иРНК, рибосома все больше отодвигается от 5'-конца, и в результате ранее занимаемый ею отрезок иРНК становится свободным и способным связывать другую рибосому. Эта вторая рибосома тоже начинает трансляцию и двигается вслед за первой рибосомой, отодвигается от 5'-концевого отрезка и дает возможность третьей рибосоме сесть на иРНК и начать трансляцию и т.д. Таким путем, двигаясь вдоль иРНК друг за другом, несколько рибосом одновременно считывают одну и ту же запись и, следовательно, синтезируют идентичные полипептидные цепи. Такая структура, в которой одна иРНК связана со многими рибосомами, ее одновременно транслирующими, называется полирибосомой
Никакого отдельного от рибосомы белка-фермента, катализирующего образование пептидных связей на рибосоме, не существует. Итак, в процессе биосинтеза белка рибосома:
принимает кодированную генетическую информацию от ДНК в виде иРНК и расшифровывает ее;
катализирует образование пептидных связей в реакции транспептидации;
передвигает цепь иРНК и молекулы тРНК.
Таким образом, рибосома - сложная белоксинтезирующая частица, обладающая одновременно генетической, ферментативной и механической функциями.
3.5.1.2. Регуляция синтеза белка
Клетки разных тканей одного организма отличаются разным набором ферментов и других белков. Но все эти разные клетки произошли из одной оплодотворенной яйцеклетки в результате множества делений. Перед каждым в клетке происходит процесс удвоения ДНК - репликация. Следовательно, во всех клетках тела имеется одинаковый набор молекул ДНК - одна и та же генетическая информация о составе и структуре белков. Однако в каждой клетке реализуется не вся а только часть генетической информации. Механизмы регуляции синтеза отдельных белков изучили в 1961 году Франсуа Жакоб, Андре-Мишель Львов, Жан Люсьен Моно у бактерий. За эту работу они получили Нобелевскую премию.
У прокариот можно выделить структуру, называемую опероном. Это участок ДНК, состоящий из следующих частей:
П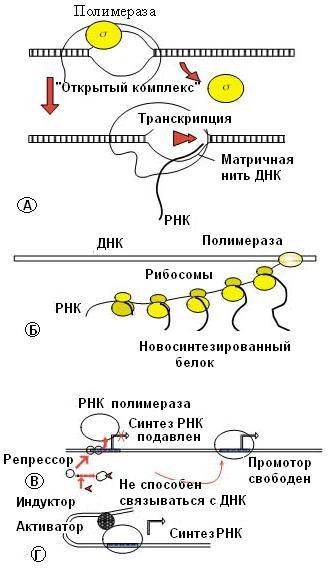
Рис. 63. Регуляция биосинтеза белка у прокариот
А- образование открытого комплекса ДНК с РНК-полимеразой, начало транскрипции;
Б – одновременный процесс транскрипции и трансляции, образование полирибосом;-
В – индуктор связывается с белком-репрессором, который на может тормозить синтез иРНК
Г – молекула ДНК изгибается, белок- активатор вступает в контакт с РНК-полимеразой, активизируя ее.
ромотор - определенная последовательность нуклеотидов, которая связывается с ферментом РНК-полимеразой. Процесс связывания является первым этапом в последующей транскрипции. Оператор - участок ДНК, связанный с белком-репрессором. До тех пор, пока эта связь не нарушена, РНК-полимераза не будет считывать информацию.
Ряд структурных генов, кодирующих информацию о ферментах, участвующих в расщеплении определенного субстрата.
При поступлении субстрата в клетку его молекулы связываются с белком-репрессором, который после этого теряет способность взаимодействовать с оператором, происходит инициация, а РНК-полимераза начинает синтезировать иРНК, комплементарную структурным генам (элонгация). Затем в рибосомах синтезируются соответствующие ферменты, расщепляющие данный субстрат. Если субстрата не остается, освобождается белок-репрессор, который вновь блокирует оператор, и синтез иРНК и ферментов прекращается. Таким образом, бактерия синтезирует только те ферменты, которые ей необходимы в данный момент, что позволяет экономить энергию.
У эукариот регуляция активности генов значительно сложнее. На нее влияют гормоны, медиаторы, другие биологически активные вещества, причем транскрипция, выход иРНК и трансляция регулируются отдельно и могут быть разделены во времени.
85





 отон света может улавливать любая из молекул. При этом один из подвижных электронов этой молекулы хлорофилла переходит в возбужденное состояние, а затем отделяется и переходит к другой молекуле фотосистемы. Заканчиваются процессы перемещения электрона тем, что он оказывается у молекулы, расположенной на вершине пирамиды - в хлорофилле-ловушке.
отон света может улавливать любая из молекул. При этом один из подвижных электронов этой молекулы хлорофилла переходит в возбужденное состояние, а затем отделяется и переходит к другой молекуле фотосистемы. Заканчиваются процессы перемещения электрона тем, что он оказывается у молекулы, расположенной на вершине пирамиды - в хлорофилле-ловушке.  бразовавшиеся электроны замещают электроны, отданные молекулами хлорофилла, а атомы кислорода объединяются в молекулы и как побочный продукт удаляются в атмосферу.
бразовавшиеся электроны замещают электроны, отданные молекулами хлорофилла, а атомы кислорода объединяются в молекулы и как побочный продукт удаляются в атмосферу. нергетический уровень АТФ выше, чем у АДФ, на присоединение этой фосфатной группы должна затрачиваться энергия. Именно та энергия, которая поставляется реакциями окисления-восстановления, затрачивается на образование АТФ и, следовательно, запасается в его молекуле. Это достигается благодаря сопряжению реакции фосфорилирования, т. е. переноса фосфатной группы, с реакциями окисления-восстановления (с переносом электронов).
нергетический уровень АТФ выше, чем у АДФ, на присоединение этой фосфатной группы должна затрачиваться энергия. Именно та энергия, которая поставляется реакциями окисления-восстановления, затрачивается на образование АТФ и, следовательно, запасается в его молекуле. Это достигается благодаря сопряжению реакции фосфорилирования, т. е. переноса фосфатной группы, с реакциями окисления-восстановления (с переносом электронов). 6H12O6 + 2H3PO4 + 2АДФ + 2НАД+ → 2CH3COCOOH + 2АТФ + 2НАДH
6H12O6 + 2H3PO4 + 2АДФ + 2НАД+ → 2CH3COCOOH + 2АТФ + 2НАДH

 рансляция - перевод информации с кода триплетов иРНК в последовательность аминокислот полипептидной цепи. Трансляция идет на рибосомах с помощью транспортной РНК (тРНК), которая содержит 60-100 нуклеотидов. Несколько комплиментарных участков цепи тРНК слипаются за счет водородных связей и образуют крестообразную структуру. К одному концу тРНК прикрепляется аминокислота, противоположный конец - антикодон определяет аминокислоту, с которой соединяется акцепторный участок.
рансляция - перевод информации с кода триплетов иРНК в последовательность аминокислот полипептидной цепи. Трансляция идет на рибосомах с помощью транспортной РНК (тРНК), которая содержит 60-100 нуклеотидов. Несколько комплиментарных участков цепи тРНК слипаются за счет водородных связей и образуют крестообразную структуру. К одному концу тРНК прикрепляется аминокислота, противоположный конец - антикодон определяет аминокислоту, с которой соединяется акцепторный участок.
 Рис. 62 Схема цикла трансляции осле инициации, двигаясь по цепи иРНК, рибосома все больше отодвигается от 5'-конца, и в результате ранее занимаемый ею отрезок иРНК становится свободным и способным связывать другую рибосому. Эта вторая рибосома тоже начинает трансляцию и двигается вслед за первой рибосомой, отодвигается от 5'-концевого отрезка и дает возможность третьей рибосоме сесть на иРНК и начать трансляцию и т.д. Таким путем, двигаясь вдоль иРНК друг за другом, несколько рибосом одновременно считывают одну и ту же запись и, следовательно, синтезируют идентичные полипептидные цепи. Такая структура, в которой одна иРНК связана со многими рибосомами, ее одновременно транслирующими, называется полирибосомой
Рис. 62 Схема цикла трансляции осле инициации, двигаясь по цепи иРНК, рибосома все больше отодвигается от 5'-конца, и в результате ранее занимаемый ею отрезок иРНК становится свободным и способным связывать другую рибосому. Эта вторая рибосома тоже начинает трансляцию и двигается вслед за первой рибосомой, отодвигается от 5'-концевого отрезка и дает возможность третьей рибосоме сесть на иРНК и начать трансляцию и т.д. Таким путем, двигаясь вдоль иРНК друг за другом, несколько рибосом одновременно считывают одну и ту же запись и, следовательно, синтезируют идентичные полипептидные цепи. Такая структура, в которой одна иРНК связана со многими рибосомами, ее одновременно транслирующими, называется полирибосомой 










