
1.Определите, о каком веществе идёт речь
Бесцветный газ, плохо растворим в воде, легко соединяется с кислородом воздуха, образуя бурый газ.

Ответ
NO – оксид азота (II)

2.Определите, о каком веществе идёт речь
Газ бурого цвета с характерным резким запахом, хорошо растворим в воде

Ответ: NО 2 - оксид азота (IV)

3. Составьте уравнения реакций по схеме. Назовите вещество Х
NO → NO 2 → Х
Если про вещество Х известно, «Она родилась в самой волшебной, самой удивительной стране – химической лаборатории. Ее папа – оксид азота (IV), был мужчина злого нрава и носил прозвище «Лисий хвост». Ее мама была простой спокойной женщиной и звали ее Вода. Она появилась в атмосфере кислорода, дали ей красивое женское имя – Кислота. Но фамилию она получила……

X – HNO3 (азотная кислота)
2.4NO 2 +2H 2 O+O 2 =4HNO 3

Азотная кислота

Что мы знаем об азотной кислоте?
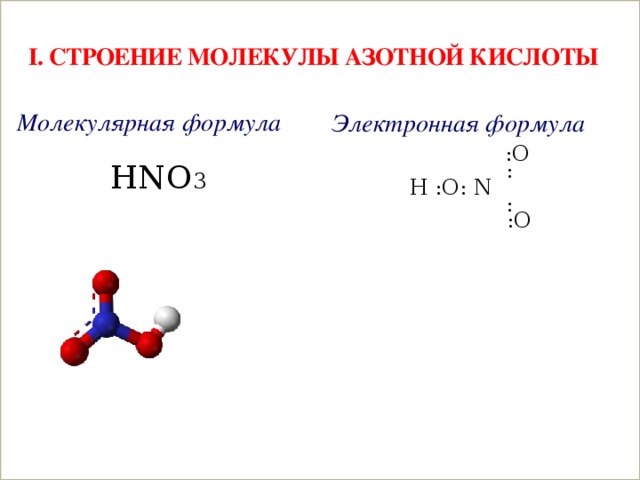
I. Строение молекулы азотной кислоты
Электронная формула
:O
:
H :O: N
:
:O
Молекулярная формула
HNO 3
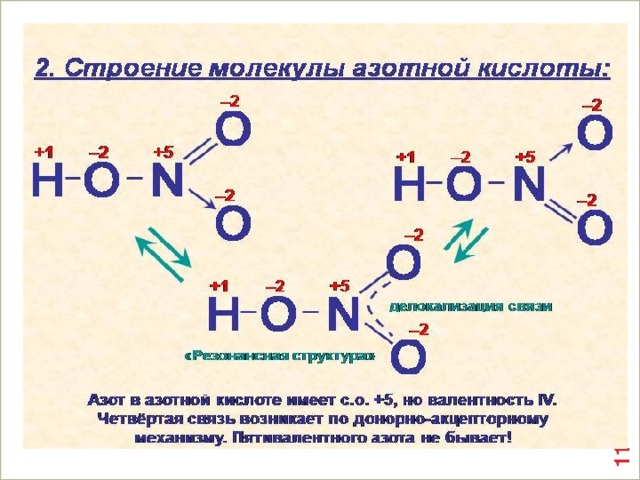

II.Характеристика азотной кислоты
1. По основности: одноосновная
2. По содержанию «О»: кислородсодержащая
3. По растворимости в воде: растворимая
4. По стабильности: нестабильная
5. По летучести: летучая
6. По степени диссоциации: сильная

III . Физические свойства азотной кислоты
Агрегатное состояние – жидкость ;
Цвет – без цвета, при хранении на свету разлагается , приобретая желтоватый оттенок:
4HNO 3 =4NO 2 ↑ + O 2 ↑ + 2H 2 O
Запах – резкий;
Растворимость в воде – хорошая;
«Дымит» на воздухе ,если концентрация более 60%;

Из выданного перечня веществ выберите вещества с которыми будет реагировать разбавленная азотная кислота. Напишите уравнения соответствующих реакций в тетради:
CuO, SO 3 , Cu(OH) 2 , O 2 ,Na 2 CO 3,
HCI

IV. Химические свойства HNO 3
А) с оксидами металлов:
CuO + 2HNO 3 = Cu(NO 3 ) 2 + H 2 O
Б) с основаниями:
Cu(OH) 2 + 2HNO 3 = Cu(NO 3 ) 2 + 2H 2 O
В) с солями:
Na 2 CO 3 + 2HNO 3 = 2NaNO 3 + CO 2 ↑ + H 2 O
 60% Не реагируют (пассивируют) HNO 3 от 30 % до 60% NO 2 , N 2 Малоактивные Очень разбавленная кислота Cr - Sn NO, NO 2 NO 2 Pb - Ag HNO 3 Благородные NН 3 N 2 O N 2 O, NН 3 NO, NO 2 - Au , Pt Соли аммония NO - - N 2 O, NН 3 - " width="640"
60% Не реагируют (пассивируют) HNO 3 от 30 % до 60% NO 2 , N 2 Малоактивные Очень разбавленная кислота Cr - Sn NO, NO 2 NO 2 Pb - Ag HNO 3 Благородные NН 3 N 2 O N 2 O, NН 3 NO, NO 2 - Au , Pt Соли аммония NO - - N 2 O, NН 3 - " width="640"
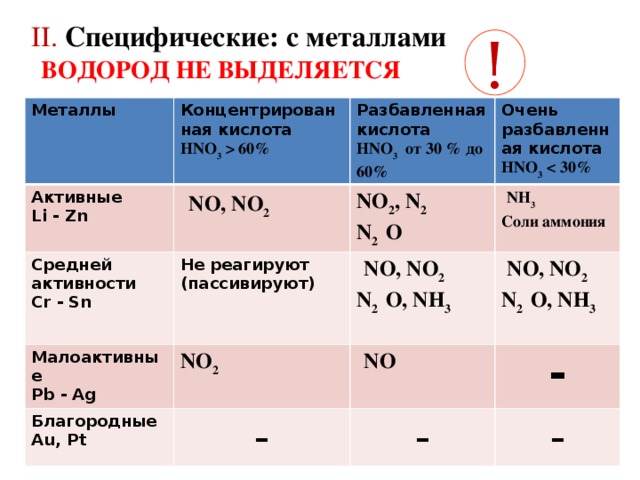
II. Cпецифические: с металлами
!
ВОДОРОД НЕ ВЫДЕЛЯЕТСЯ
Металлы
Активные
Концентрированная кислота
NO, NO 2
Li - Zn
Средней активности
Разбавленная кислота
HNO 3 60%
Не реагируют (пассивируют)
HNO 3 от 30 % до 60%
NO 2 , N 2
Малоактивные
Очень разбавленная кислота
Cr - Sn
NO, NO 2
NO 2
Pb - Ag
HNO 3
Благородные
NН 3
N 2 O
N 2 O, NН 3
NO, NO 2
-
Au , Pt
Соли аммония
NO
-
-
N 2 O, NН 3
-

Взаимодействие железа с концентрированной азотной кислотой

Взаимодействие ртути с концентрированной азотной кислотой

Задание 1: Составьте уравнения реакций, методом электронного баланса подберите коэффициенты
1 вариант: Реакция разбавленной азотной кислоты с медью.
2 вариант: Реакция концентрированной азотной кислоты с медью

1 вариант
Cu + 4HNO 3 (конц) = Cu(NO 3 ) 2 + 2H 2 O + 2NO 2 ↑
2 вариант
3Cu + 8HNO 3 (разб) = 3Cu(NO 3 ) 2 + 4H 2 O + 2NO ↑

Окислительные свойства . Взаимодействие с неметаллами: (S, P, C)
Азотная кислота превращается в NO (или в NO 2 ); неметаллы окисляются до соответствующих кислот:
Видео "Взаимодействие азотной кислоты с фосфором"

2. Окислительные свойства Взаимодействует с неметаллами: (S, P, C)
S 0 + 6HNO 3 ( конц ) → H 2 S +6 O 4 + 6NO 2 + 2H 2 O
B 0 + 3HNO 3 → H 3 B +3 O 3 + 3NO 2
3P 0 + 5HNO 3 + 2H 2 O → 5NO + 3H 3 P +5 O 4

Взаимодействует с органическими веществами (скипидар) (видеоопыт)

V.Получение азотной кислоты
А) в лаборатории
КNO 3 + H 2 SO 4 (к) =KHSO 4 +HNO 3
25
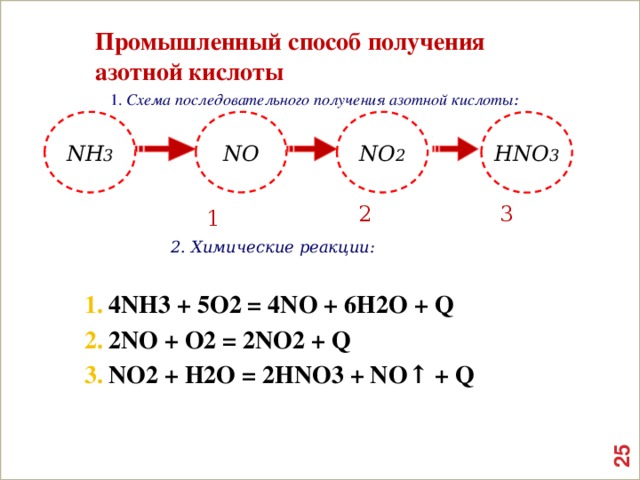
Промышленный способ получения азотной кислоты
1. Схема последовательного получения азотной кислоты :
NH 3
NО
NО 2
НNО 3
3
2
1
2. Химические реакции:
- 4NH3 + 5О2 = 4NO + 6Н2О + Q
- 2NO + O2 = 2NO2 + Q
- NO2 + H2O = 2HNO3 + NO↑ + Q
26
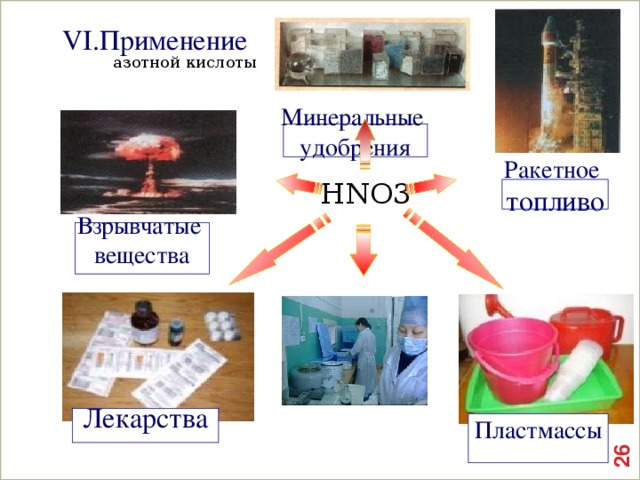
VI.Применение
азотной кислоты
Минеральные
удобрения
HNO3
Ракетное
топливо
Взрывчатые
вещества
Лекарства
Пластмассы

Выберите цифры правильных утверждений:
1.Степень окисления азота в азотной кислоте +5,а валентность только четыре.
2.Азотная кислота двухосновная кислородосодержащая кислота.
3. Азотная кислота слабый окислитель.
4.Азотная кислота окрашивает белки в желтый цвет.
5.Концентрированную азотную кислоту можно перевозить в железных цистернах.

цифры правильных утверждений:
1.Степень окисления азота в азотной кислоте +5,а валентность только четыре .
4.Азотная кислота окрашивает белки в желтый цвет.
5.Концентрированную азотную кислоту можно перевозить в железных цистернах.

Домашнее задание
§ 27, стр.158
упр. 2,3,5

Оцените свою деятельность на уроке
по 4 бальной системе: Если активно участвовали – 4 балла. Если ответили на 2 вопроса – 3 балла. Если ответили на 1 вопрос – 2 балла.
За каждое правильно выполненное задание-1 балл Подсчитайте общее количество баллов Если вы набрали 16-14 балла – оценка «5» Если вы набрали 13-11 баллов – оценка «4» Если вы набрали 10-7 баллов - оценка «3» Если вы набрали менее 6 – вам надо подтянуться.





















 60% Не реагируют (пассивируют) HNO 3 от 30 % до 60% NO 2 , N 2 Малоактивные Очень разбавленная кислота Cr - Sn NO, NO 2 NO 2 Pb - Ag HNO 3 Благородные NН 3 N 2 O N 2 O, NН 3 NO, NO 2 - Au , Pt Соли аммония NO - - N 2 O, NН 3 - " width="640"
60% Не реагируют (пассивируют) HNO 3 от 30 % до 60% NO 2 , N 2 Малоактивные Очень разбавленная кислота Cr - Sn NO, NO 2 NO 2 Pb - Ag HNO 3 Благородные NН 3 N 2 O N 2 O, NН 3 NO, NO 2 - Au , Pt Соли аммония NO - - N 2 O, NН 3 - " width="640"
























