
Зовут меня на букву «С»
Все видно на моем лице,
Валентность у меня IV ,
Бывает иногда и II .
По атомной 12 массе
Встречаюсь я везде, всегда.
В свободном виде крайне редко,
Алмазом крепким я лежу.
А вот графитом- очень часто,
Везде и всюду я пишу.
Но это только в чистом виде,
А если посмотреть вокруг-
В живых и мертвых организмах,
В угле, и торфе, и оксидах,
В солях, кислотах, даже меле-
Везде и всюду я живу!

Урок по теме «Углерод, кремний и их важнейшие соединения. Распространение углерода, кремния и их соединений в природе. Демонстрация № 8 «Поглощение активированным углем растворенных веществ (адсорбция)»

Цели урока
- 10.2.1.34 изучить физические и химические свойства углерода, кремния и их соединений;
- 10.2.1.35 объяснять, как происходит отравление угарным газом и описывать способы оказания первой помощи;

Строение атома
Si 14 ) 2e ) 8e ) 4e

Строение атома углерода

Аллотропные модификации углерода
Название модификации
Строение кристаллической решетки
Алмаз
Свойства
Графит
Прозрачное бесцветное вещество с сильной лучепреломляемостью. Кристаллы алмаза отличаются особо прочной структурой, благодаря чему он является самым твердым веществом в мире.
Химически устойчивое вещество .
Вещество серо-стального цвета, мягкий и жирный на ощупь. Хорошо проводит электрический ток. Кристаллы имеют слоистую структуру, благодаря чему обладает способностью оставлять следы на бумаге.

АЛЛОТРОПИЯ КРЕМНИЯ
Кристаллический кремний
Аморфный кремний


ОКСИДЫ КРЕМНИЯ И УГЛЕРОДА
СО 2
Кислотный оксид
SiO 2
Кислотный оксид
Молекулярная
кристаллическая решетка
Атомная
кристаллическая решетка
Бесцветный газ.
Кристаллическое, твердое вещество, тугоплавкое.
Химические
свойства
H 2 O + CO 2 = H 2 CO 3
Не взаимодействует
CO 2 + CaO = CaCO 3
SiO 2 + CaO = CaSiO 3
CO 2 + Ca(OH) 2 =CaCO 3 + H 2 O
SiO 2 + NaOH = Na 2 SiO 3 + H 2 O
CO 2 + 2Mg = 2MgO + C
SiO 2 + 2C = 2MgO + Si
C + CO 2 = 2CO
SiO 2 + 2C = Si + 2CO

КИСЛОТЫ
H 2 CO 3
H 2 SiO 3
Двухосновная, кислородсодержащая, слабая, непрочная, т.к. летучая.
Двухосновная, кислородсодержащая, слабая, нерастворимая в воде.
Получение: СО 2 + Н 2 О = Н 2 СО 3
Получение: SiO 2 + H 2 O = нельзя
Нестойкая, непрочная, при стоянии или нагревании разлагается:
Н 2 СО 3 = СО 2 + Н 2 О
Выделить в чистом виде нельзя, т.к. при нагревании разлагается:
H 2 SiO 3 = SiO 2 + H 2 O
Zn + H 2 CO 3 = ZnCO 3 + H 2
Незначительное выделение газа
__________
![СОЛИ A 3 B 2 [SiO 4 ] 3 , где A – кальций, магний, железо(II) ; B – алюминий, хром, железо(III) Топаз Al 2 [SiO 4 ] (F,OH) 2 Угольной кислоты - карбонаты; - гидрокарбонаты; Кремниевой кислоты Карбонаты обладают всеми свойствами солей, являются сильными электролитами, полностью диссоциируют на ионы(растворимых в воде). - силикаты; Растворимыми являются только соли щелочных металлов, остальные образуют нерастворимые или вообще не образуют солей( Al +3 , Cr +3 , Ag + ) .](https://static.multiurok.ru/multiurok/html/2020/04/02/s_5e8609f11f1f9/img10.jpg)
СОЛИ
A 3 B 2 [SiO 4 ] 3 , где A – кальций, магний, железо(II) ; B – алюминий, хром, железо(III)
Топаз Al 2 [SiO 4 ] (F,OH) 2
Угольной кислоты
- карбонаты;
- гидрокарбонаты;
Кремниевой кислоты
Карбонаты обладают всеми свойствами солей, являются сильными электролитами, полностью диссоциируют на ионы(растворимых в воде).
- силикаты;
Растворимыми являются только соли щелочных металлов, остальные образуют нерастворимые или вообще не образуют солей( Al +3 , Cr +3 , Ag + ) .
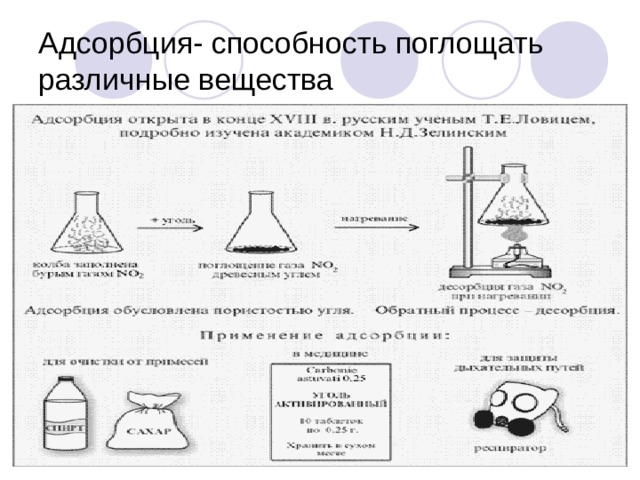
Адсорбция- способность поглощать различные вещества

Применение адсорбции
- Современные адсорбционные колонны применяют для очистки спиртов, сахара, осушения и очистки различных газов от примесей и водяных паров, а также для получения особо чистых веществ.

Изобретение, которое спасло тысячи жизней.
- В 1915 году русский химик-органик, академик АН СССР Николай Дмитриевич Зелинский совместно с инженером
А. Кумантом, основываясь на адсорбционных свойствах древесного угля, изобрел противогаз .

Демонстрация № 8 Поглощение активированным углем растворенных веществ (адсорбция) .
https://www.youtube.com/watch?time_continue=11&v=OJ3AvNHJXUo&feature=emb_logo

















![СОЛИ A 3 B 2 [SiO 4 ] 3 , где A – кальций, магний, железо(II) ; B – алюминий, хром, железо(III) Топаз Al 2 [SiO 4 ] (F,OH) 2 Угольной кислоты - карбонаты; - гидрокарбонаты; Кремниевой кислоты Карбонаты обладают всеми свойствами солей, являются сильными электролитами, полностью диссоциируют на ионы(растворимых в воде). - силикаты; Растворимыми являются только соли щелочных металлов, остальные образуют нерастворимые или вообще не образуют солей( Al +3 , Cr +3 , Ag + ) .](https://static.multiurok.ru/multiurok/html/2020/04/02/s_5e8609f11f1f9/img10.jpg)














