
Ароматические
углеводороды.
Углубленный уровень
10 класс

План урока
- 1.Общая формула и номенклатура.
- 2.Строение молекул.
- 3. Изомерия, гомология.
- 4. Физические свойства
- 5. Химические свойства.
- 6. Получение.

Общая формула
Арены – углеводороды, в молекулах которых содержится одно или несколько бензольных колец.
Общая формула
гомологического ряда:
Где n≥6
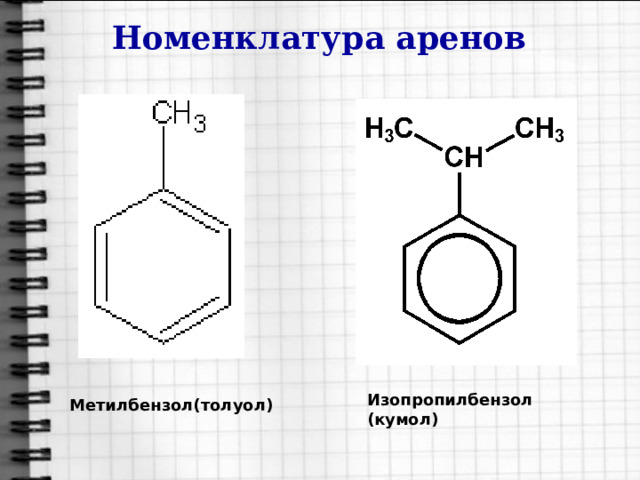
Номенклатура аренов
Изопропилбензол (кумол)
Метилбензол(толуол)
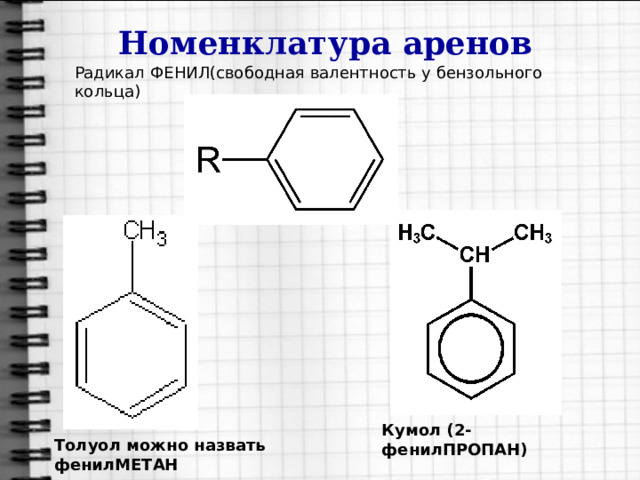
Номенклатура аренов
Радикал ФЕНИЛ(свободная валентность у бензольного кольца)
Кумол (2-фенилПРОПАН)
Толуол можно назвать фенилМЕТАН
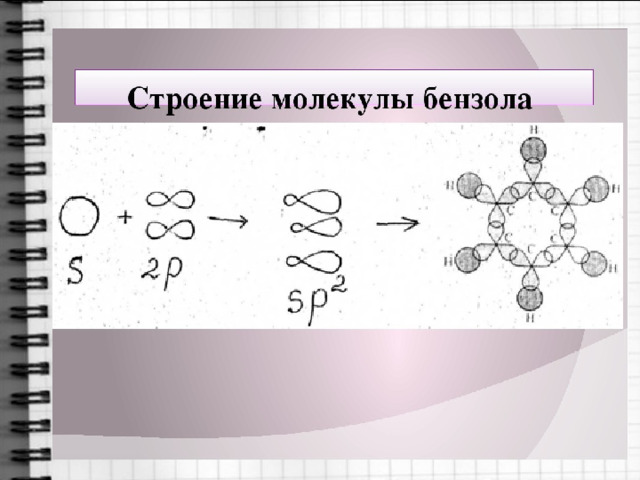
Строение молекулы бензола

Строение молекулы бензола
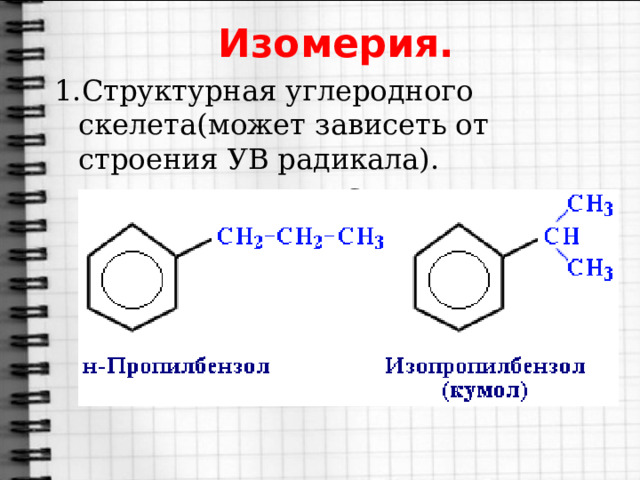
Изомерия.
1.Структурная углеродного скелета(может зависеть от строения УВ радикала).
С 9 Н 12

Структурная
(от положения заместителей в бензольном кольце).
цц
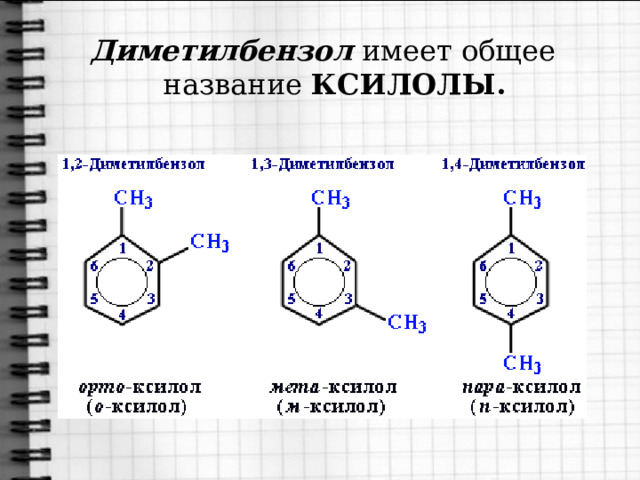
Диметилбензол имеет общее название КСИЛОЛЫ.

Фенил Бензил
Бензил имеет свободную валентность у метильной группы заместителя

ФИЗИЧЕСКИЕ СВОЙСТВА

Физические свойства
- Бензол – легкокипящая ( t плав = 5,5°С; t кип = 80°С), бесцветная жидкость с характерным запахом, не растворяется в воде
- Внимание! Бензол – яд, действует на почки, изменяет формулу крови (при длительном воздействии), может нарушать структуру хромосом.
- Большинство ароматических углеводородов опасны для жизни, токсичны.

Физические свойства
Ближайшие гомологи бензола также являются жидкостями, не растворимыми в воде.
С увеличением молярной массы повышается t кип соединений ряда бензола, причем
орто-изомеры кипят при более высокой t , чем пара-изомеры.

Химические свойства.
1 группа.
Реакции ЗАМЕЩЕНИЯ.
1.Галогенирование.(ионный механизм)

Реакция происходит с молекулярным бромом; при нагревании
C 6 H 5 -CH 3 + Cl 2 AlCl3 → ( смесь орта, пара производных ) + HCl
C 6 H 5 -CH 3 + Cl 2 hν → C 6 H 5 -CH 2 -Cl + HCl

2. Нитрование бензола.

3. Нитрование толуола
- C 6 H 5 -CH 3 + 3HO-NO 2 t, H2SO4 → СH 3 -C 6 H 2 (NO 2 ) 3 + 3H 2 O
2,4,6-тринитротолуол
(тол, тротил)

4. Алкилирование бензола галогеноалканами. Реакция Фриделя-Крафтса

5. Алкилирование алкенами.

2 группа. Реакции присоединения. 6. Гидрирование.

7. Хлорирование.
(по радикальному механизму)
8. Полимеризация.

3 группа. Окисление.
- Бензол не окисляется даже под действием сильных окислителей (KMnO 4 , K 2 Cr 2 O 7 и т.п.). Поэтому он часто используется как инертный растворитель при проведении реакций окисления других органических соединений. Бензол при обычных условиях не обесцвечивает бромную воду и водный раствор марганцовки!
- В отличие от бензола его гомологи окисляются довольно легко.
- При действии раствора KMnO 4 и нагревании в гомологах бензола окислению подвергаются только боковые цепи:

9. Окисление в кислой среде – до бензойной кислоты
Гомологи, содержащие две боковые цепи, дают двухосновные кислоты:
5C 6 H 5 -C 2 H 5 + 12KMnO 4 + 18H 2 SO 4 → 5C 6 H 5 COOH + 5CO 2 + 6K 2 SO 4 + 12MnSO 4 +28H 2 O
5C 6 H 5 -CH 3 + 6KMnO 4 + 9H 2 SO 4 → 5C 6 H 5 COOH + 3K 2 SO 4 + 6MnSO 4 +14H 2 O
Упрощённо:
C 6 H 5 -CH 3 + 3O KMnO4 → C 6 H 5 COOH + H 2 O


10. Окисление в нейтральной и слабощелочной среде
- Гомологи бензола могут быть окислены раствором перманганата калия в нейтральной среде до бензоата калия:
- C 6 H 5 CH 3 +2KMnO 4 = C 6 H 5 COOK + 2MnO 2 + + KOH + H 2 O (при кипячении)
- C 6 H 5 CH 2 CH 3 + 4KMnO 4 = C 6 H 5 COOK +
+ K 2 CO 3 + 2H 2 O + 4MnO 2 + KOH
(при нагревании)

7. Горение (полное окисление).
Бензол и его гомологи на воздухе горят коптящим пламенем, что обусловлено высоким содержанием углерода в их молекулах:
Бензол и его летучие гомологи образуют с воздухом и кислородом взрывоопасные смеси.

Получение аренов
В лаборатории
1. Сплавление солей бензойной кислоты с твёрдыми щелочами
C 6 H 5 -COONa + NaOH t → C 6 H 6 + Na 2 CO 3
бензоат натрия
2. Реакция Вюрца-Фиттинга : (здесь Г – галоген)
С 6 H 5 - Г + 2 Na + R- Г → C 6 H 5 -R + 2Na Г
С 6 H 5 -Cl + 2Na + CH 3 -Cl → C 6 H 5 -CH 3 + 2NaCl

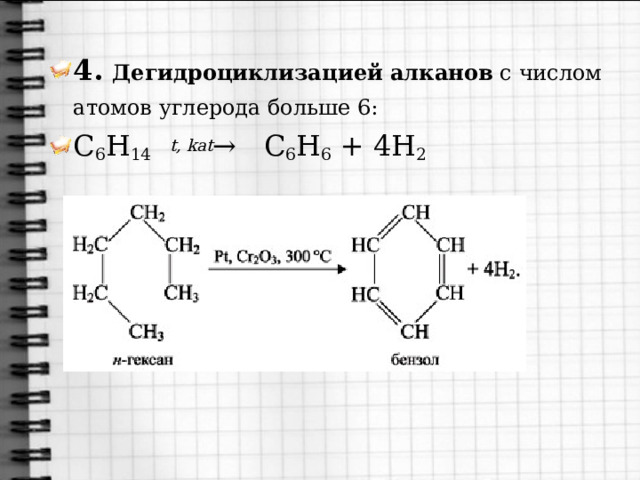
- 4. Дегидроциклизацией алканов с числом атомов углерода больше 6:
- C 6 H 14 t, kat → C 6 H 6 + 4H 2

5 . Тримеризация ацетилена (только для бензола) –
реакция Зелинского :
3 С 2 H 2 600°C, акт. уголь → C 6 H 6
6. Дегидрированием циклогексана и его гомологов:
Советский академик Николай Дмитриевич Зелинский установил, что бензол образуется из циклогексана (дегидрирование циклоалканов
C 6 H 12 t, kat → C 6 H 6 + 3H 2
C 6 H 11 -CH 3 t, kat → C 6 H 5 -CH 3 + 3H 2
метилциклогексан толуол

Применение бензола и его гомологов.
- Бензол C 6 H 6 – хороший растворитель. Бензол в качестве добавки улучшает качество моторного топлива. Служит сырьем для получения многих ароматических органических соединений – нитробензола C 6 H 5 NO 2 (растворитель, из него получают анилин), хлорбензола C 6 H 5 Cl, фенола C 6 H 5 OH, стирола и т.д.

Применение бензола и его гомологов.
- Толуол C 6 H 5 –CH 3 – растворитель, используется при производстве красителей, лекарственных и взрывчатых веществ (тротил (тол), или 2,4,6-тринитротолуол ТНТ).

Применение бензола и его гомологов.
- Ксилолы C 6 H 4 (CH 3 ) 2 . Технический ксилол – смесь трех изомеров ( орто -, мета - и пара -ксилолов) – применяется в качестве растворителя и исходного продукта для синтеза многих органических соединений.

Применение бензола и его гомологов.
- Изопропилбензол C 6 H 5 –CH(CH 3 ) 2 служит для получения фенола и ацетона.

Применение бензола и его гомологов.
- Хлорпроизводные бензола используют для защиты растений. Так, продукт замещения в бензоле атомов Н атомами хлора – гексахлорбензол С 6 Сl 6 – фунгицид; его применяют для сухого протравливания семян пшеницы и ржи против твердой головни. Продукт присоединения хлора к бензолу – гексахлорциклогексан (гексахлоран) С 6 Н 6 Сl 6 – инсектицид; его используют для борьбы с вредными насекомыми. Упомянутые вещества относятся к пестицидам – химическим средствам борьбы с микроорганизмами, растениями и животными.

Применение бензола и его гомологов.
- Стирол C 6 H 5 – CH = CH 2 очень легко полимеризуется, образуя полистирол, а сополимеризуясь с бутадиеном – бутадиенстирольные каучуки.




















































